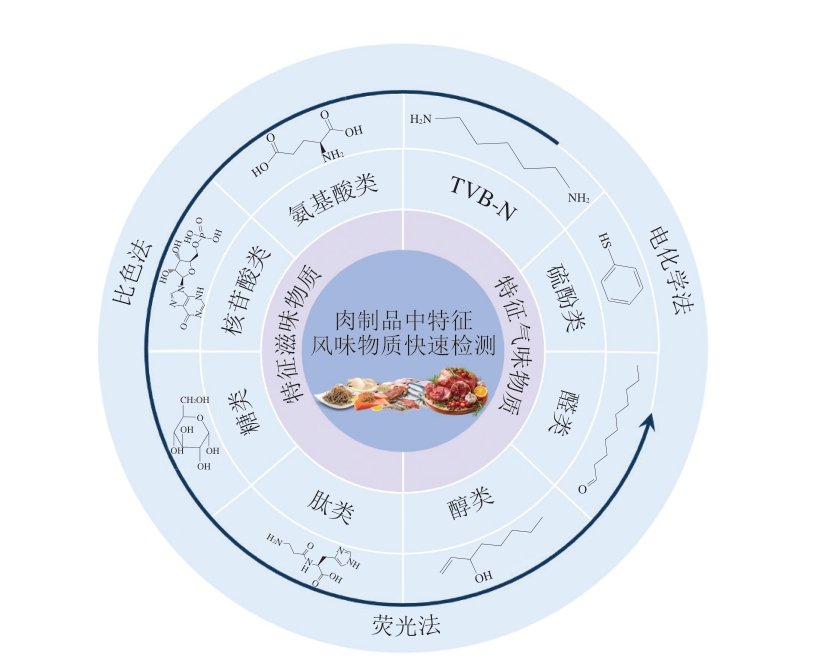
图1 肉制品中特征风味物质快速检测技术的研究框架
Fig. 1 Research framework for the rapid detection technologies of characteristic flavor compounds in meat products
TVB-N.总挥发性盐基氮(total volatile basic nitrogen)。
Advances in Rapid Detection Technologies and Their Applications for Characteristic Flavor Compounds in Meat Products
石佳慧, 黄家硕, 杨薇熹, 等. 肉制品中特征风味物质快速检测技术及应用研究进展[J]. 肉类研究, 2026, 40(5): 90-99.DOI:10.7506/rlyj1001-8123-20250617-185. http://www.rlyj.net.cn
SHI Jiahui, HUANG Jiashuo, YANG Weixi, et al. Advances in rapid detection technologies and their applications for characteristic flavor compounds in meat products[J]. Meat Research, 2026, 40(5): 90-99. (in Chinese with English abstract)DOI:10.7506/rlyj1001-8123-20250617-185. http://www.rlyj.net.cn
肉制品风味是决定消费者接受度和产品市场竞争力的关键因素之一。风味物质的检测不仅是食品品质控制的关键环节,而且更关联食品安全风险控制及产品真实性验证[1]。传统仪器分析方法,如气相色谱(gas chromatography,GC)、液相色谱(liquid chromatography,LC)及其与质谱(mass spectrometry,MS)的联用技术,虽具有高灵敏度和准确性,但存在设备昂贵、操作复杂、耗时长等不足,难以满足现场快速检测需求。因此,开发快速、简便、便携的检测方法成为当前食品风味检测领域的重要研究方向。
随着功能材料和传感技术的发展,基于比色法、荧光法和电化学法等检测平台构建的特异性传感系统在食品风味物质检测应用中取得显著进展。这些快速检测方法区别于传统仪器分析方法,不依赖色谱分离过程,具有操作简便、响应快速等优势,在食品风味物质检测中表现出良好的适用性,逐渐成为传统仪器检测的有效补充。然而,由于省略了分离步骤,这类方法在特异性识别方面存在不足,特别是在复杂食品基质和多组分共存的条件下更易受到干扰,难以精准识别目标物质,这对传感系统中识别元件的特异性提出了更高要求[2]。此外,许多关键风味物质含量极低,对检测灵敏度要求极高,而现有技术在痕量分析能力方面尚有不足。同时,快速检测技术的商品化和普及化仍面临成本高、设备复杂等问题,这也限制了其在实际生产中的应用[3]。
本文系统综述近年来基于比色法、荧光法、电化学法等检测平台开发的特异性传感系统在肉制品特征风味物质检测中的应用进展,详细介绍其检测原理及具体应用(图1)。同时探讨当前快速检测技术面临的挑战,并展望通过新型传感器设计、大数据融合等方向提升快速检测技术性能和应用范围的前景,旨在为肉制品中风味物质快速检测技术的发展提供理论参考和研究思路。

图1 肉制品中特征风味物质快速检测技术的研究框架
Fig. 1 Research framework for the rapid detection technologies of characteristic flavor compounds in meat products
TVB-N.总挥发性盐基氮(total volatile basic nitrogen)。
特征风味物质作为衡量食品品质、安全性及真实性的重要指标,在食品检测与监测中发挥着关键作用。目前,风味物质的定性与定量检测主要依赖于色谱分离及与MS联用技术。在风味物质检测中,GC作为常用技术,尤其在肉类挥发性风味成分检测方面表现突出,可有效分离和检测醛类、酮类、醇类、短链脂肪酸和内酯等挥发性化合物[4],具有分离速率快、灵敏度高等优势。Wang Yanke等[5]采用GC-嗅觉技术结合气味活度值分析从鸡肉中鉴定出8 种特征香气物质,不仅明确了鸡肉基础特征香气成分,还识别出不同品种鸡肉的特有香气物质,为品种识别与品质评价提供了依据。然而,GC不适用于热不稳定物质分析[6],且其定性分析依赖于标准品,难以鉴定未知物。相比之下,LC在分析热不稳定性化合物方面具有优势[7],尤其适用于氨基酸、有机酸及部分小分子风味前体检测[8],已成为补充GC不足的重要手段。然而,该方法也存在诸多局限,如分离效率相对较低、分析耗时较长、仪器设备成本较高,以及检测器特异性较强、对目标物质结构和性质依赖性较大。
MS技术因其出色的结构解析能力和多组分同时定量分析能力,通过与GC或LC联用,不仅可实现复杂样品中风味成分的高效分离与痕量检测,还可提供准确定性的分子质量和结构信息,广泛应用于风味成分鉴定、产品溯源与质量控制[9]。GC-MS和LC-MS等联用技术结合了色谱的分离能力与MS的结构鉴定优势,已成为当前风味物质检测的主流手段,为复杂食品基质中风味物质的全面解析提供了有力支持。近年来,随着分析技术的持续进步,色谱-MS系统亦不断更新迭代,涌现出一系列高性能的新型检测手段。例如,全二维GC凭借更强的分离能力能够高效解析传统GC难以分离的复杂风味组分,尤其在痕量物质分辨中表现优异[10]。超高效液相色谱技术在提升分离效率和缩短分析时间方面具有显著优势[11],广泛应用于复杂风味物质及其代谢产物的快速检测。此外,离子迁移谱(ion mobility spectrometry,IMS)作为一种新型MS分析技术,凭借分离效率高、灵敏度高及可在线监测等优势,在肉类新鲜度现场快速检测中展现出良好应用前景[12]。然而,单独使用IMS存在选择性不足、易受复杂食品基质干扰等不足,且对同分异构体分离能力有限,需依赖标准品进行化合物鉴定;与色谱、MS联用时产生的多维数据解析复杂,缺乏通用自动化处理软件,且仪器参数差异导致数据重复性不足[13],其在实际应用中仍面临挑战。
尽管色谱-MS联用技术在风味物质分析中仍占据主导地位,但其设备昂贵,且常因食品基质复杂而需要复杂的前处理步骤,导致检测周期较长,难以满足现场快速检测需求[14]。因此,研究者积极探索更高效、便捷的快速检测技术(图2)。与传统色谱-MS方法相比,快速检测技术省略了分离步骤,具有高效性和便捷性等优势,逐渐成为风味物质现场检测和预警监测的重要补充。快速检测技术是一类新兴检测策略,其基于特定检测平台引入具有靶向识别能力的传感元件,如特异性识别分子、功能纳米材料等,通过其与风味物质发生特异性反应所产生的信号变化,实现目标化合物的定性或定量检测,当前常用的快速检测方法主要包括比色法、荧光法和电化学法(图2)。比色法通过化学响应染料与分析物反应产生颜色变化,可借助比色传感器阵列实现原位可视化检测,具有无需复杂仪器、检测范围广、成本低和可实现多重分析等优势。然而,其检测结果的准确性仍有待提升[15]。荧光法通过特殊设计荧光分子探针与风味物质作用后产生荧光强度或颜色变化实现定性与定量分析[16],具有响应快速、操作简便和灵敏度高等优势,但也面临探针稳定性差、检测范围受限等问题,制约其进一步应用。电化学法则通过测定风味物质与电极表面相互作用过程中产生的电流、电位或电化学发光信号变化实现定性与定量分析,其关键在于电极材料的选择和传感界面的构建。近年来,基于电化学的多类型传感器如酶传感器、免疫传感器逐渐兴起,为风味物质的快速检测提供了新思路,该方法具有反应灵敏、响应迅速、成本较低等特点,但在特异性和抗干扰能力方面仍需进一步优化[17]。因此,快速检测方法为食品风味物质检测提供了新思路,尤其为食品实时监控与溯源提供了解决方案,有助于更高效、精准地解析食品中的风味物质。
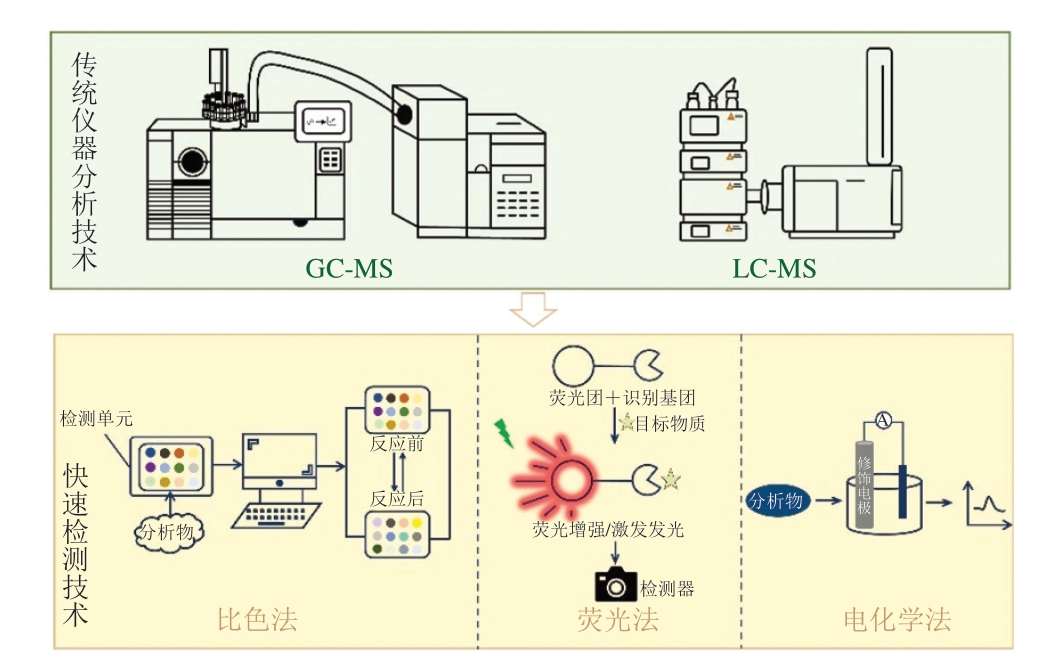
图2 风味化合物的传统仪器分析与快速检测技术
Fig. 2 Traditional instrumental analysis and rapid detection techniques for flavor compounds
肉制品中特征滋味物质主要包括氨基酸、核苷酸、肽类及糖类等非挥发性风味成分。这些物质不仅赋予肉类鲜味、甜味或苦味等基本风味特征,还通过与其他风味组分的协同作用显著影响整体风味的层次与协调性[18]。此外,滋味物质广泛参与美拉德反应、Strecker降解及氨基酸代谢等风味生成途径,是肉类风味形成的重要前体[19]。由于其在风味呈现、品质判定及产品溯源等方面具有重要作用,对其进行快速、准确检测已成为当前肉类食品分析领域的研究热点。
氨基酸具有直接呈味作用,包括鲜味氨基酸(如谷氨酸、天冬氨酸)、甜味氨基酸(如甘氨酸、丙氨酸)及苦味氨基酸(如精氨酸、苯丙氨酸)等[20]。此外,氨基酸也参与风味代谢途径,是美拉德反应和Strecker降解的关键参与者,在肉及肉制品风味形成过程中发挥关键作用[21]。因此,对食品中的氨基酸进行定量和定性检测具有重要意义。
电化学法因响应速率快、检测灵敏度高、传感设备成本低等优势,成为当前最常用的传感器类型,包括安培法、电位法、阻抗法、光电化学法和电致化学发光法等[22]。其中,安培传感器和电位传感器在氨基酸电化学法快速检测中应用最为广泛。Wang Xiaodan等[23]提出一种用于检测牛肉L-Glu含量的安培式电化学生物传感器。该传感系统以金电极为基底,通过依次修饰金纳米颗粒、氧化石墨烯和壳聚糖构建复合材料表面,为酶固定提供良好的生物相容性。经交联剂活化,将L-谷氨酸氧化酶(L-glutamate oxidase,GluOx)共价固定于复合材料表面,可实现对L-Glu的特异性识别。在识别过程中,GluOx催化L-Glu氧化生成α-酮戊二酸、氨和H2O2,H2O2在电极表面进一步发生氧化还原反应为并转化为电信号。由于H2O2生成量与L-Glu浓度成正比,电流响应强度可用于定量L-Glu含量。该传感器具有高灵敏度和选择性,多层功能材料的协同作用能够有效提升信号放大效果和电极稳定性,可确保检测准确性。在最佳条件下,其灵敏度和准确性与氨基酸分析仪相当,为2.3×10-5 mol/L。此外,Wang Xiaodan等[24]还构建了一种电位式电化学传感器,用于同步定量检测牛肉L-Glu与Asp。该传感器以铂电极(Pt)为基底,通过电聚合形成聚吡咯(polypyrrole,PPy)导电层,再浸渍含二苯基硫脲(N,N’-diphenylthiourea,DPTU)的聚氯乙烯(polyvinyl chloride,PVC)增塑膜,最终制备出DPTU/PVC/PPy/Pt工作电极。当L-Glu或Asp进入溶液时,其双羧基和α-氨基结构优先与DPTU的硫羰基及氮原子通过氢键-静电协同作用形成稳定复合物,该复合物在膜表面形成阻挡层,导致离子通道受阻,使识别前后界面电荷密度发生变化,从而引起开路电位负向移动,电位变化量与氨基酸浓度在1.0×10-5~1.0×10-3 mol/L范围内呈良好线性关系,检出限为1.2×10-6 mol/L,检测性能与氨基酸分析仪相当。
尽管电化学传感器展现出良好的定性与定量效果,但其存在电极易污染、使用寿命短等问题,且其检测时间较光学感传感器更长[25]。因此,荧光法被开发用于氨基酸的高灵敏度检测,尤其适合用于痕量风味物质的定量分析。Han Tingting等[26]开发出一种基于氮掺杂石墨烯量子点(nitrogen-doped graphene quantum dots,N-GQDs)的荧光传感系统,用于同步检测L-Glu和L-Asp。该探针由柠檬酸与尿素经一步水热法合成,其表面富含正电荷官能团,当带负电的L-Glu和L-Asp进入该体系后,通过静电作用与N-GQDs表面发生静态猝灭,引起荧光强度下降;加入Al3+后,其优先与L-Glu形成络合物,从而屏蔽其对N-GQDs的猝灭作用,而L-Asp仍可猝灭荧光,因此基于2 次荧光强度的变化即可实现L-Glu和L-Asp的同时定量检测。该探针对L-Glu和L-Asp的检测限分别为1.51×10-8 mol/L和2.09×10-8 mol/L,与氨基酸分析仪检测结果具有良好一致性。此外,有研究设计出一种基于咔唑-吡啶的荧光探针(carbazole-pyridine fluorescent probe,CPI),用于检测鸡胸肉、牛排等样品中的Cys。当Cys进入体系后会与CPI形成稳定产物CPI-Cys,从而阻断原有分子内电荷转移,导致吸收峰从372 nm蓝移至273 nm,荧光由“关闭”状态转变成“开启”状态。基于此机制,CPI探针可实现对Cys的快速、灵敏检测,其检出限低至3.8×10-6 mol/L[27]。
核苷酸类物质不仅影响肉制品鲜味[28],还与保水性等品质密切相关[29]。以肌苷一磷酸(inosine monophosphate,IMP)和鸟苷一磷酸(guanosine monophosphate,GMP)为例,其含量异常波动常引发风味缺陷:一方面,过量会导致鲜味过于浓烈,掩盖其他风味成分,使整体风味趋于单一;另一方面,可能诱发金属异味,破坏风味的协调与自然感。相反,含量不足则会导致鲜味显著减弱。
IMP是腺苷三磷酸的降解产物之一,其含量随肉类贮藏时间延长和品质劣变而逐渐下降,因而常作为评价肉类鲜度的重要指标[30]。为实现IMP的快速、灵敏检测,Wang Guangxian等[31]构建出一种基于3 层功能单元的双酶电化学生物传感器,其底层为滴涂Ti3C4Tx(MXene)-Au@Pt纳米花的玻碳电极(glassy carbon electrode,GCE),中层固定5′-核苷酸酶和黄嘌呤氧化酶,形成三明治式结构。当体系中存在IMP时,经双酶催化氧化生成H2O2,而H2O2在Au@Pt纳米花表面发生电化学氧化反应产生电子,并通过MXene快速传递至电极产生电流。H2O2浓度随IMP含量线性增加,可通过监测电流变化实现定量检测,其线性范围为1.15×10-4~4.88×10-2 mol/L,检测限为7.84×10-6 mol/L。随后,针对鲜肉中的IMP检测,Wang Guangxian等[32]又提出一种双酶电化学发光生物传感器,其构建思路与前述三明治式传感系统类似,不同之处在于将纳米材料替换为ZIF-67@AgNPs-鲁米诺复合材料,构建出GCE/ZIF-67@AgNPs-鲁米诺/纳米酶电化学发光一体化界面。IMP经双酶联合催化产生H2O2,其在ZIF-67@AgNPs-鲁米诺复合材料催化下可氧化鲁米诺生成激发态3-氨基邻苯二甲酸盐,并在其回到基态时发射蓝紫色光信号。该传感器在8.62×10-6~7.18×10-2 mol/L范围内表现出良好的线性响应,检测限为4.88×10-6 mol/L,已成功应用于实际肉类样品检测。类似地,另有研究[33]利用Pt、二维多孔石墨炔、金纳米颗粒、鲁米诺、5′-核苷酸酶和黄嘌呤氧化酶构建多功能检测界面,基于相同的光信号原理实现肉类中IMP的快速、灵敏、特异性检测。鉴于纳米酶电化学生物传感器存在催化活性较低、对生物组分依赖性强等局限[34],研究者开发出非酶催化技术以提升传感器在实际应用中的适用性与经济性。Fei Qiqi等[35]提出一种新型非酶传感器,用于测定肉类中GMP并评估其品质。该传感系统以石墨相氮化碳(graphitic carbon nitride,g-C3N4)掺杂羧基化多壁碳纳米管的纳米复合材料为核心,通过简单的一步法合成。在未结合GMP时,g-C3N4掺杂的纳米复合材料表现出良好的电导性,电流响应较高。当GMP与纳米复合材料结合后,由于GMP分子的电荷分布和空间位阻效应,电子转移受阻,导致电流响应显著降低。这种电流变化与GMP浓度在1.38×10-9~2.75×10-4 mol/L范围内呈线性关系,检出限低至3.0×10-10 mol/L。综上,非酶传感器具有成本低、检测限低和抗干扰能力强等优势。
除电化学外,高田毅等[36]构建出一种基于柠檬酸-铕纳米配位聚合物的荧光探针,用于快速检测肉汤煲中IMP含量。该探针与IMP结合时,由于—OH的伸缩振动导致振动波和发射波重叠,从而猝灭探针的蓝色荧光信号,该探针线性范围为7.18×10-9~5.74×10-4 mol/L,检出限为4.88×10-10 mol/L。
在食品体系中,肽类物质不仅作为代谢途径的中间产物参与风味前体的生成,还在增强食品风味强度与复杂性方面发挥重要作用。例如,在海鲜风味制品中,肽类可与含硫挥发性化合物协同作用,显著增强海鲜特征风味的感官表现[37]。此外,肽类在肉类来源鉴别中具有重要价值。不同来源的肉类在酶解、代谢及加工过程中形成的肽类物质在种类、含量及比例上均表现出特异性[38],可为溯源识别提供理论依据和技术支撑。因此,开发快速、准确的肽类物质分析方法,对肉类产品溯源、防范食品欺诈及维护市场交易的公正性与规范性具有重要的现实意义。
目前,肽类物质的快速检测以电化学法为主,荧光法和比色法的应用尚不多见。这主要是由于肽类分子结构多样、极性较强,且多数不具备天然的发色或荧光基团,难以直接参与比色或荧光反应。相比之下,电化学法因不依赖肽类的光学性质,且可通过构建功能化电极材料实现对目标分子的高选择性识别,显示出更强的适应性与应用优势。Jozanović等[39]提出一种基于微芯片电泳结合电容耦合非接触式电导检测器(capacitively coupled contactless conductivity detector,C4D)的传感系统,用于检测肉类中的咪唑二肽(肌肽和鹅肌肽)。该方法的识别基于二肽在酸性条件下带正电荷并在电场中向阴极迁移的特性,结合其等电点差异实现有效区分。当二肽通过检测区域时,电极间电导变化被C4D检测器转化为可量化的电流信号,信号强度与分析物浓度呈良好的线性关系,检测限分别为3.80×10-8 mol/L(肌肽)和4.79×10-8 mol/L(鹅肌肽)。该方法已成功应用于肉及肉制品、饲料中动物二肽的检测、物种鉴定和定量分析,在食品检测和防伪领域展现出应用潜力。
肉制品中糖类物质(如葡萄糖、糖原、核糖等)含量直接影响肉品色泽、嫩度及持水性等品质特性[40]。其中,葡萄糖含量常被视为评估肉类新鲜度的重要指标[41]。电化学传感器因糖类氧化酶易固定于电极表面形成酶基传感器及产业成熟等优势在糖类检测中占据主导地位。Umuhumuza等[41]开发出一种基于L-Cys修饰金电极的葡萄糖传感器,其以表面修饰L-Cys的金电极为基底,通过静电相互作用将聚谷氨酸-葡萄糖氧化酶复合物固定于修饰后的电极表面,构建出具有生物识别功能的传感界面。在检测过程中,当肉类样品中的葡萄糖与葡萄糖氧化酶接触时,该酶催化葡萄糖氧化生成葡萄糖酸和H2O2,在极化电压下,H2O2在电极表面发生氧化反应生成电子,电子转移引起电流变化并形成可测电信号。随着葡萄糖浓度的升高,催化反应速率加快,H2O2生成量增加,电极电流响应增强,从而实现葡萄糖的定量检测。
肉及肉制品中特征滋味物质的快速检测方法如表1所示。
表1 快速检测技术在肉及肉制品特征滋味物质检测中的应用
Table 1 Application of rapid detection technologies in the detection of characteristic taste compounds in meat and meat products
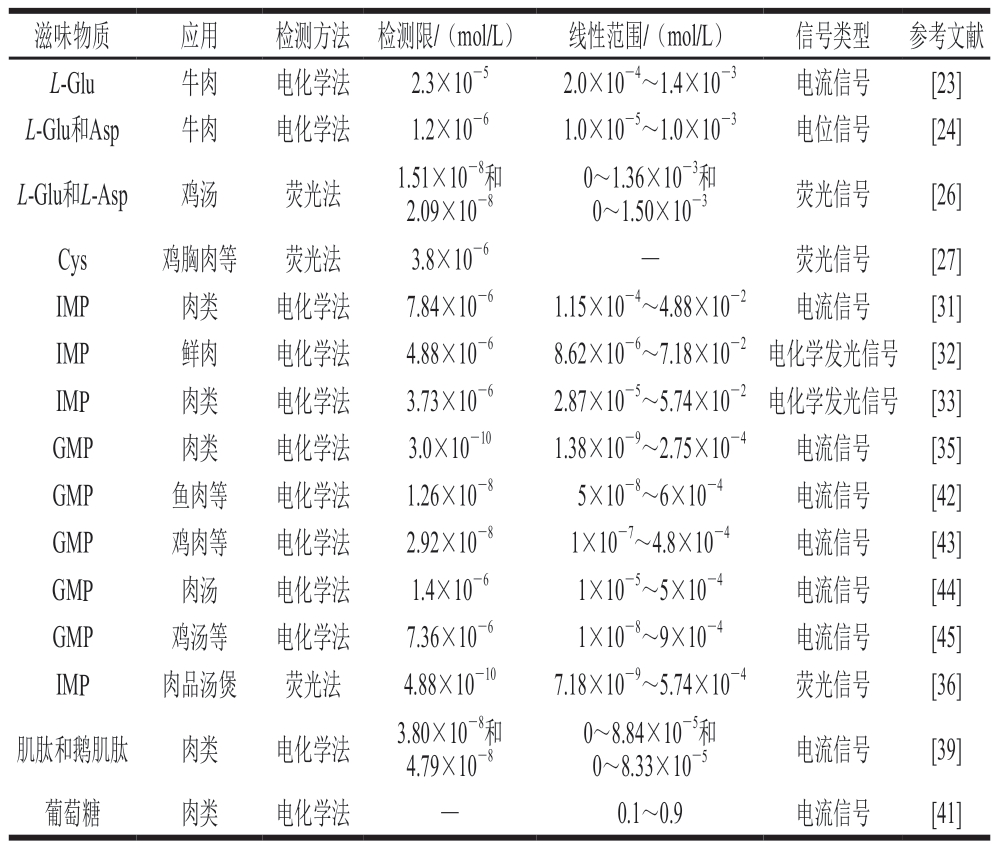
注:—.文献未提及。表2同。
滋味物质应用检测方法检测限/(mol/L)线性范围/(mol/L)信号类型参考文献L-Glu牛肉电化学法2.3×10-52.0×10-4~1.4×10-3电流信号[23]L-Glu和Asp牛肉电化学法1.2×10-61.0×10-5~1.0×10-3电位信号[24]L-Glu和L-Asp鸡汤荧光法1.51×10-8和2.09×10-8 0~1.36×10-3和0~1.50×10-3荧光信号[26]Cys鸡胸肉等荧光法3.8×10-6—荧光信号[27]IMP肉类电化学法7.84×10-61.15×10-4~4.88×10-2电流信号[31]IMP鲜肉电化学法4.88×10-68.62×10-6~7.18×10-2电化学发光信号[32]IMP肉类电化学法3.73×10-62.87×10-5~5.74×10-2电化学发光信号[33]GMP肉类电化学法3.0×10-101.38×10-9~2.75×10-4电流信号[35]GMP鱼肉等电化学法1.26×10-85×10-8~6×10-4电流信号[42]GMP鸡肉等电化学法2.92×10-81×10-7~4.8×10-4电流信号[43]GMP肉汤电化学法1.4×10-61×10-5~5×10-4电流信号[44]GMP鸡汤等电化学法7.36×10-61×10-8~9×10-4电流信号[45]IMP肉品汤煲荧光法4.88×10-107.18×10-9~5.74×10-4荧光信号[36]肌肽和鹅肌肽肉类电化学法3.80×10-8和4.79×10-8 0~8.84×10-5和0~8.33×10-5电流信号[39]葡萄糖肉类电化学法—0.1~0.9电流信号[41]
挥发性风味物质作为肉制品风味及腐败程度的重要感官指标,因其能够在微量条件下引发显著的气味变化受到广泛关注[19]。随着分析检测技术的进步,荧光探针、比色传感器、气敏元件及智能识别算法等多种方法被应用于挥发性风味物质快速检测,显著提升了肉类新鲜度评价的灵敏性与便携性。这些检测方法不仅具有高效性,还具有良好的可视化潜力,适用于现场实时监测。
TVB-N是动物性食品在酶和微生物作用下发生腐败而产生的氨、二甲胺、三甲胺等挥发性碱性含氮化合物的总和[46]。其含量增加通常反映蛋白质(尤其是蛋氨酸与酪氨酸)剧烈降解,将导致食品安全性与风味品质下降。因此,TVB-N含量是评估鱼类及肉类新鲜度的重要指标[47]。
鉴于传统TVB-N检测方法存在样品处理繁琐、检测周期长及潜在环境污染等问题,近年来针对TVB-N的快速检测技术得到广泛应用[48]。其中,荧光法和比色法是当前主流手段。Li Min等[49]开发出一种基于黄酮类化合物的荧光传感器阵列,用于肉类新鲜度无损检测。该传感器阵列将黄酮类化合物与柔性薄膜复合,当氨气与黄酮类化合物接触时,其分子结构中的酚羟基发生离子化,导致荧光增强。通过智能手机拍摄图像并捕捉与记录荧光强度变化,利用深度卷积神经网络模型分析图像数据,从而实现对肉类新鲜度的智能分类和识别。随着肉类新鲜度的降低,包装内氨气浓度增加,黄酮类化合物的荧光响应也随之增强,最终通过模型预测实现对肉类新鲜度的实时、无损监测。另有研究[50]构建出一种比率荧光试纸,该传感系统以芥末色荧光的D-青霉胺包覆的银纳米簇(D-penicillamine capped silver nanoclusters,DPA-AgNCs)作为指示剂,红色发光的双金属金/银纳米簇作为内参构建而成。在检测过程中,当海鲜包装中的挥发性碱性氮(volatile basic nitrogens,VBNs)与DPA-AgNCs接触时,DPA-AgNCs荧光强度发生变化,导致试纸荧光颜色从芥末色变为深红色。这种荧光强度变化由VBNs与DPA-AgNCs之间的动态猝灭机制引起。随着VBNs浓度的增加,荧光猝灭程度加剧,试纸颜色变化也更加明显。该试纸具有较高的灵敏度,对NH3的检测限为4.7×10-6 mol/L。在比率型传感平台方面,Huang Xiaowei等[51]设计的便携式纸基传感器可实现NH3定量检测,并可利用智能手机对鸡肉新鲜度进行可视化实时监控。该荧光纸基传感器有效简化肉类新鲜度监测过程,同时还可确保准确性和稳定性。此外,Zhou Chenyue等[52]也提出一种基于自组装铜纳米团簇的荧光传感器,该方法以p-巯基苯甲酸为配体,合成的传感器在酸性条件下形成有序纳米片结构并发出橙色荧光。当VBNs与该传感器接触时,荧光强度逐渐减弱;随着VBNs浓度的增加,荧光强度进一步降低直至消失。基于此开发的便携式荧光标签可实现海鲜新鲜度的半定量、可视化和实时监测,该技术在TVB-N检测方面展现出高灵敏度和准确性。
除荧光传感器外,比色传感器作为一种快速、无损检测技术,在肉类新鲜度监测中同样受到广泛关注。Xu Weidong等[53]将比色传感器阵列(colorimetric sensor array,CSA)与仿生算法相结合,构建出一种简便的TVB-N含量测定平台。首先,制备含有12 种颜色敏感材料的CSA,用于采集牛肉气味信息并生成可视化气味指纹;其次,采用4 种仿生优化算法从CSA中提取特征指纹变量;最后,构建基于特征颜色成分的反向传播神经网络模型,实现牛肉贮藏过程中TVB-N含量的精准测定。该技术在TVB-N含量测定和肉类新鲜度评价中展现出快速、灵敏、便携等优势,但也面临环境干扰大、传感器稳定性不足等问题。未来应聚焦材料功能化与识别特异性提升,以推动该技术向智能化与实用化方向发展。
综上,TVB-N的挥发性使荧光法和比色法在检测过程中具备天然优势,相较于电化学法,这2 种方法在相关应用中展现出更高的实用性和普适性。
芳香硫酚类化合物(aromatic thiols,ArSHs)具有独特的香气特征和极低的气味阈值,即使微量存在时亦能被人类嗅觉系统感知。在熟肉制品中,适量苯硫酚(thiophenol,PhSH)及其衍生物可赋予产品独特的烘烤香气,增强风味层次感与复杂性。然而,PhSH同时具有显著的异味特征,易在加工不当或贮藏条件劣化的肉类中生成,影响产品感官品质。因此,硫酚类物质的快速、灵敏检测对肉类品质评价尤为关键。
目前,相关快速检测策略主要集中于荧光探针设计,这主要是因为硫酚类物质普遍具有较强的亲核性,易与荧光探针特定反应位点发生选择性化学反应,诱导荧光团发光行为变化,如启动或阻断内部电荷转移或分子内能量转移过程,实现荧光信号的“开-关”式响应[54]。Xu Ziyi等[55]构建的基于级联反应的高灵敏度荧光传感系统可实现肉制品和调味品中的硫酚类风味化合物检测。该系统的核心是小分子传感器通过与ArSHs反应实现信号转变。具体而言,该传感器与ArSHs相互作用时,首先发生亲核芳香取代反应,随后自发环化生成具有强绿色荧光发射的咪唑香豆素衍生物,实现从无荧光到强荧光的信号转变。这一级联反应机制不仅能够显著降低背景信号,还能够大幅缩短响应时间,使该传感系统兼具高灵敏度和快速响应能力。为实现比率荧光检测,研究者将该传感器与远红荧光化学探针结合构建了复合探针。在ArSHs存在时,复合探针呈现出从深红色到浅绿色的显著荧光颜色变化,通过荧光强度比值实现定量检测。此外,Lin Pengxu等[56]构建的用于检测PhSH的荧光传感系统由2 种荧光探针(CM-PhSH和CM-Ratio-PhSH)构成,二者均以具有优异光学性能的香豆素荧光团为基础,通过修饰烯烃不饱和键作为PhSH的反应位点。其中,CMRatio-PhSH还在特定位置引入硝基以实现比率型荧光检测。CM-PhSH通过PhSH亲核加成反应断裂共轭不饱和键,促使香豆素衍生物产生荧光发射,从而实现PhSH识别;CM-Ratio-PhSH则通过β位碳原子加成改变探针结构,导致共轭体系缩小并引发荧光发射波长偏移,基于该特征性光谱变化实现PhSH识别。这2 种探针对其他相关分析物几乎无响应,可确保识别准确性与特异性。
相较荧光法而言,电化学法在硫酚类物质检测中应用受限,这主要由于硫酚结构中的—SH基团易在电极表面发生非特异性吸附或被氧化生成二硫化物[57],导致电极表面污染与信号漂移,从而影响检测结果稳定性。比色法则因灵敏度不足,难以满足痕量、快速识别要求。
醛类化合物在食品风味形成过程中发挥关键作用,其种类与含量直接影响风味平衡与协调[58]。例如,壬醛具有柑橘与花香,2-辛烯醛带有坚果和烘烤气息,而丙二醛(malondialdehyde,MDA)则呈现出明显的酸败异味。目前,相关快速检测策略主要集中于荧光探针的设计与应用。Liu Xueting等[59]构建出一种简单的高尔基体靶向荧光探针,可同时检测生物体系和食品中的MDA和甲醛(formaldehyde,FA)。该探针以4-三氟甲基取代的7-氨基喹啉作为高尔基体靶向基团和荧光团,以肼基团作为识别位点。在识别过程中,该探针通过肼基团与MDA和FA发生特异性反应,实现对2 种分析物的区分和检测:MDA与肼基团反应生成吡唑结构,改变肼基团中仲氨基电子供体能力,抑制光诱导电子转移(photoinduced electron transfer,PET)和分子内电荷转移效应,导致荧光在424 nm波长处显著增强并蓝移;FA与氨基反应形成C=N双键,抑制PET效应,从而导致520 nm波长处荧光增强。基于反应机制和发射波长差异,探针能够在相同的激发条件下同时检测MDA和FA,且两者之间互不干扰。该传感系统兼具高灵敏度和特异性,可为生物体系和食品安全监测提供有效工具。类似地,另有研究[60]也基于醛类与肼的缩合反应阻断PET过程,开发出荧光探针MDA-6用于MDA检测。
在肉制品中,部分醇类物质具有润滑功能,可赋予产品顺滑口感并丰富其风味层次。作为食品风味的重要组成成分,醇类化合物因其较高挥发性可直接影响食品的整体气味特征。特定醇类的存在及其浓度变化可作为评价食品品质、新鲜度、真实性和安全性的指示性成分。例如,己醛与1-辛烯-3-醇已被确认为冷藏草鱼片新鲜度的重要标志物[61]。Siraj等[62]构建出一种气体传感器,用于检测红肉腐败过程中释放的挥发性有机化合物(volatile organic compounds,VOCs),特别是己醛、1-辛烯-3-醇和1-戊醇。该传感系统通过溶液混合和超声处理制备ZnO/WSe2纳米复合材料,并通过将其滴涂在聚对苯二甲酸乙二醇酯基底上构建传感器。在检测过程中,VOCs与传感器表面的氧离子反应释放电子,电子转移至ZnO/WSe2材料中,增加其自由载流子数量,导致电阻降低,电阻变化转化为电信号以实现VOCs定性与定量检测。由于结构特性和较低电离能,己醛在与表面氧离子反应时更易释放电子,因此在相同浓度下引发的传感器响应最强。单一气体和混合气体检测结果表明,该传感器对VOCs具有高灵敏度和选择性。
目前针对醇类(小分子挥发性物质)的检测仍主要依赖传统仪器分析方法,快速检测技术应用仍较少,这主要是因为其分子结构简单、缺乏可高效识别的官能团,在复杂食品基质中易受水分和脂类干扰,影响检测的灵敏度与准确性。此外,醇类物质分子质量较小、挥发性强,捕获难度大。未来需深入挖掘醇类物质的识别特征,设计高选择性的快速检测策略,以实现更精准的检测。
肉及肉制品中特征气味物质的快速检测方法如表2所示。
表2 快速检测技术在肉及肉制品特征气味物质检测中的应用
Table 2 Application of rapid detection technologies in the detection of characteristic odor compounds in meat and meat products
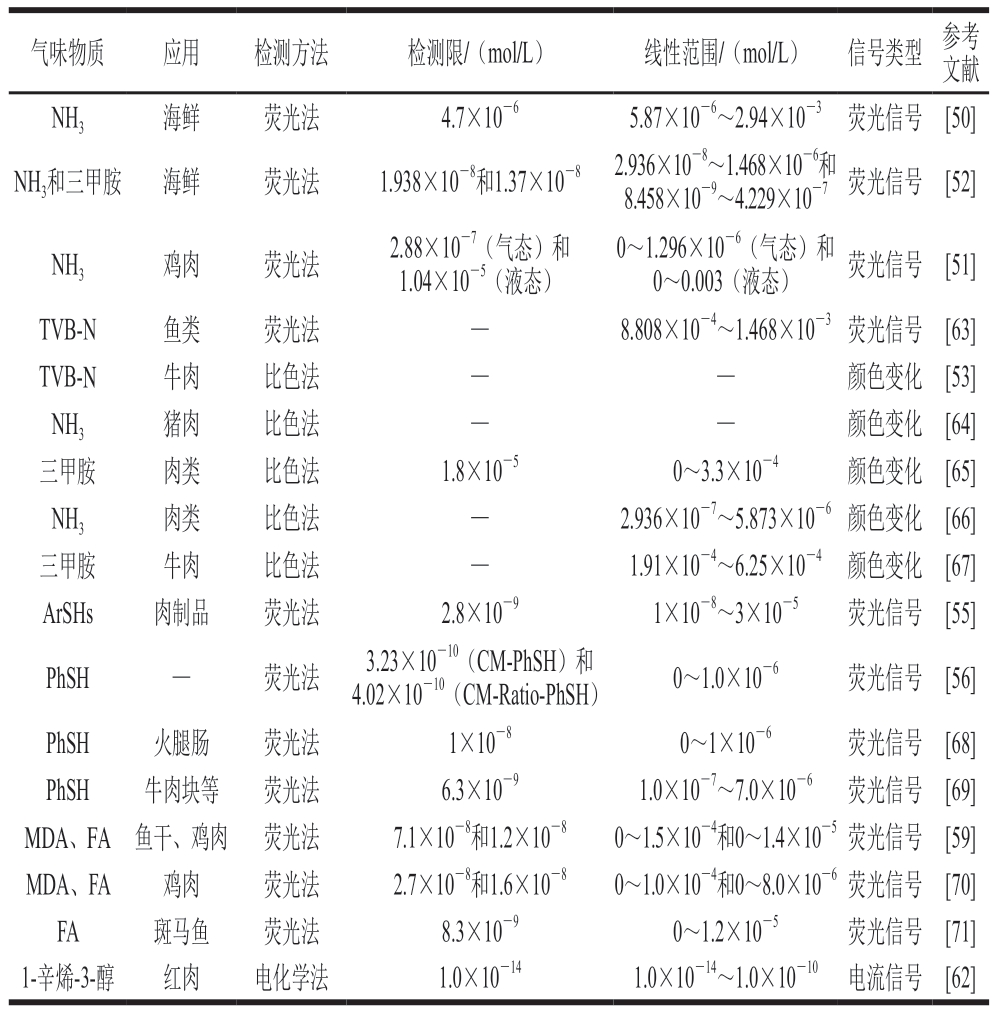
气味物质应用检测方法检测限/(mol/L)线性范围/(mol/L)信号类型参考文献NH3海鲜荧光法4.7×10-65.87×10-6~2.94×10-3荧光信号[50]NH3和三甲胺海鲜荧光法1.938×10-8和1.37×10-82.936×10-8~1.468×10-6和8.458×10-9~4.229×10-7荧光信号[52]NH3鸡肉荧光法2.88×10-7(气态)和1.04×10-5(液态)0~1.296×10-6(气态)和0~0.003(液态)荧光信号[51]TVB-N鱼类荧光法—8.808×10-4~1.468×10-3荧光信号[63]TVB-N牛肉比色法——颜色变化[53]NH3猪肉比色法——颜色变化[64]三甲胺肉类比色法1.8×10-50~3.3×10-4颜色变化[65]NH3肉类比色法—2.936×10-7~5.873×10-6颜色变化[66]三甲胺牛肉比色法—1.91×10-4~6.25×10-4颜色变化[67]ArSHs肉制品荧光法2.8×10-91×10-8~3×10-5荧光信号[55]PhSH—荧光法3.23×10-10(CM-PhSH)和4.02×10-10(CM-Ratio-PhSH)0~1.0×10-6荧光信号[56]PhSH火腿肠荧光法1×10-80~1×10-6荧光信号[68]PhSH牛肉块等荧光法6.3×10-91.0×10-7~7.0×10-6荧光信号[69]MDA、FA鱼干、鸡肉荧光法7.1×10-8和1.2×10-80~1.5×10-4和0~1.4×10-5荧光信号[59]MDA、FA鸡肉荧光法2.7×10-8和1.6×10-80~1.0×10-4和0~8.0×10-6荧光信号[70]FA斑马鱼荧光法8.3×10-90~1.2×10-5荧光信号[71]1-辛烯-3-醇红肉电化学法1.0×10-141.0×10-14~1.0×10-10电流信号[62]
表3 不同快速检测技术在肉制品风味物质检测中的性能比较
Table 3 Performance comparison of different rapid detection technologies for flavor compound detection in meat products
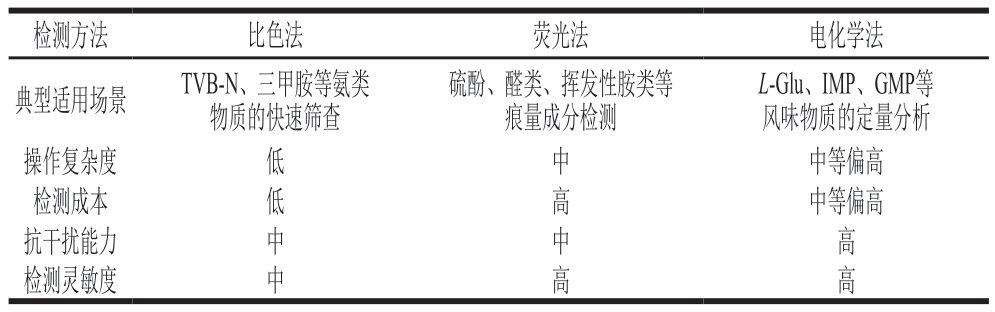
检测方法比色法荧光法电化学法典型适用场景TVB-N、三甲胺等氨类物质的快速筛查L-Glu、IMP、GMP等风味物质的定量分析操作复杂度低中中等偏高检测成本低高中等偏高抗干扰能力中中高检测灵敏度中高高硫酚、醛类、挥发性胺类等痕量成分检测
尽管肉制品中风味物质的快速检测技术已取得显著进展,但在实际应用中仍面临诸多挑战(图3)。首先,在特异性识别方面,食品基质复杂,常含有大量结构相似的同类物质,导致目标组分的精准识面临干扰问题。其次,在检测灵敏度方面,多种关键风味物质含量极低,现有部分检测技术难以实现对痕量物质的可靠检测,限制了对风味组分的全面解析。结合表1~3可知,电化学法在风味物质检测中展现出良好的灵敏度(最高可达10-10 mol/L),且在复杂基质中抗干扰能力强,适用于定量分析场景,但传感器构建较复杂,对材料与操作条件要求较高;荧光法在痕量气味物质检测中表现出优异的响应灵敏度(最高可达10-10 mol/L)和可视化优势,适用于实时监测与智能识别场景,但其探针设计门槛高,稳定性仍是制约其广泛应用的主要因素;比色法则以简便、低成本的特点适用于TVB-N和三甲胺含量等指标的快速筛查,但灵敏度及抗干扰能力有限,适用于初步定性判断。此外,在数据标准化与关联建模方面,多数风味物质与食品品质、感官评分或市场价值之间尚缺乏明确的数量关联,这使得风味检测结果难以直接用于质量评估与溯源分析,影响其在产业中的推广应用。因此,快速检测技术的选择应充分考虑检测对象的理化特征、目标浓度区间、所处环境条件及后续应用需求,合理匹配检测平台,从而在实际场景中实现“快速-准确-可行”的最佳检测效果。
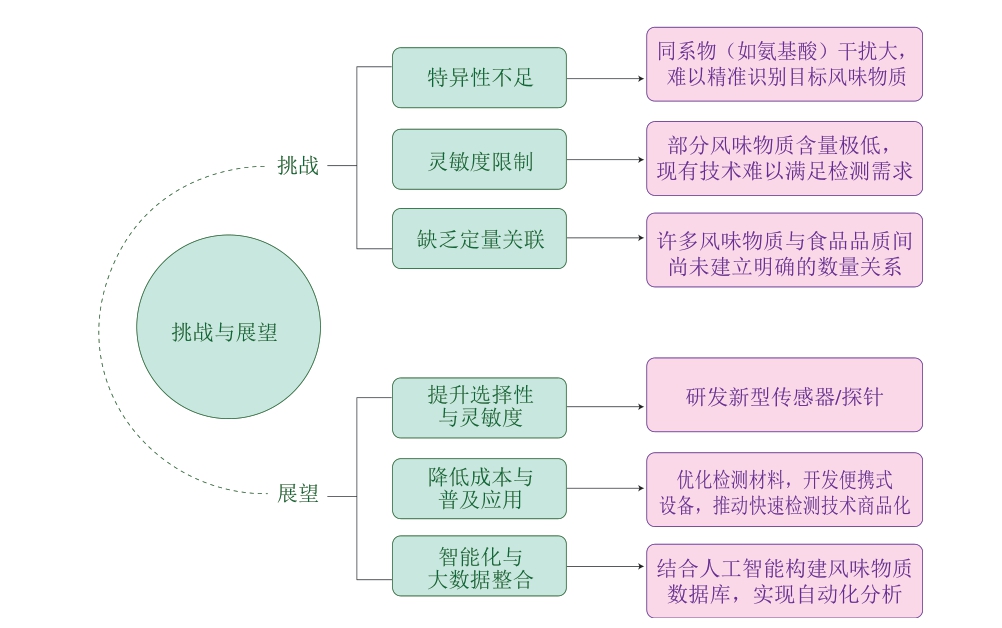
图3 快速检测技术在食品风味分析中面临的挑战与未来展望
Fig. 3 Challenges and future prospects of rapid detection technologies in food flavor analysis
针对上述挑战,未来风味物质快速检测技术的发展应从多个维度协同推进。首先,在识别元件与探针分子设计方面,可深入开发分子印迹聚合物、纳米酶等新型识别单元,通过多位点协同机制增强对同分异构体和痕量物质的识别特异性。其次,应突破单一信号检测模式限制,将比色、荧光、电化学与MS等多种检测机制集成于同一平台,推动多模态检测技术融合,实现复杂食品基质中风味物质的多维识别与互补验证。在检测终端形式方面,借助柔性材料、微流控芯片和纸基平台等低成本材料,开发便携式甚至可穿戴传感装置,满足移动检测和冷链贮运过程中的实时监测需求。同时,结合现场化、智能化与信息化发展趋势,将快速检测技术与人工智能及大数据技术深度融合,构建风味数据库,整合快速检测数据、感官评价与环境变量,并结合机器学习算法建立风味分子与感官特征之间的映射关系。例如,可借助大数据构建风味数据库,系统整合风味物质的检测数据与感官评价,实现快速比对与趋势追踪;同时,人工智能算法能够对检测结果进行自动分析与判断,提高数据处理效率和准确性,进而实现风味变化趋势预测,为肉制品的生产调控、贮藏管理及品质控制提供科学支持[72]。因此,风味快速检测技术应以“高通量、强识别、低成本、智能化”为目标,融合先进材料科学、信息技术与感官科学,实现从实验室研究向实际场景应用的深度转化。
特征风味物质作为肉制品品质评估、溯源识别及消费接受度判断的重要理化指标,其快速、准确检测对于肉类产品的品质控制与食品安全保障具有重要意义。以比色法、荧光法、电化学法为代表的快速检测技术在灵敏度、响应速率及便携性方面优势显著,逐步成为传统仪器分析技术的有力补充,并已广泛应用于L-Glu、IMP、肌肽、TVB-N、醛类与硫酚类等关键风味物质的定性与定量检测,显著提升风味物质检测的实时性与现场适用性。然而,该领域仍面临多个瓶颈问题,包括目标识别的特异性不足、复杂基质的干扰效应尚未完全克服、传感器稳定性与通用性有待提升等。未来研究应着重于高选择性识别元件开发、新型多模态传感平台构建,以及与人工智能、大数据等信息技术的深度融合,实现风味快速检测技术的高通量、自动化与智能化发展。通过持续技术优化与标准体系建设,风味快速检测技术将在肉类产品品质控制、溯源追踪与食品安全保障中发挥更加关键的作用。
[1] 杜春林, 赵春萍, 谭娅. 肉类风味物质检测技术研究进展[J]. 肉类研究, 2023, 37(8): 46-51. DOI:10.7506/rlyj1001-8123-20230517-047.
[2] NATH S. Advancements in food quality monitoring: integrating biosensors for precision detection[J]. Sustainable Food Technology,2024, 2(4): 976-992. DOI:10.1039/d4fb00094c.
[3] AWLQADR F H, ALTEMIMI A B, QADIR S A, et al. Emerging trends in nano-sensors: a new frontier in food safety and quality assurance[J].Heliyon, 2025, 11(1): e41181. DOI:10.1016/j.heliyon.2024.e41181.
[4] RIBEIRO C, GONÇALVES R, TIRITAN M E. Separation of enantiomers using gas chromatography: application in forensic toxicology, food and environmental analysis[J]. Critical Reviews in Analytical Chemistry, 2021, 51(8): 787-811. DOI:10.1080/10408347.2 020.1777522.
[5] WANG Y K, LIU L, LIU X J, et al. Identification of characteristic aroma compounds in chicken meat and their metabolic mechanisms using gas chromatography-olfactometry, odor activity values, and metabolomics[J]. Food Research International, 2024, 175: 113782.DOI:10.1016/j.foodres.2023.113782.
[6] FENG T, SUN M, SONG S Q, et al. Gas chromatography for food quality evaluation[M]//ZHONG J, WANG X C. Evaluation technologies for food quality. Amsterdam: Elsevier, 2019: 219-265.DOI:10.1016/b978-0-12-814217-2.00012-3.
[7] 江海. 高效液相色谱法在食品检测中的应用[J]. 现代食品, 2019,25(1): 127-128. DOI:10.16736/j.cnki.cn41-1434/ts.2019.01.044.
[8] SIDDIQUE I M. High-performance liquid chromatography:comprehensive techniques and cutting-edge innovations[J]. European Journal of Advances in Engineering and Technology, 2023, 10(9): 66-70. DOI:10.5281/zenodo.11545742.
[9] CAO G D, LI K, GUO J G, et al. Mass spectrometry for analysis of changes during food storage and processing[J]. Journal of Agricultural and Food Chemistry, 2020, 68(26): 6956-6966. DOI:10.1021/acs.jafc.0c02587.
[10] MILANI N B L, VAN GILST E, PIROK B W J, et al. Comprehensive two-dimensional gas chromatography: a discussion on recent innovations[J]. Journal of Separation Science, 2023, 46(21): 2300304.DOI:10.1002/jssc.202300304.
[11] VANITHA MADHURI T, PANDREKA M K, GEETHA GAYATRI B,et al. Advances in high-performance liquid chromatography (HPLC)and ultra-performance liquid chromatography (UPLC): review article[J]. Journal of Pharma Insights and Research, 2024, 2(6): 39-46.DOI:10.69613/t4nhz921.
[12] WANG S Q, CHEN H T, SUN B G. Recent progress in food flavor analysis using gas chromatography-ion mobility spectrometry(GC-IMS)[J]. Food Chemistry, 2020, 315: 126158. DOI:10.1016/j.foodchem.2019.126158.
[13] HERNÁNDEZ-MESA M, ROPARTZ D, GARCÍA-CAMPAÑA A M,et al. Ion mobility spectrometry in food analysis: principles, current applications and future trends[J]. Molecules, 2019, 24(15): 2706.DOI:10.3390/molecules24152706.
[14] LIANG L, DUAN W, ZHAO C, et al. Recent development of twodimensional liquid chromatography in food analysis[J]. Food Analytical Methods, 2022, 15(5): 1214-1225. DOI:10.1007/s12161-021-02190-2.
[15] PIRIYA V S A, JOSEPH P, DANIEL S C G K, et al. Colorimetric sensors for rapid detection of various analytes[J]. Materials Science and Engineering: C, 2017, 78: 1231-1245. DOI:10.1016/j.msec.2017.05.018.
[16] TIAN X X, ZHENG X C, CHEN L, et al. Recent advances in photoluminescent fluorescent probe technology for food flavor compounds analysis[J]. Food Chemistry, 2024, 459: 140455.DOI:10.1016/j.foodchem.2024.140455.
[17] 王艳, 包士雷, 孙立瑞, 等. 电化学技术在食品检测中的应用研究进展[J]. 食品科学, 2024, 45(3): 295-306. DOI:10.7506/spkx1002-6630-20230416-148.
[18] AFZAL A, SAEED F, AFZAAL M, et al. The chemistry of flavor formation in meat and meat products in response to different thermal and non-thermal processing techniques: an overview[J].Journal of Food Processing and Preservation, 2022, 46(10): e16847.DOI:10.1111/jfpp.16847.
[19] BLEICHER J, EBNER E E, BAK K H. Formation and analysis of volatile and odor compounds in meat: a review[J]. Molecules, 2022,27(19): 6703. DOI:10.3390/molecules27196703.
[20] SONG C Y, WANG Z J, LI H Q, et al. Recent advances in taste transduction mechanism, analysis methods and strategies employed to improve the taste of taste peptides[J]. Critical Reviews in Food Science and Nutrition, 2025, 65(4): 695-714. DOI:10.1080/10408398.2023.2280246.
[21] FU Y H, CAO S Y, YANG L, et al. Flavor formation based on lipid in meat and meat products: a review[J]. Journal of Food Biochemistry,2022, 46(12): e14439. DOI:10.1111/jfbc.14439.
[22] BARANWAL J, BARSE B, GATTO G, et al. Electrochemical sensors and their applications: a review[J]. Chemosensors, 2022, 10(9): 363.DOI:10.3390/chemosensors10090363.
[23] WANG X D, DUAN J J, CAI Y M, et al. A modified nanocomposite biosensor for quantitative L-glutamate detection in beef[J]. Meat Science, 2020, 168: 108185. DOI:10.1016/j.meatsci.2020.108185.
[24] WANG X D, HU F, ZHU L T, et al. N,N′-Diphenylthiourea electrochemical sensor for the detection of L-glutamate and aspartate in beef[J]. Journal of Food Science, 2020, 85(11): 3852-3857.DOI:10.1111/1750-3841.15494.
[25] MOTA F A R, PASSOS M L C, SANTOS J L M, et al. Comparative analysis of electrochemical and optical sensors for detection of chronic wounds biomarkers: a review[J]. Biosensors and Bioelectronics, 2024,251: 116095. DOI:10.1016/j.bios.2024.116095.
[26] HAN T T, HUANG Y, GAO T Y, et al. Fabrication of nitrogen-doped graphene quantum dots based fluorescent probe and its application for simultaneous, sensitive and selective detection of umami amino acids[J]. Food Chemistry, 2023, 404(Pt A): 134509. DOI:10.1016/j.foodchem.2022.134509.
[27] DAS S, GHOSH A, KUNDU S, et al. Development of a new fluorescent probe for cysteine detection in processed food samples[J].Analytical and Bioanalytical Chemistry, 2019, 411(23): 6203-6212.DOI:10.1007/s00216-019-02012-9.
[28] 金睿, 曹满湖, 黄泰来, 等. 鸡肉肌苷酸含量影响因素研究进展[J]. 中国家禽, 2021, 43(10): 87-93. DOI:10.16372/j.issn.1004-6364.2021.10.013.
[29] DE SOUZA C, EYNG C, VIOTT A M, et al. Effect of dietary guanidinoacetic acid or nucleotides supplementation on growth performances, carcass traits, meat quality and occurrence of myopathies in broilers[J]. Livestock Science, 2021, 251: 104659.DOI:10.1016/j.livsci.2021.104659.
[30] FUKUSHIMA H, YAMADA K, WADA R, et al. Thermal stabilities of inosine monophosphate-degrading enzymes in several fish muscles[J].International Journal of Food Properties, 2020, 23(1): 1158-1167.DOI:10.1080/10942912.2020.1785492.
[31] WANG G X, SUN J F, YAO Y, et al. Detection of inosine monophosphate (IMP) in meat using double-enzyme sensor[J]. Food Analytical Methods, 2020, 13(2): 420-432. DOI:10.1007/s12161-019-01652-y.
[32] WANG G X, LIU J, YUE F L, et al. Dual enzyme electrochemiluminescence sensor based on in situ synthesis of ZIF-67@AgNPs for the detection of IMP in fresh meat[J]. LWTFood Science and Technology, 2022, 165: 113658. DOI:10.1016/j.lwt.2022.113658.
[33] LIU J, SHEN Y Z, WANG G X, et al. Highly-sensitive electrochemiluminescence biosensor for detection of inosine monophosphate in meat based on graphdiyne/AuNPs/luminol nanocomposites[J]. Food Science and Human Wellness, 2023, 12(4):1149-1156. DOI:10.1016/j.fshw.2022.10.040.
[34] WANG X Y, DONG S J, WEI H. Recent advances on nanozymebased electrochemical biosensors[J]. Electroanalysis, 2023, 35(1):e202100684. DOI:10.1002/elan.202100684.
[35] FEI Q Q, ZHANG N N, SUN C, et al. A novel non-enzymatic sensing platform for determination of 5’-guanosine monophosphate in meat[J]. Food Chemistry, 2019, 286: 515-521. DOI:10.1016/j.foodchem.2019.02.052.
[36] 高田毅, 孙冲, 朱宏星, 等. 基于柠檬酸-铕纳米配位聚合物构建荧光探针快速检测汤煲中5′-肌苷酸含量[J]. 食品科学, 2021, 42(24):283-288. DOI:10.7506/spkx1002-6630-20210201-018.
[37] SHI L F, LI Z R, ZHANG Y H, et al. Electrospun starch-based nanofiber mats for odor adsorption of oyster peptides: recyclability and structural characterization[J]. Food Hydrocolloids, 2024, 147: 109408.DOI:10.1016/j.foodhyd.2023.109408.
[38] 胡文彦, 徐道坤, 刘真, 等. 基于多肽标记物分析的肉制品掺伪定量检测技术[J]. 分析测试学报, 2020, 39(12): 1481-1486. DOI:10.3969/j.issn.1004-4957.2020.12.007.
[39] JOZANOVIĆ M, SAKAČ N, SAK-BOSNAR M, et al. A simple and reliable new microchip electrophoresis method for fast measurements of imidazole dipeptides in meat from different animal species[J].Analytical and Bioanalytical Chemistry, 2018, 410(18): 4359-4369.DOI:10.1007/s00216-018-1087-6.
[40] SIONEK B, PRZYBYLSKI W, TAMBOR K. Biosensors in evaluation of quality of meat and meat products: a review[J]. Annals of Animal Science, 2020, 20(4): 1151-1168. DOI:10.2478/aoas-2020-0057.
[41] UMUHUMUZA L C, SUN X L. Rapid detection of pork meat freshness by using L-cysteine-modified gold electrode[J]. European Food Research and Technology, 2011, 232(3): 425-431. DOI:10.1007/s00217-010-1405-5.
[42] SHI Y K, NIU Z J, CHEN S C, et al. Sensitive detection of umami substances in meat with synthesized electrochemical sensor enhanced by MXene surface-doped peroxidase-mimic nanoenzymes (Fe3O4)[J].Food and Bioprocess Technology, 2025, 18(1): 807-817. DOI:10.1007/s11947-024-03507-9.
[43] SHI Y K, NIU Z J, RODAS-GONZALEZ A, et al. An electrochemical adsorption-catalysis sensor based on 2D MXene/g-C3N4 doped with Au-COOH for selective detection of GMP in meat[J].Chemical Engineering Journal, 2024, 500: 155893. DOI:10.1016/j.cej.2024.155893.
[44] YU Y, HUAN S Q, WANG X D, et al. An electrochemical sensor based on [Ru(bpy)2dpp]2+/SMWCNTs/Au modified glassy carbon electrode for the detection of 5’-GMP[J]. Applied Biological Chemistry, 2022,65(1): 51. DOI:10.1186/s13765-022-00721-x.
[45] YU Y, WANG X D, LI M Y, et al. Design fabrication of electrochemical sensor based on Ru(bpy)2 2+/SMWCNTs/Au/GCE electrode for the selective determination of 5′-guanosine monophosphate[J]. Food Chemistry, 2023, 418: 135841. DOI:10.1016/j.foodchem.2023.135841.
[46] 齐广宇. 基于QCM气敏传感器的鱼肉中TVB-N快速检测[D]. 淄博:山东理工大学, 2023. DOI:10.27276/d.cnki.gsdgc.2023.000979.
[47] BEKHIT A E A, HOLMAN B W B, GITERU S G, et al. Total volatile basic nitrogen (TVB-N) and its role in meat spoilage:a review[J]. Trends in Food Science & Technology, 2021, 109: 280-302. DOI:10.1016/j.tifs.2021.01.006.
[48] ERNA K H, ROVINA K, MANTIHAL S. Current detection techniques for monitoring the freshness of meat-based products: a review[J].Journal of Packaging Technology and Research, 2021, 5(3): 127-141.DOI:10.1007/s41783-021-00120-5.
[49] LI M, XU J G, PENG C F, et al. Deep learning-assisted flavonoidbased fluorescent sensor array for the nondestructive detection of meat freshness[J]. Food Chemistry, 2024, 447: 138931. DOI:10.1016/j.foodchem.2024.138931.
[50] ZHANG W Y, MA J, SUN D W. Dual-signal fluorescent test strips for spoilage sensing of packaged seafood: visual monitoring of volatile basic nitrogens[J]. Food Chemistry, 2023, 416: 135725. DOI:10.1016/j.foodchem.2023.135725.
[51] HUANG X W, ZHAO W Y, SUN W, et al. A paper-based ratiometric fluorescent sensor for NH3 detection in gaseous phase: real-time monitoring of chilled chicken freshness[J]. Food Chemistry: X, 2024,21: 101054. DOI:10.1016/j.fochx.2023.101054.
[52] ZHOU C Y, SUN D W, MA J, et al. Assembly-induced emission of copper nanoclusters: revealing the sensing mechanism for detection of volatile basic nitrogen in seafood freshness on-site monitoring[J]. ACS Applied Materials & Interfaces, 2024, 16(5): 6533-6547. DOI:10.1021/acsami.3c13321.
[53] XU W D, HE Y C, LI J H, et al. Portable beef-freshness detection platform based on colorimetric sensor array technology and bionic algorithms for total volatile basic nitrogen (TVB-N)determination[J]. Food Control, 2023, 150: 109741. DOI:10.1016/j.foodcont.2023.109741.
[54] GUO Y Q, ZHANG D B, WANG J Y, et al. Luminescent probe based on photochromic cyclometalated iridium(III) complex for high selectivity detection of thiophenol[J]. Dyes and Pigments, 2020, 175:108191. DOI:10.1016/j.dyepig.2020.108191.
[55] XU Z Y, WANG X H, LUO H Q, et al. Cascade reaction-based highly sensitive fluorescent sensing systems applicable for dual-pattern fluorescence visualizing of thiophenol flavors in meat products and condiments[J]. Food Chemistry, 2023, 407: 135120. DOI:10.1016/j.foodchem.2022.135120.
[56] LIN P X, XIE C, LIU T, et al. Rational construction of reliable fluorescent probes for rapid detection and imaging evaluation of hazardous thiophenol in real-food and biosystems[J]. Food Chemistry,2024, 432: 137264. DOI:10.1016/j.foodchem.2023.137264.
[57] DU Z Y, QI Q Q, GAO W, et al. Electrochemical heteroatomheteroatom bond construction[J]. The Chemical Record, 2022, 22(1):e202100178. DOI:10.1002/tcr.202100178.
[58] JELEN H. Food flavors: chemical, sensory and technological properties[M]. Boca Raton: CRC Press, 2011. DOI:10.1201/b11187
[59] LIU X T, WANG K, WEI L C, et al. A highly sensitive Golgi-targeted fluorescent probe for the simultaneous detection of malondialdehyde and formaldehyde in living systems and foods[J]. Talanta, 2024, 278:126427. DOI:10.1016/j.talanta.2024.126427.
[60] LIN M Y, LIU S B. Naphthalimide-based fluorescent probe for profiling of aldehydes during oxidation of unsaturated lipids[J].Journal of Agricultural and Food Chemistry, 2022, 70(44): 14304-14311. DOI:10.1021/acs.jafc.2c05659.
[61] LI H, DENG N, CAI Y J, et al. Dynamic changes in postmortem quality of grass carp (Ctenopharyngodon idella) muscle: from the perspectives of muscle degradation and flavor evolution[J]. Food Chemistry: X, 2024, 23: 101751. DOI:10.1016/j.fochx.2024.101751.
[62] SIRAJ S, SHARMA A, HOSSAIN N I, et al. Room temperature-based ZnO/WSe2 VOC (hexanal, 1-octen-3-ol, 1-pentanol) sensor for red meat degradation[J]. ACS Applied Electronic Materials, 2025, 7(15):7311-7320. DOI:10.1021/acsaelm.5c01079.
[63] LIU X Y, WANG Y, ZHANG Z X, et al. On-package ratiometric fluorescent sensing label based on AIE polymers for real-time and visual detection of fish freshness[J]. Food Chemistry, 2022, 390:133153. DOI:10.1016/j.foodchem.2022.133153.
[64] KOSHY R R, KOSHY J T, MARY S K, et al. Preparation of pH sensitive film based on starch/carbon nano dots incorporating anthocyanin for monitoring spoilage of pork[J]. Food Control, 2021,126: 108039. DOI:10.1016/j.foodcont.2021.108039.
[65] ZHAI X D, ZOU X B, SHI J Y, et al. Amine-responsive bilayer films with improved illumination stability and electrochemical writing property for visual monitoring of meat spoilage[J]. Sensors and Actuators B: Chemical, 2020, 302: 127130. DOI:10.1016/j.snb.2019.127130.
[66] NIE W G, CHEN Y F, ZHANG H, et al. A novel colorimetric sensor array for real-time and on-site monitoring of meat freshness[J].Analytical and Bioanalytical Chemistry, 2022, 414(20): 6017-6027.DOI:10.1007/s00216-022-04176-3.
[67] ZHOU Z X, LI C H, HE J, et al. A dual-color ratiometric fluorescence sensor of biogenic amines with dye encapsulated covalent organic framework for meat freshness[J]. LWT-Food Science and Technology,2024, 209: 116788. DOI:10.1016/j.lwt.2024.116788.
[68] WANG H, WU X M, YANG S X, et al. A rapid and visible colorimetric fluorescent probe for benzenethiol flavor detection[J]. Food Chemistry,2019, 286: 322-328. DOI:10.1016/j.foodchem.2019.02.033.
[69] WU J H, ZENG Q, LUO H Q, et al. A ratiometric fluorescent probe based on quinoxaline for detection of thiophenols in food samples and living cells[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2025, 331: 125774. DOI:10.1016/j.saa.2025.125774.
[70] LIU X T, LI Z L, WANG Z Y, et al. Lysosome-specific fluorescent probe for malondialdehyde/formaldehyde detection in oxidative/carbonyl stressed nerve cells and foods[J]. Bioorganic Chemistry,2025, 162: 108585. DOI:10.1016/j.bioorg.2025.108585.
[71] YUAN G Q, DING H Y, PENG L P, et al. A novel fluorescent probe for ratiometric detection of formaldehyde in real food samples,living tissues and zebrafish[J]. Food Chemistry, 2020, 331: 127221.DOI:10.1016/j.foodchem.2020.127221.
[72] CUI Z Y, QI C L, ZHOU T X, et al. Artificial intelligence and food flavor: how AI models are shaping the future and revolutionary technologies for flavor food development[J]. Comprehensive Reviews in Food Science and Food Safety, 2025, 24(1): e70068.DOI:10.1111/1541-4337.70068.