Optimization of Extraction Process and Characterization of Gelatin from Chicken Heads
王明月, 王晓明, 李欣怡, 等. 鸡头明胶提取工艺优化及产物特性分析[J]. 肉类研究, 2026, 40(5): 36-44. DOI:10.7506/rlyj1001-8123-20250621-199. http://www.rlyj.net.cn
WANG Mingyue, WANG Xiaoming, LI Xinyi, et al. Optimization of extraction process and characterization of gelatin from chicken heads[J]. Meat Research, 2026, 40(5): 36-44. (in Chinese with English abstract) DOI:10.7506/rlyj1001-8123-20250621-199. http://www.rlyj.net.cn
近年来,由于肉鸡生产和消费量的持续增长,鸡副产物废弃量也逐年增加。畜禽屠宰副产物是指除畜禽屠宰加工过程中主要肉制品外的其余产物。根据美国农业部数据显示,2024年全球肉鸡产量为10 304.60万 t,较2023年下降78.20万 t。鸡头约占全鸡质量的2%,预估2024年全球鸡头产量超1 000万 t。在众多鸡副产物中,鸡头因其原料来源充足,营养价值丰富且较少涉及动物传染病风险,展现出较高的潜在利用价值[1]。目前,鸡头综合利用开发方向包括明胶[2]、胶原蛋白肽[3]、透明质酸钠[4]和可食用鸡头等。其中,明胶因其优异的成膜性、生物相容性和可降解性,在食品包装[5]、医药载体[6]、环保材料[7]等领域应用广泛。随着全球对明胶需求的持续增长,开发基于鸡头的新型明胶既能满足市场需求,又能拓宽原料来源[8]。
采用传统酸法/碱法处理原料存在能源与资源消耗大、明胶得率低等问题,且产生的废水呈现高盐碱和高有机物浓度等复合污染特征[9],对环境造成严重压力。基于传统酸法/碱法对不同原料明胶进行提取的工艺优化研究中,Gómez-Guillén等[10]采用0.05 mol/L乙酸处理鱼皮/鱼鳞,并结合水热法提取明胶,发现传统酸法处理鱼皮/鱼鳞的明胶得率较低,最高仅为2.60%。Ee等[11]采用添加NaCl的碱法从鸡头中提取明胶,得率可达10.05%。为探究碱处理过程中添加NaCl对得率的影响,Yu Ermeng等[12]采用酸碱预处理结合盐渍法处理鱼皮,发现NaCl能够增加胶原蛋白溶解性并可产生强电离,有利于明胶形成。相比之下,在酸法中添加酶进行明胶提取更环保且更具安全性,例如,Abedinia等[13]采用添加胃蛋白酶的乙酸处理结合水热法从北京鸭脚中提取明胶,得率较酸法和碱法高,达5.75%,显示出酶法处理的优势。
目前直接从鸡头中提取明胶的研究有限,在进行鸡副产物明胶提取时,一般将鸡头与鸡脚、鸡皮[14]或其他副产物共混[15],其原因在于鸡头由骨骼、肌腱、软骨、皮肤、肉和其他组织(如眼球、脂肪、神经组织等)等多种组织构成,其中骨骼、软骨和皮肤均为胶原蛋白优质来源,但其占比相对较低(约20%),而占比最高的骨骼需进行脱矿处理,胶原提取难度较大,这导致鸡头明胶提取效率总体较低,且所需能耗较大。酸法作为其他明胶提取方法的基础,应用最为广泛。采用酸法提取鱼皮明胶的得率较高,且能保留更为完整的三螺旋结构,而猪、牛、鸭等来源明胶得率普遍较低(3%~5%)[16]。为提高明胶提取效率并降低能耗,有必要探究酸处理与其他方法相结合对明胶得率和性能的影响,为提高鸡头明胶得率和性能、实现鸡头资源高效利用和增值开发提供技术支持与理论基础。本研究对鸡头明胶提取工艺进行优化,采用酸法、酸碱法和酸酶法处理结合水热提取鸡头明胶,系统比较水热提取温度(55、60、65 ℃)与时间(3、4.5、6 h)对明胶得率的影响,基于单因素试验优化水热提取工艺参数,并对明胶产物特性进行分析。
新鲜白羽肉鸡鸡头(818肉杂鸡,日龄40~55 d)新兴县温氏佳丰食品有限公司。
羟脯氨酸试剂盒 北京博奥森生物技术有限公司;双缩脲蛋白含量测定试剂盒 北京索莱宝科技有限公司;冰乙酸(ACS级)、NaOH、NaHCO3、5-磺基水杨酸、甲醇、三乙胺、异硫氰酸苯酯、Na2HPO4(均为分析纯)、猪胃蛋白酶(3 000 U) 上海阿拉丁生化科技股份有限公司。
JR05-300电动绞肉机 浙江苏泊尔股份有限公司;5810R低温高速冷冻离心机 德国艾本德股份公司;THZ-103B小型恒温摇床培养箱、MF12L马弗炉 天津泰斯特仪器有限公司;CR400色差仪 日本柯尼卡美能达株式会社;DW-86L388(J)-80 ℃超低温冷冻储藏箱青岛海尔生物医疗股份有限公司;SKD-6800全自动凯氏定氮仪、PQZF-1000全自动脂肪测定仪 上海沛欧分析仪器有限公司;LC-20AT高效液相色谱(high performance liquid chromatography,HPLC)仪日本岛津制作所;TA.XT Plus质构仪 英国Stable Micro Systems公司;Zetasizer Nano ZS90 Zeta电位仪 英国Malvern Panalytical公司;MCR92流变仪 安东帕(上海)商贸有限公司;PHS-3E pH计 上海仪电科学仪器股份有限公司。
1.3.1 明胶提取
1.3.1.1 前处理将鸡头肉样绞碎后,按照1∶4(g/mL)加入纯水,4 ℃搅拌15 min后,经1 mm孔径筛子过滤后备用。
1.3.1.2 脱脂
温水脱脂:按照1∶10(g/mL)加入纯水,200 r/min振荡6 h,每2 h更换一次溶液;冷脱脂[17]:按照1∶10(g/mL)加入乙醇-石油醚混合溶液(1∶1,V/V),200 r/min振荡6 h,每2 h更换一次脱脂溶液;碱溶液脱脂[18]:按照1∶4(g/mL)加入15 mmol/L NaHCO3溶液,4 ℃振荡1 h,4 ℃、10 000×g离心10 min,重复3 次。比较不脱脂、温水脱脂、冷脱脂、碱溶液脱脂4 种脱脂方法的脱脂率。采用全自动脂肪测定仪基于增重法测定鸡头和明胶中的脂肪含量。脱脂率按式(1)计算:
式中:m0为鸡头中脂肪质量/g;m1为明胶中脂肪质量/g。
1.3.1.3 预处理
60 ℃烘箱干燥18 h后称质量,并按以下3 种方法进行预处理。1)酸法:干燥后的肉样以1∶10(g/mL)加入0.05 mol/L冰乙酸,室温搅拌3 h,纱布过滤,加入10 mol/L NaOH溶液调节pH值为7;2)酸碱法:参考Ee等[19]的方法并作适当修改,按照1∶10(g/mL)加入10 mol/L NaOH溶液(含5、10、15 g/L NaCl),碱处理1 h后,纱布过滤,按照1∶10(g/mL)加入0.05 mol/L冰乙酸,酸处理24 h后,纯水冲洗,采用10 mol/L NaOH溶液将pH值调节至7;3)酸酶法:按照1∶10(g/mL)加入0.05 mol/L冰乙酸(含猪胃蛋白酶,添加量15 U/g[20]),4 ℃搅拌3 h后,使用10 mol/L NaOH溶液调节pH值至7,4 ℃振荡1 h使酶失活。
1.3.1.4 水热提取单因素试验
以预处理后的肉样为原料,确保肉样质量及料液比(肉样与纯水)固定。采用单一变量法分别探究水热提取温度与时间对明胶得率的影响。研究提取温度时,固定提取时间为3 h,设置提取温度分别为55、60、65 ℃。研究提取时间时,固定提取温度为55 ℃,设置提取时间分别为3、4.5、6 h。提取完成后,使用纱布过滤得上清液,冷冻干燥。每组重复3 次,取平均值。
1.3.2 明胶理化与功能特性指标测定
1.3.2.1 得率
为避免明胶成品吸湿影响得率测定结果,冷冻干燥后立即称质量,得率按式(2)计算:
式中:m0为干燥后肉样质量/g;m1为冻干明胶质量/g。
1.3.2.2 基础成分含量
鸡头和明胶水分含量参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》第一法(直接干燥法)进行测定;粗蛋白含量参照GB 5009.5—2025《食品安全国家标准 食品中蛋白质的测定》,采用全自动凯氏定氮仪测定;灰分含量参照GB 6783—2013《食品安全国家标准 食品添加剂 明胶》,采用马弗炉测定;粗脂肪含量按1.3.1.2节方法测定。
1.3.2.3 色泽
采用色差仪测定明胶的亮度值(L*)、红度值(a*)及黄度值(b*)。
1.3.2.4 pH值
将明胶溶于纯水配制成6.67%(m/m,下同)明胶溶液,55 ℃水浴加热使其完全溶解,于35 ℃条件下使用pH计测定溶液pH值。
1.3.2.5 等电点(isoelectric point,pI)
使用电位仪测定明胶溶液在pH 4、6、8、10、12的缓冲溶液中的Zeta电位,通过Zeta电位-pH值曲线确定pI。
1.3.2.6 纯度
使用羟脯氨酸试剂盒测定明胶纯度,并根据AOAC 990.26标准,以14%作为转换系数估算原料胶原蛋白质量分数。
1.3.2.7 氨基酸组成
使用HPLC法测定明胶氨基酸组成与相对含量[21]。称取2~4 g明胶,加入20 mL 3 g/100 mL 5-磺基水杨酸溶液,定容至100 mL,振荡18 h后4 ℃、12 000 r/min离心10 min。取10 µL上清液于5 mL离心管中,氮气吹干,加入10 µL干燥剂(甲醇-纯水-三乙胺,2∶2∶1,V/V)进行干燥,再次氮气吹干。加入20 µL衍生剂(纯水-甲醇-三乙胺-异硫氰酸苯酯,1∶7∶1∶1,V/V)密闭衍生30 min,衍生化产物经氮气吹干,加入200 µL稀释剂(纯水将0.71 g Na2HPO4溶解并定容至1 L,磷酸-乙腈溶液(19∶1,V/V)调节pH值至7.4)复溶待测。
1.3.2.8 凝胶强度(Bloom值)
配制6.67%明胶溶液,溶胀2 h后60 ℃加热10 min使其完全溶解,10 ℃恒温保持17 h形成凝胶。8 ℃放置18 h后,使用质构仪测定Bloom值,参数:量程5 kN、穿刺速率0.5 mm/s,取探头穿刺4 mm深度时的最大阻力值[22]。
1.3.2.9 溶解度
配制6.67%明胶溶液,取5 mL于离心管,用1 mol/L NaOH溶液调节pH值至2~12,并用对应pH值的缓冲溶液定容至10 mL。所有样品在室温下9 000×g离心10 min,采用双缩脲蛋白含量测定试剂盒测定离心前后蛋白质量。溶解度按式(3)计算:
式中:m0为离心后上清液中蛋白质量/g;m1为离心前样品中蛋白质量/g。
1.3.2.10 动态黏弹性
参考Kurt等[23]的方法并作适当改动,使用流变仪进行振荡剪切-温度扫描,以测定明胶的黏弹性特征。参数:以1 ℃/min加热/冷却速率在5~45 ℃范围内进行升降温循环,记录储能模量(G’)和损耗模量(G”)随温度的变化曲线。
所有实验均设置3 次重复,使用Microsoft Excel 2019软件进行数据统计,使用SPSS Statistics 25软件进行单因素方差分析,P<0.05表示差异显著,使用Origin 2025软件绘图。
鸡头基础营养成分质量分数从高到低依次为水分(75.61%)、粗蛋白(14.19%)、粗脂肪(13.35%)、灰分(2.91%),以水分含量最高,其次为粗蛋白和粗脂肪,灰分含量最低。由于粗蛋白中包含多种蛋白质(可能富含胶原蛋白),且灰分含量低,对明胶品质影响较小,均无需去除,因此仅需进行脂肪脱除处理。鸡头脂肪含量较高且易氧化酸败产生异味,影响明胶品质,故需优先去除。
由图1可知,脱脂率从高到低依次为冷脱脂(89.74%)、碱脱脂(86.9%)、温水脱脂(71.52%)、不脱脂(27.73%)。从脱脂时间上看,温水脱脂耗时最长(18 h),其次为冷脱脂(6 h)和碱脱脂(1.5 h),脱脂时间最短为不脱脂(0 h)。综合考虑脱脂效率和耗时,碱脱脂和冷脱脂均能有效去除脂肪,其中碱脱脂在较短时间内即可达到较高脱脂率。因此选择碱脱脂作为最佳脱脂方式。
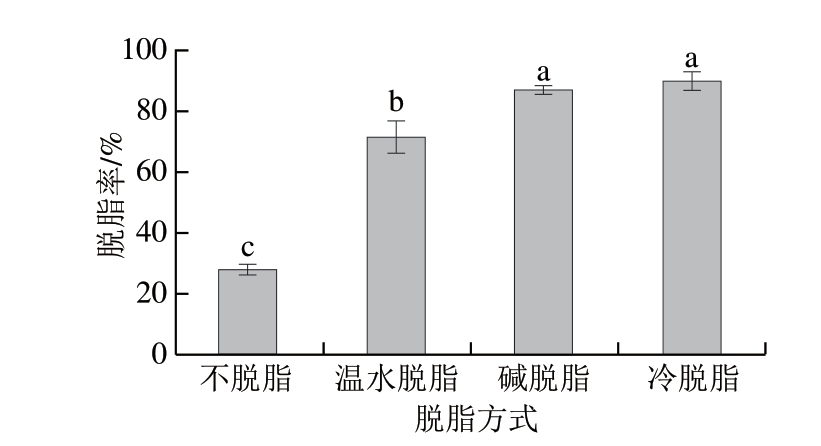
图1 不同脱脂方式对鸡头脱脂率的影响
Fig. 1 Effect of different defatting methods on fat removal rate from chicken heads
小写字母不同表示组间差异显著(P<0.05)。图2同。
由图2可知,添加10 g/L NaCl时,酸碱法制备明胶得率最高,为6.53%,显著高于其他组(P<0.05)。其次为15 g/L NaCl组(6.06%)和5 g/L NaCl组(5.76%),而不添加NaCl时,酸碱法制备明胶得率最低,仅为4.37%。由此可见,NaCl含量过高或过低均会降低明胶得率。这是由于NaCl含量过低会导致溶液中离子强度不足,而NaCl含量过高会导致离子强度过高,进而引发胶原蛋白竞争性脱水,造成其过早溶出和沉淀[24],最终导致明胶得率下降。
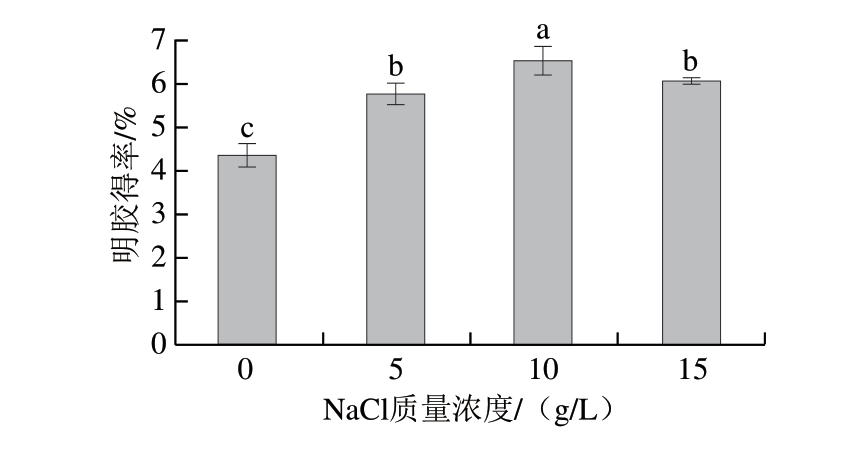
图2 不同NaCl含量对酸碱法制备明胶得率的影响
Fig. 2 Effect of different NaCl contents on the yield of gelatin using the alkaline-acid method
由表1可知,在55 ℃、3 h条件下,酸法、酸碱法和酸酶法制备明胶得率分别为1.72%、4.17%和4.29%,酸碱法与酸酶法之间无显著差异(P>0.05),二者均显著高于酸法(P<0.05)。低温提取时,酸酶法因胃蛋白酶特异性切割端肽区,能够有效降低胶原分子间作用力,减少水热溶出阻力,且不会对三螺旋结构产生明显影响[25]。当提取温度升至60 ℃时,酸碱法制备明胶得率有所提升,这是由于酸碱预处理能够破坏胶原蛋白分子间的共价键和氢键,使得胶原蛋白结构松散并充分溶胀[26],升温能够促进其溶解。此时,酸酶法制备明胶得率较酸碱法低,这可能与三螺旋结构的解折叠、疏水基团暴露形成聚集体有关。在60 ℃、6 h条件下,3 种方法的明胶得率均达到最高值,分别为2.52%、10.08%和9.08%,且组间差异显著(P<0.05),其中,酸碱法与酸酶法制备明胶得率分别为酸法的4.0 倍和3.6 倍。但当提取温度继续升至65 ℃时,3 种方法的明胶得率均有所下降,这是由于高温长时间提取会导致胶原蛋白过度水解[19]。但总体而言,酸法制备明胶得率始终维持较低水平,表明酸碱法和酸酶法在工业化生产中更具得率优势。基于得率考虑,本研究采用酸碱法进行预处理,并在60 ℃、6 h条件下进行水热提取。
表1 不同水热提取条件下3 种方法制备明胶的得率
Table 1 Yields of gelatins using three methods under different hydrothermal extraction conditions
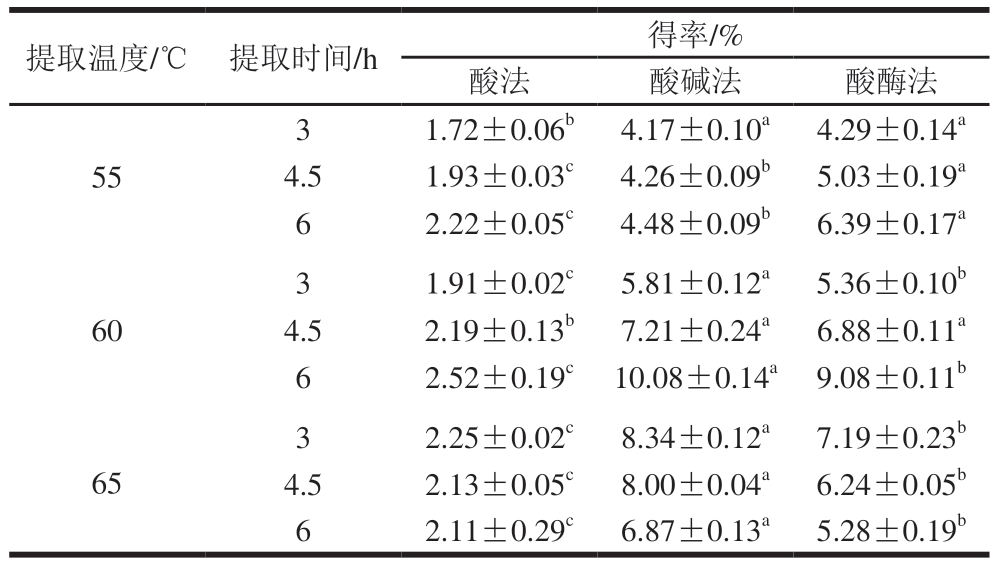
注:同行小写字母不同表示显著差异(P<0.05)。表2~4同。
提取温度/℃提取时间/h得率/%酸法酸碱法酸酶法55 31.72±0.06b4.17±0.10a4.29±0.14a 4.51.93±0.03c4.26±0.09b5.03±0.19a 62.22±0.05c4.48±0.09b6.39±0.17a 60 31.91±0.02c5.81±0.12a5.36±0.10b 4.52.19±0.13b7.21±0.24a6.88±0.11a 62.52±0.19c10.08±0.14a9.08±0.11b 32.25±0.02c8.34±0.12a7.19±0.23b 4.52.13±0.05c8.00±0.04a6.24±0.05b 62.11±0.29c6.87±0.13a5.28±0.19b 65
2.4.1 明胶基础成分组成
由表2可知,相较于鸡头,明胶粗蛋白含量更高,水分、脂肪和灰分含量更低,表明预处理、前处理、提取和干燥已有效去除鸡头中的脂肪、矿物质、水分和其他杂质。酸法、酸碱法及酸酶法制备明胶的灰分含量均符合GB 6783—2013和QB/T 4087—2010《食用明胶》的限量要求(灰分质量分数≤2.0%)。值得注意的是,灰分含量通常与明胶纯度呈负相关,低灰分往往意味着更高的品质。其中,酸碱法制备明胶具有最高的粗蛋白含量和最低的灰分含量,可判定该工艺制备的明胶具有更高的质量[27]。
表2 酸法、酸碱法及酸酶法制备明胶的基础成分含量
Table 2 Basic component contents of gelatin prepared by acid,alkaline-acid, acid-enzymatic methods %

基础成分酸法酸碱法酸酶法水分质量分数14.55±0.27b15.89±0.15a15.58±0.29a粗脂肪质量分数1.15±0.08b2.12±0.13a1.93±0.16a粗蛋白质量分数64.63±0.06b77.33±0.32a57.43±0.15c灰分质量分数1.45±0.21a0.90±0.03b1.39±0.13a
2.4.2 明胶色泽
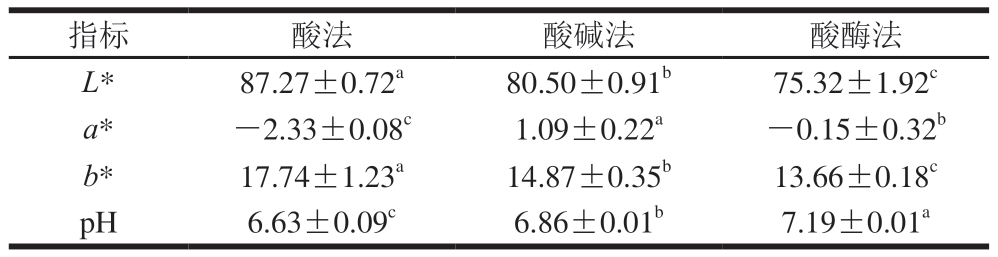
色泽虽会影响明胶成品外观和消费者接受度,但对其实际应用品质无显著影响[28]。由表3可知,酸法、酸碱法及酸酶法制备明胶色泽参数存在显著差异(P<0.05)。其中,酸碱法制备明胶a*最高,L*和b*也相对较高,表明其色泽明亮且偏黄,呈现较为天然的浅琥珀色,这与其提取过程中酸碱处理导致的色素溶出特性相关。
表3 酸法、酸碱法及酸酶法制备明胶色泽和pH值
Table 3 Color parameters and pH value of gelatin prepared by acid,acid-alkali and acid-enzyme methods
指标酸法酸碱法酸酶法L*87.27±0.72a80.50±0.91b75.32±1.92c a*-2.33±0.08c1.09±0.22a-0.15±0.32b b*17.74±1.23a14.87±0.35b13.66±0.18c pH6.63±0.09c6.86±0.01b7.19±0.01a
2.4.3 明胶pH值
Gómez-Guillén等[29]报道称,A型明胶pH值一般为7~9,B型明胶一般为4~5。由表3可知,3 种明胶pH值均符合A型明胶特征。其中,酸法制备明胶pH值为6.63,可能源于乙酸残留或pH值调节过程产生的影响;酸碱法制备明胶pH值为6.86,呈中性偏酸;酸酶法制明胶pH值为7.19,呈中性偏碱,考虑为pH值调节过程所使用的碱溶液残留导致。综上所述,明胶pH值受处理过程所使用酸、碱等提取试剂浓度及洗涤条件的共同调控。
2.4.4 明胶pI
明胶pI是指明胶分子在溶液中表面正负电荷数相等,净电荷为零时的pH值[30]。而Zeta电位与蛋白质表面净电荷有关,一般认为Zeta电位达到0 mV时的pH值为pI[31]。由图3可知,酸法和酸酶法制备明胶pI分别为6.39和6.35,而酸碱法制备明胶pI略高,为8.21,这是由于碱处理可诱导胶原蛋白脱酰胺化,将酰胺基团转化为羧基,增加负电荷基团数量,为维持电荷平衡需更高pH值环境。综上,3 种明胶pI均符合A型明胶特征。
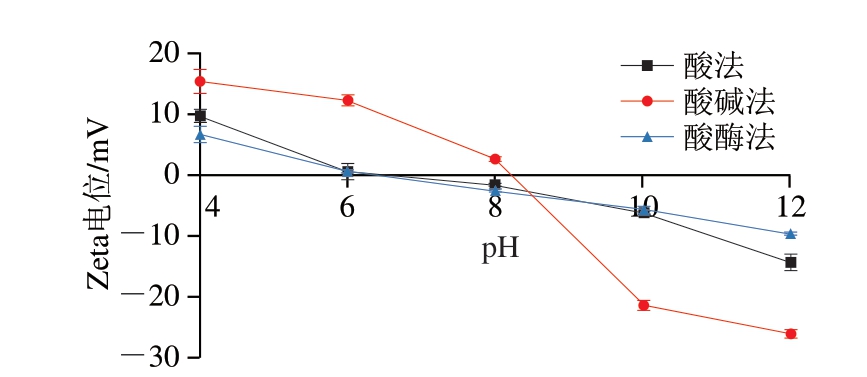
图3 酸法、酸碱法及酸酶法制备明胶pI
Fig. 3 Isoelectric point of gelatin prepared by acid, alkaline-acid,acid-enzymatic methods
2.4.5 明胶纯度
Usman等[32]报道,明胶纯度由胶原蛋白含量和前处理工艺共同调控。羟脯氨酸作为胶原蛋白的特征性氨基酸[33],其含量在不同物种胶原蛋白中保持相对稳定,可作为评估明胶纯度的可靠指标[34]。由表4可知,酸法、酸碱法及酸酶法制备明胶羟脯氨酸质量分数分别为9.56%、10.27%和9.40%,按照转换系数推算胶原蛋白质量分数分别为68.28%、73.33%和67.12%。其中,酸碱法制备明胶的胶原蛋白含量显著高于其他组(P<0.05),表现出最优纯度,表明该处理方法能最大限度保留胶原蛋白结构,避免过度水解,具有更广阔的应用前景。值得注意的是,原料鸡头中的羟脯氨酸质量分数为4.26%,胶原蛋白质量分数为30.39%,表明提取过程有效实现了不溶性胶原蛋白向可溶性明胶的转化。
表4 酸法、酸碱法及酸酶法制备明胶羟脯氨酸与胶原蛋白质量分数
Table 4 Mass fractions of hydroxyproline and collagen in gelatin prepared by acid, alkaline-acid, acid-enzymatic methods%

指标酸法酸碱法酸酶法羟脯氨酸质量分数9.56±0.30b10.27±0.29a9.40±0.30b胶原蛋白质量分数68.28±2.14b73.33±2.08a67.12±2.11b
2.4.6 明胶氨基酸组成
基于HPLC法分析明胶氨基酸组成可有效鉴别明胶类别和胶原蛋白来源。其中,酸法和酸酶法因无碱处理步骤,所制备明胶可直接判定为A型明胶,而酸碱法制备明胶同时存在酸碱处理,需经氨基酸组成分析以判断明胶类型。明胶中应不含胱氨酸或半胱氨酸[35]。由表5可知,酸法、酸碱法及酸酶法制备明胶均未检出胱氨酸,符合明胶基本特征。A型明胶中,胶原蛋白的特征性氨基酸包括甘氨酸、脯氨酸和羟脯氨酸,以甘氨酸含量最高[36],脯氨酸和羟脯氨酸相对含量总和应超20%。酸法、酸碱法和酸酶法制备明胶甘氨酸相对含量分别为32.29%、33.38%和34.81%,脯氨酸和羟脯氨酸相对含量分别为20.08%、20.03%和20.17%,均符合A型明胶特征。酸酶法制备明胶甘氨酸相对含量最高,其次为酸碱法,甘氨酸含量与胶原蛋白水解程度呈现正相关[37],表明酸酶法和酸碱法处理能够提高胶原蛋白水解效率。
表5 酸法、酸碱法及酸酶法制备明胶氨基酸组成与相对含量
Table 5 Amino acid composition and relative content of gelatin prepared by acid, alkaline-acid, acid-enzymatic methods%
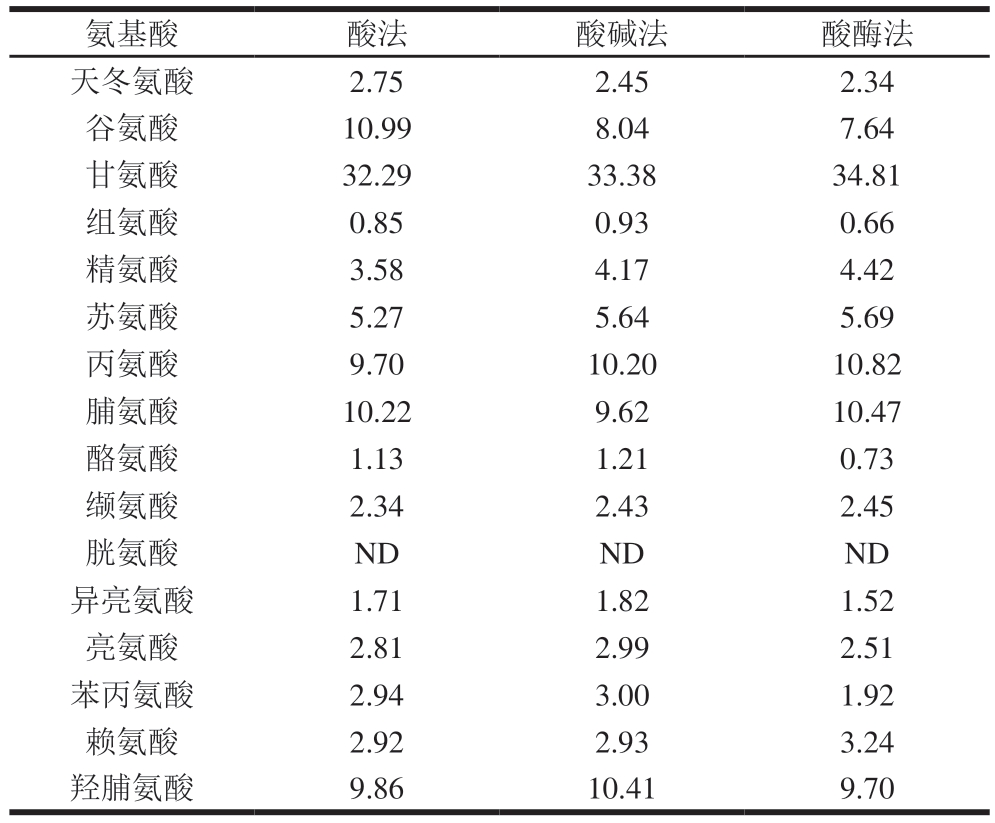
注:ND.未检出。
氨基酸酸法酸碱法酸酶法天冬氨酸2.752.452.34谷氨酸10.998.047.64甘氨酸32.2933.3834.81组氨酸0.850.930.66精氨酸3.584.174.42苏氨酸5.275.645.69丙氨酸9.7010.2010.82脯氨酸10.229.6210.47酪氨酸1.131.210.73缬氨酸2.342.432.45胱氨酸NDNDND异亮氨酸1.711.821.52亮氨酸2.812.992.51苯丙氨酸2.943.001.92赖氨酸2.922.933.24羟脯氨酸9.8610.419.70
2.5.1 明胶凝胶强度
凝胶强度由Bloom值表征,是评价明胶品质的重要指标[38],反映其形成凝胶网络的能力。高Bloom值表明明胶具有更好的贮藏稳定性和抗变形能力[39]。酸法、酸碱法及酸酶法制备明胶Bloom值分别为382.50、302.02、360.96 g。其中,酸法与酸酶法制备明胶Bloom值差异不显著(P>0.05),二者均显著高于酸碱法制备明胶(P<0.05)。Bloom值主要由α肽链和β肽链含量决定[40],酸碱处理会加剧胶原蛋白水解,导致α/β肽链降解为小分子肽段,三螺旋结构破坏[41],从而导致凝胶强度降低。A型明胶Bloom值较高(>250 g),属于高品质明胶,而B型明胶Bloom值较低(<150 g),属于低品质明胶。本研究3 种明胶Bloom值均符合A型明胶特征。
2.5.2 明胶溶解度
明胶溶解度是反映其在特定溶剂中溶解能力的重要指标。Ahmad等[42]研究表明,当溶液pH值接近明胶pI,其溶解度最低,这种现象源于明胶分子间静电斥力减弱而疏水相互作用增强,导致分子聚集沉淀。相反,当pH值远离pI时,明胶分子处于去质子化(pH值>pI)或质子化状态(pH值<pI),分子静电荷增加,静电斥力增强,从而导致溶解度升高。因此,溶解度-pH值曲线的最低点可指示明胶的pI。由图4可知,酸酶法、酸法和酸碱法制备明胶溶解度分别在pH 6、7、8降至最低(82.58%、21.88%和39.17%),表明其pI分别位于pH 6、7、8附近。由溶解度分析可知,酸酶法制备明胶表现出卓越的pH值稳定性,其溶解度恒定在85%~95%之间。与之相比,酸碱法制备明胶pI位于弱碱性区域,这一特性可保证其能够在远离pI的酸性和中性区域维持较高的溶解度。pH 7时,酸碱法制备明胶溶解度可达66.81%,虽低于酸酶法制备明胶的86.16%,但明显高于酸法制备明胶的21.88%。因此,可认为酸碱法制备明胶具有适中的溶解度。
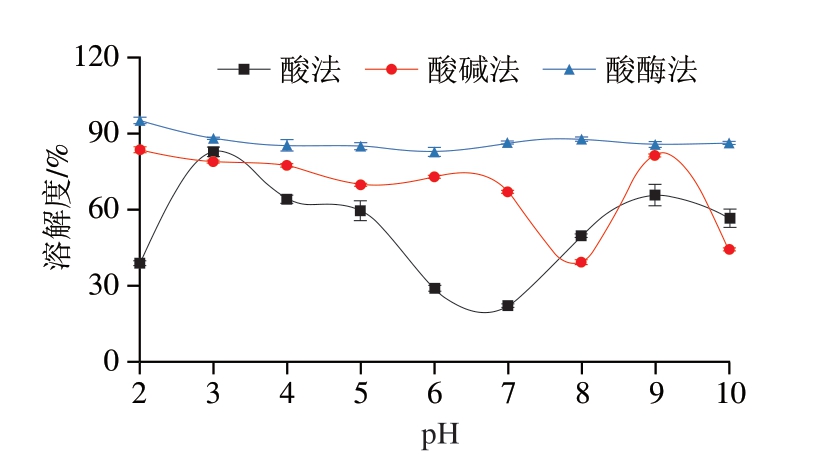
图4 不同pH值缓冲溶液对明胶溶解度的影响
Fig. 4 Effect of different pH buffer solutions on gelatin solubility
酸法制备明胶溶解度在pI附近最低,这是因为其溶液pH值(6.63)与pI(6.39)相近,导致Zeta电位趋近于0,静电斥力消失引发明胶分子疏水聚集。相比之下,酸碱法和酸酶法制备明胶在pI附近的溶解度均高于酸法明胶,这是由于两者溶液pH值(6.86和7.19)均远离pI(8.21和6.35),使明胶分子保持质子化或去质子化状态,Zeta电位绝对值增大,静电斥力增强,从而维持较高溶解度。这些结果不仅符合明胶溶解度-pH值曲线指示pI的规律,还佐证了Zeta电位随pH值变化的结果。
2.5.3 明胶动态黏弹性
G’和G”能够反映明胶的弹性和黏性特性[43]。Sila等[44]报道,在加热和冷却过程中,G’和G”曲线的交叉点可用于确定明胶熔点(Tmelt)和胶凝点(Tgel)。在加热过程中,G’急剧下降而G”迅速上升且G”>G’时,表明明胶从凝胶态(G’>G”)转变为溶胶态(G”>G’),此时交点温度即为Tmelt。在冷却过程中,G’急剧上升而G”急剧下降且G’>G”时,交叉点温度即为Tgel。由图5~7可知,酸法制备明胶Tmelt和Tgel分别位于35.05~36.05 ℃和26.93~25.93 ℃,酸碱法制备明胶Tmelt和Tgel分别位于33.04~34.04 ℃和23.06~21.06 ℃,酸酶法制备明胶Tmelt和Tgel分别位于36.04~37.04 ℃和24.93~23.93 ℃。
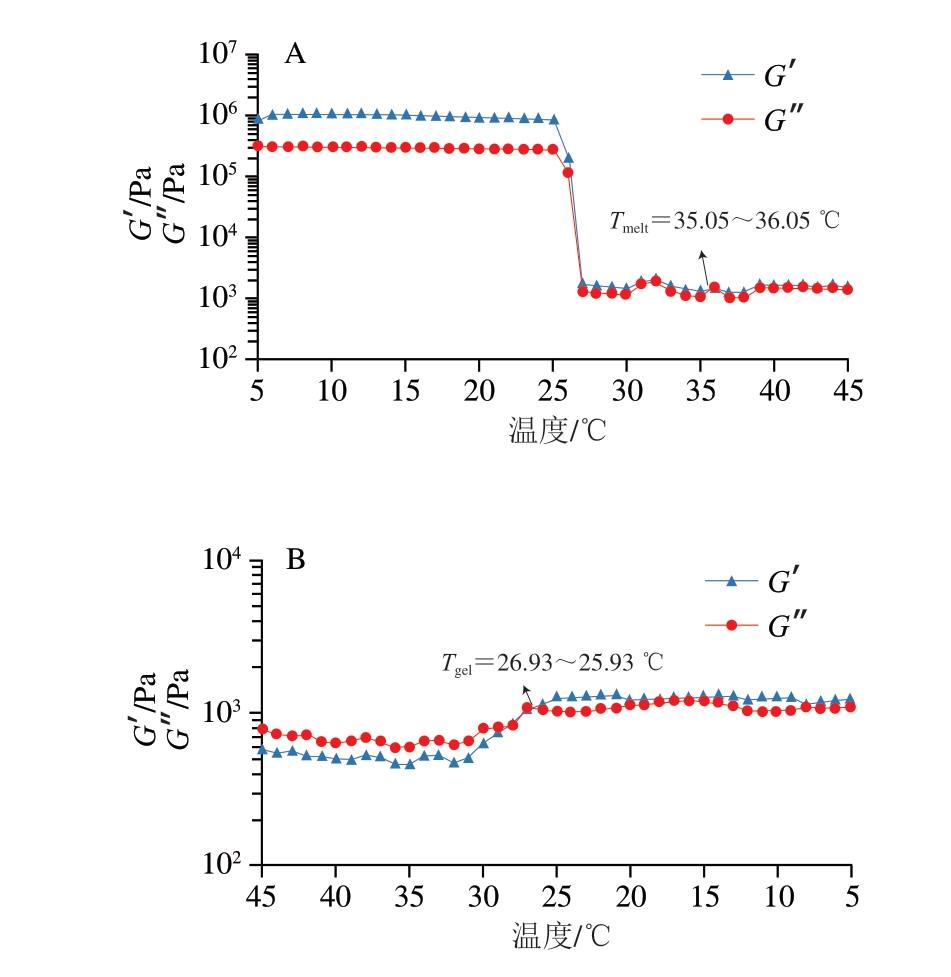
图5 酸法制备明胶加热(A)和冷却(B)过程中黏弹性变化
Fig. 5 Evolution of the viscoelasticity of gelatin prepared by the acid method during heating (A) and cooling (B) processes
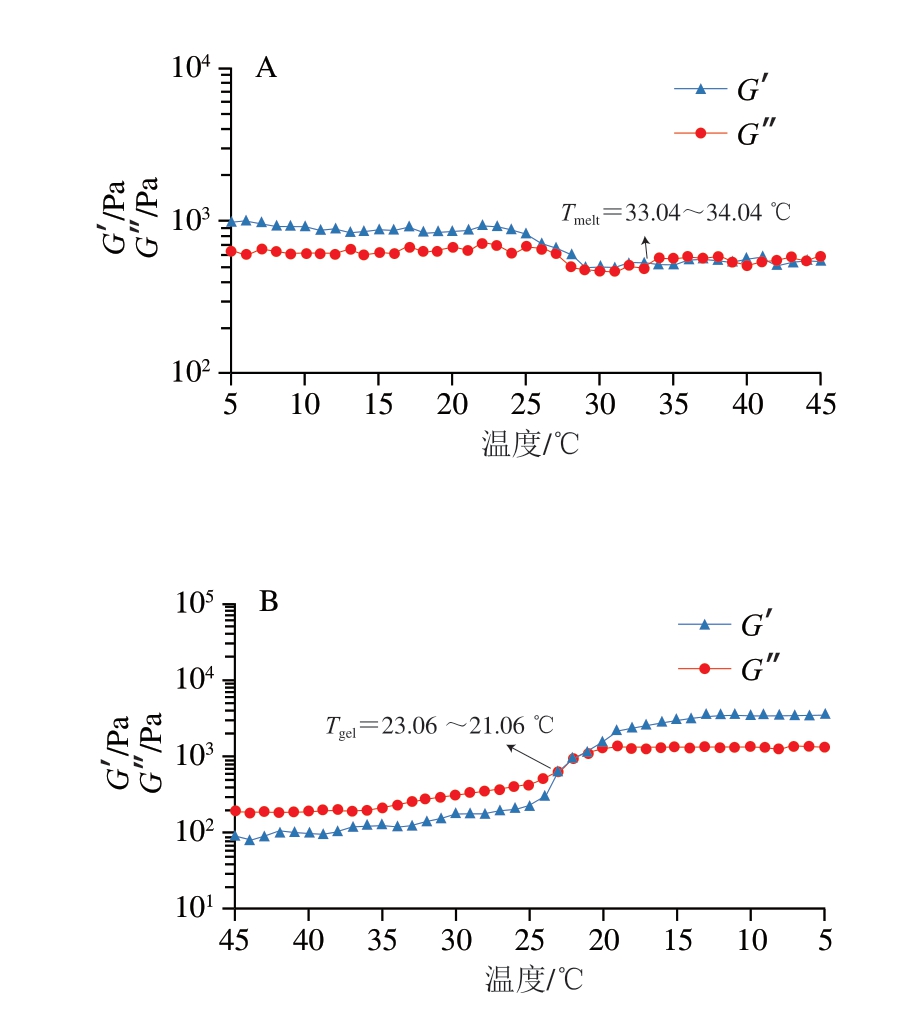
图6 酸碱法制备明胶加热(A)和冷却(B)过程中黏弹性的变化
Fig. 6 Evolution of the viscoelasticity of gelatin prepared by the alkaline-acid method during heating (A) and cooling (B) processes
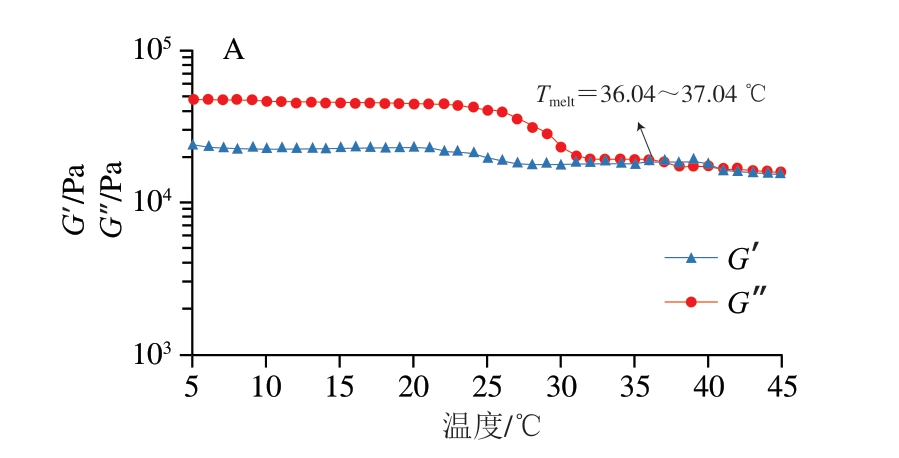
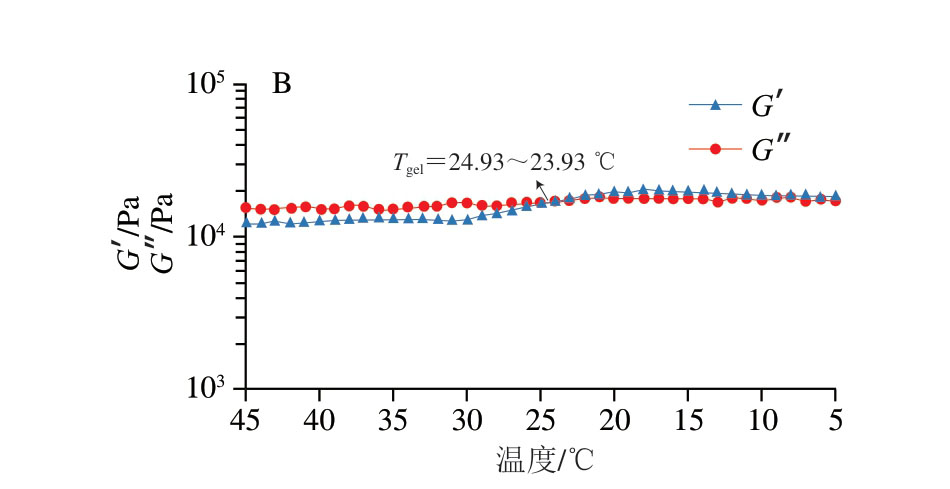
图7 酸酶法制备明胶加热(A)和冷却(B)过程中黏弹性的变化
Fig. 7 Evolution of the viscoelasticity of gelatin prepared by the acid-enzymatic method during heating (A) and cooling (B) processes
对比分析表明,3 种方法制备明胶Tmelt依次为酸酶法>酸法>酸碱法,Tgel依次为酸法>酸酶法>酸碱法。其中,酸碱法制备明胶Tmelt和Tgel均最低,这可能与脯氨酸相对含量较低(9.62%,低于A型明胶的10%~18%)有关,这些亚氨基酸的减少会影响明胶的热稳定性[45],导致Tmelt和Tgel降低。此外,明胶的黏弹性与其分子质量分布密切相关[18]。吴诗雨等[46]研究指出,明胶Tmelt和Tgel不仅受氨基酸组成影响,还受明胶分子质量调控。分子质量越高,表明在提取过程中胶原蛋白水解程度越低,分子链保留越完整。高分子质量是明胶形成高强度凝胶网络的关键,主要表现为高Bloom值和低溶解度,需更高的温度熔断网络或更低的温度形成凝胶。Tmelt和Tgel降低与低分子质量组分含量高有关[19],其中酸碱法制备明胶Bloom值较低且甘氨酸相对含量与溶解度较高,Tmelt和Tgel均最低,说明酸碱法制备明胶在提取过程中胶原蛋白水解程度较高,符合低分子质量明胶的特征,且低分子质量组分含量高。酸酶法与酸碱法制备明胶分子质量特征和各组分含量较为一致。而酸法制备明胶Tmelt和Tgel均最高,表明其高分子质量组分含量较高,而其具有的低溶解度、高Bloom值及低甘氨酸相对含量也符合高分子质量明胶的特征。综上,酸碱法制备明胶的低Tmelt和低Tgel使其在食品工业中具有低温加工适应性,能够缩短生产周期,优化食用明胶口感,并有利于开发功能性食品。
该研究系统考察脱脂方式对脱脂率、NaCl含量对酸碱法明胶得率、水热提取参数及不同提取方式对鸡头明胶得率的影响。结果表明,碱溶液脱脂效果最佳,10 g/L NaCl最有利于酸碱法制备明胶得率的提升,最佳水热提取参数为60 ℃、6 h,酸碱法处理可获得最佳提取效果。在理化特性方面,酸碱法制备明胶展现出显著优势,其得率、蛋白质和胶原蛋白含量均为最高。高得率和高蛋白质含量表明该工艺能充分提取原料有效成分,产物纯度高、品质佳;而较高的胶原蛋白含量则说明明胶分子链保存完整,在加工过程中未发生显著水解或破坏。此外,酸碱法明胶呈现出天然浅琥珀色,色泽明亮,具有良好感官特性。结构和功能特性指标分析显示,酸碱法制备明胶具有典型A型明胶特征,高凝胶强度赋予其稳定的三维网状结构,较高的甘氨酸与亚氨基酸相对含量有利于维持三螺旋结构稳定性,这些特性为其高附加值应用提供了可行性。同时,适中的溶解度、较宽的pH值适应范围及良好的低温加工适应性能够保证其贮藏稳定性,拓展其在功能性食品开发中的应用前景。
综上所述,与传统酸法工艺相比,酸碱法结合水热提取制备鸡头明胶在得率方面具有显著优势,且明胶成品表现出更优良的性能。本研究可为推动鸡头从低附加值屠宰废弃物向高附加值生物材料方向发展提供理论基础,实现鸡副产物的高效资源化利用。
[1] ZOU Y, CHEN X Y, LAN Y B, et al. Find alternative for bovine and porcine gelatin: study on physicochemical, rheological properties and water-holding capacity of chicken lungs gelatin by ultrasound treatment[J]. Ultrasonics Sonochemistry, 2024, 109: 107004.DOI:10.1016/j.ultsonch.2024.107004.
[2] ABEDINIA A, MOHAMMADI NAFCHI A, SHARIFI M, et al.Poultry gelatin: characteristics, developments, challenges, and future outlooks as a sustainable alternative for mammalian gelatin[J]. Trends in Food Science & Technology, 2020, 104: 14-26. DOI:10.1016/j.tifs.2020.08.001.
[3] ROMERO-GARAY M G, MONTALVO-GONZÁLEZ E,HERNÁNDEZ-GONZÁLEZ C, et al. Bioactivity of peptides obtained from poultry by-products: a review[J]. Food Chemistry: X, 2022, 13:100181. DOI:10.1016/j.fochx.2021.100181.
[4] ABDALLAH M M, FERNÁNDEZ N, MATIAS A A, et al. Hyaluronic acid and chondroitin sulfate from marine and terrestrial sources:extraction and purification methods[J]. Carbohydrate Polymers, 2020,243: 116441. DOI:10.1016/j.carbpol.2020.116441.
[5] 张跃宏, 代浪浪, 杨晨, 等. 明胶基薄膜的制备方法及在食品包装中的应用研究进展[J]. 精细化工, 2024, 41(12): 2603-2615.DOI:10.13550/j.jxhg.20231001.
[6] 刘松林, 张兵, 王爱东, 等. 酶法明胶在空心胶囊应用方面的研究[J].化工设计通讯, 2024, 50(10): 99-101. DOI:10.37155/2972-4333-0212-28.
[7] 刘颖, 魏敏, 杨平华, 等. 明胶/PVA类肥料包膜材料的制备与环保性能研究[J]. 中国农学通报, 2021, 37(14): 90-96. DOI:10.32629/eep.v3i4.742.
[8] KARIM A A, BHAT R. Fish gelatin: properties, challenges,and prospects as an alternative to mammalian gelatins[J].Food Hydrocolloids, 2009, 23(3): 563-576. DOI:10.1016/j.foodhyd.2008.07.002.
[9] ZHANG T, SUN R, DING M Z, et al. Effect of extraction methods on the structural characteristics, functional properties, and emulsion stabilization ability of tilapia skin gelatins[J]. Food Chemistry, 2020,328: 127114. DOI:10.1016/j.foodchem.2020.127114.
[10] GÓMEZ-GUILLÉN M C, TURNAY J, FERNÁNDEZ-DÍAZ M D, et al.Structural and physical properties of gelatin extracted from different marine species: a comparative study[J]. Food Hydrocolloids, 2002,16(1): 25-34. DOI:10.1016/S0268-005X(01)00035-2.
[11] EE S C, SAARI N, ABAS F, et al. Properties of chicken head gelatins as affected by extraction method[J]. International Food Research Journal, 2019, 26(2): 499-508.
[12] YU E M, PAN C Y, CHEN W J, et al. Gelatin from specific freshwater and saltwater fish extracted using six different methods: component interactions, structural characteristics, and functional properties[J].LWT-Food Science and Technology, 2024, 191: 115656. DOI:10.1016/j.lwt.2023.115656.
[13] ABEDINIA A, ARIFFIN F, HUDA N, et al. Extraction and characterization of gelatin from the feet of Pekin duck (Anas platyrhynchos domestica) as affected by acid, alkaline, and enzyme pretreatment[J]. International Journal of Biological Macromolecules,2017, 98: 586-594. DOI:10.1016/j.ijbiomac.2017.01.139.
[14] BHARGAVI P K, BANERJEE R, MD R, et al. Sustainable gelatin extraction from poultry skin-head-feet blend: an ultrasound-assisted approach[J]. Poultry Science, 2025, 104(4): 104975. DOI:10.1016/j.psj.2025.104975.
[15] AIDAT O, BELKACEMI L, BELALIA M, et al. Physicochemical,rheological, and textural properties of gelatin extracted from chicken by-products (feet-heads) blend and application[J]. International Journal of Gastronomy and Food Science, 2023, 32: 100708. DOI:10.1016/j.ijgfs.2023.100708.
[16] HE X, LIN L, JIANG S T, et al. Characterization of acid-soluble collagen (ASC) derived from walleye pollock and silver carp skin and comparison them with the collagen from pig and duck skin[J]. Food Chemistry Advances, 2024, 4: 100746. DOI:10.1016/j.focha.2024.100746.
[17] 谭佳, 王雅欣, 甄大卫, 等. 鸡脚脱脂除杂蛋白预处理工艺[J]. 精细化工, 2021, 38(1): 138-146. DOI:10.13550/j.jxhg.20200484.
[18] DU L, KHIARI Z, PIETRASIK Z, et al. Physicochemical and functional properties of gelatins extracted from turkey and chicken heads[J]. Poultry Science, 2013, 92(9): 2463-2474. DOI:10.3382/ps.2013-03161.
[19] EE S C, BAKAR J, SAARI N, et al. Rheological and molecular properties of chicken head gelatin as affected by combined temperature and time using warm water rendering[J]. International Journal of Food Properties,2021, 24(1): 1495-1509. DOI:10.1080/10942912.2021.1978484.
[20] NALINANON S, BENJAKUL S, VISESSANGUAN W, et al.Improvement of gelatin extraction from bigeye snapper skin using pepsin-aided process in combination with protease inhibitor[J].Food Hydrocolloids, 2008, 22(4): 615-622. DOI:10.1016/j.foodhyd.2007.01.012.
[21] 侯钰柯, 王鹏, 徐幸莲, 等. 不同鸡肉香精对鸡汤食用品质的影响[J].食品与发酵工业, 2023, 49(4): 77-87. DOI:10.13995/j.cnki.11-1802/ts.030302.
[22] GÁL R, MOKREJŠ P, MRÁZEK P, et al. Chicken heads as a promising by-product for preparation of food gelatins[J]. Molecules,2020, 25(3): 494. DOI:10.3390/molecules25030494.
[23] KURT A, TOKER O S, AKBULUT M, et al. Textural, rheological, and structural properties of Turkey and chicken gelatins from mechanical deboning residues[J]. Food Science & Nutrition, 2024, 12(7): 4952-4965. DOI:10.1002/fsn3.4143.
[24] OYMACI P, OFFERINGA P E, BORNEMAN Z, et al. Effect of osmotic pressure on whey protein concentration in forward osmosis[J].Membranes, 2021, 11(8): 573. DOI:10.3390/membranes11080573.
[25] SINGH P, BENJAKUL S, MAQSOOD S, et al. Isolation and characterisation of collagen extracted from the skin of striped catfish(Pangasianodon hypophthalmus)[J]. Food Chemistry, 2011, 124(1):97-105. DOI:10.1016/j.foodchem.2010.05.111.
[26] ERGE A, ZORBA Ö. Optimization of gelatin extraction from chicken mechanically deboned meat residue using alkaline pre-treatment[J].LWT-Food Science and Technology, 2018, 97: 205-212. DOI:10.1016/j.lwt.2018.06.057.
[27] YAHDIANA H, IRWANDI J, EFFIONORA A. Characterization and functional properties of gelatin extracted from goatskin[J].International Food Research Journal, 2018, 25(1): 275-281.
[28] YANG H J, WANG H F, HUANG M, et al. Repurposing fish waste into gelatin as a potential alternative for mammalian sources:a review[J]. Comprehensive Reviews in Food Science and Food Safety,2022, 21(2): 942-963. DOI:10.1111/1541-4337.12920.
[29] GÓMEZ-GUILLÉN M C, GIMÉNEZ B, LÓPEZ-CABALLERO M E,et al. Functional and bioactive properties of collagen and gelatin from alternative sources: a review[J]. Food Hydrocolloids, 2011, 25(8):1813-1827. DOI:10.1016/j.foodhyd.2011.02.007.
[30] KEPPLER J K, HEYSE A, SCHEIDLER E, et al. Towards recombinantly produced milk proteins: physicochemical and emulsifying properties of engineered whey protein β-lactoglobulin variants[J]. Food Hydrocolloids, 2021, 110: 106132. DOI:10.1016/j.foodhyd.2020.106132.
[31] LAUTENBACH V, HOSSEINPOUR S, PEUKERT W. Isoelectric point of proteins at hydrophobic interfaces[J]. Frontiers in Chemistry,2021, 9: 712978. DOI:10.3389/fchem.2021.712978.
[32] USMAN M, ISHAQ A, MAC REGENSTEIN J, et al. Valorization of animal by-products for gelatin extraction using conventional and green technologies: a comprehensive review[J]. Biomass Conversion and Biorefinery, 2023: 1-13. DOI:10.1007/s13399-023-04547-5.
[33] ISLAM M R, YUHI T, MENG D W, et al. Purity and properties of gelatins extracted from the head tissue of the hybrid Kalamtra sturgeon[J]. LWT-Food Science and Technology, 2021, 142: 110944.DOI:10.1016/j.lwt.2021.110944.
[34] AKSUN TÜMERKAN E T, CANSU Ü, BORAN G, et al.Physiochemical and functional properties of gelatin obtained from tuna, frog and chicken skins[J]. Food Chemistry, 2019, 287: 273-279.DOI:10.1016/j.foodchem.2019.02.088.
[35] SUN X D, HOLLEY R A. Factors influencing gel formation by myofibrillar proteins in muscle foods[J]. Comprehensive Reviews in Food Science and Food Safety, 2011, 10(1): 33-51. DOI:10.1111/j.1541-4337.2010.00137.x.
[36] VENUPRIYA V, KRISHNAVENI V, RAMYA M. Effect of acidic and alkaline pretreatment on functional, structural and thermal properties of gelatin from waste fish scales[J]. Polymer Bulletin, 2023, 80(9):10533-10567. DOI:10.1007/s00289-022-04600-9.
[37] AL-HASSAN A A. Gelatin from camel skins: extraction and characterizations[J]. Food Hydrocolloids, 2020, 101: 105457.DOI:10.1016/j.foodhyd.2019.105457.
[38] PORTANGUEN S, DUMOULIN C, DUCONSEILLE A, et al.Impact of water content and bloom index on gelatin glycation[J].Food Hydrocolloids, 2023, 145: 109096. DOI:10.1016/j.foodhyd.2023.109096.
[39] BAYDIN T, AARSTAD O A, DILLE M J, et al. Long-term storage stability of type A and type B gelatin gels: the effect of Bloom strength and co-solutes[J]. Food Hydrocolloids, 2022, 127: 107535.DOI:10.1016/j.foodhyd.2022.107535.
[40] 黄丽金, 闻怡凡, 罗美玲, 等. 提取温度对乌鱼鱼鳞明胶功能性质和结构特性的影响[J]. 食品工业科技, 2024, 45(9): 83-90.DOI:10.13386/j.issn1002-0306.2023060092.
[41] 詹丽, 陈雪岚. 鱼明胶特性及改性对其品质影响的研究进展[J]. 食品工业科技, 2021, 42(23): 385-393. DOI:10.13386/j.issn1002-0306.2020090047.
[42] AHMAD M, BENJAKUL S. Characteristics of gelatin from the skin of unicorn leatherjacket (Aluterus monoceros) as influenced by acid pretreatment and extraction time[J]. Food Hydrocolloids, 2011, 25(3):381-388. DOI:10.1016/j.foodhyd.2010.07.004.
[43] 王加雯, 陈安妮, 舒圣, 等. 透明质酸对鱼明胶凝胶性能和结构特征的影响[J]. 食品与发酵工业, 2024, 50(22): 123-130. DOI:10.13995/j.cnki.11-1802/ts.038027.
[44] SILA A, MARTINEZ-ALVAREZ O, KRICHEN F, et al. Gelatin prepared from European eel (Anguilla anguilla) skin: physicochemical,textural, viscoelastic and surface properties[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2017, 529: 643-650.DOI:10.1016/j.colsurfa.2017.06.032.
[45] ABUIBAID A, ALSENAANI A, HAMED F, et al. Microstructural,rheological, gel-forming and interfacial properties of camel skin gelatin[J]. Food Structure, 2020, 26: 100156. DOI:10.1016/j.foostr.2020.100156.
[46] 吴诗雨, 陈楠, 杨文鸽, 等. 不同pH值条件下超声波辅助水浴提取对鱼鳞明胶凝胶特性、流变特性和结构特性的影响[J]. 食品科学,2024, 45(15): 178-185. DOI:10.7506/spkx1002-6630-20240123-205.