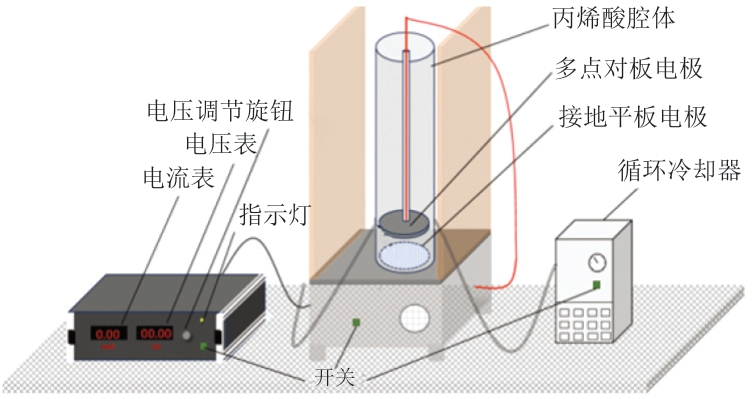
图1 HVEF实验装置示意图
Fig. 1 Schematic diagram of HVEF device
Effects of High Voltage Electrostatic Field Treatment on Muscle Quality and Water Distribution Characteristics in Channel Catfish
张贤珊, 郭兵兵, 石柳, 等. 高压静电场处理对鮰鱼肌肉品质和水分分布特性的影响[J]. 肉类研究, 2026, 40(5): 27-35.DOI:10.7506/rlyj1001-8123-20250516-155. http://www.rlyj.net.cn
ZHANG Xianshan, GUO Bingbing, SHI Liu, et al. Effects of high voltage electrostatic field treatment on muscle quality and water distribution characteristics in channel catfish[J]. Meat Research, 2026, 40(5): 27-35. DOI:10.7506/rlyj1001-8123-20250516-155. http://www.rlyj.net.cn
斑点叉尾鮰(Ictalurus punctatus)作为全球最重要的淡水养殖品种鱼之一,自1984年由湖北省水产科学研究所从美国加利福尼亚州引入我国后,已成为我国具显著经济价值的特色淡水渔业资源[1]。统计[2]数据显示,2022年,我国鮰鱼产量达4.162×105 t。鮰鱼因富含优质蛋白质及多不饱和脂肪酸[3]而深受大众喜爱,然而,其以鲜销[4]为主,保鲜期较短,且易受微生物污染,从而影响品质[5],这极大限制了鮰鱼产业的发展。延长鮰鱼的保鲜期并保持其品质成为研究热点。冷藏作为最常用的保鲜方法之一,通过低温抑制微生物生长、降低酶活性,以此达到保鲜的目的。但低温只能抑制微生物生长,并不能彻底杀灭微生物[6],且长期冷藏可能导致鱼肉品质下降[7]。随着消费者对食品质量安全要求的提升,开发新型保鲜技术以突破传统冷藏技术瓶颈已成为当前水产品加工领域的研究热点。
高压静电场(high voltage electrostatic field,HVEF)技术通过施加高压电场产生的电穿孔效应、离子迁移现象和活性物质能有效抑制微生物生长并延缓酶促反应[8]。近年来,HVEF技术在食品保鲜、干燥、速冻和解冻等领域展现出独特优势[9]。电场作用下,肽键(C=O与N—H)偶极矩增强会破坏蛋白质氢键网络并暴露疏水核心,导致二级结构(如α-螺旋、β-折叠)解旋与重排。水分是鱼肉中最重要的组成成分之一,其分布状态和迁移行为直接影响鱼肉的持水力和感官品质[10]。研究[11]表明,鱼类肌肉中盐溶性蛋白在加热作用下通过分子间疏水相互作用和氢键包裹水分,重新形成立体网状结构,成为具有凝胶特性的鱼糜制品。此外,HVEF还会诱导蛋白质分子构象发生变化,从而影响鱼肉的微观结构和品质[10]。杨娇等[12]通过对比实验发现,与传统热风干燥相比,HVEF对马铃薯蛋白质二级结构的影响更小,这表明HVEF可能是一种对蛋白质结构影响较小的干燥方法。在鱼类保鲜中,HVEF处理已被证明能够改善鱼肉的持水力[13]、嫩度[14]和色泽[15]。在食品解冻方面,研究发现,HVEF可以产生小而均匀的冰晶,对肌肉组织的损伤较小[16],可用于解冻冷冻肉制品(如猪肉、鸡肉和鱼类),提高其质构特性和蛋白含量[17]。然而,目前关于HVEF处理对鮰鱼片水分分布、分子间作用力及品质特性的影响机制研究仍较少,尤其是不同处理时间对鮰鱼片品质的影响尚未被系统探讨。
本研究通过表征组织结构、测定分子间作用力、傅里叶变换红外光谱、十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)、pH值、剪切力、白度、水分含量、持水力和水分分布等指标,研究HVEF处理对鮰鱼片品质的影响,为HVEF对鮰鱼片的保鲜提供基础理论依据。
鲜活斑点叉尾鮰购于湖北省武汉市白沙洲水产品批发市场,每尾质量(3.00±0.05)kg。
氯化钠、盐酸、SDS 国药集团化学试剂有限公司;考马斯亮蓝 南京建成生物有限公司;蛋白上样缓冲液 武汉科瑞生物技术有限公司;蛋白上样缓冲液(含β-巯基乙醇) 上海圻明生物科技有限公司;以上试剂均为分析纯。
HVEF装置 本实验室自主研发;IKA均质机广州东南科创科技有限公司;PL602-L电子天平 梅特勒-托利多仪器(上海)有限公司;Gen Pure纯水仪 美国赛默飞世尔科技公司;TA.XT Plus质构仪 英国Stable Micro System公司;VERTEX 70傅里叶变换红外光谱仪德国Bruker Optice公司;PB-10 pH计 德国Sartorius公司;CR-400色差仪 柯尼卡-美能达(中国)投资有限公司;NMI20-025V-I低场核磁共振(low-field nuclear magnetic resonance,LF-NMR)仪 苏州纽迈分析仪器股份有限公司;Nano ZS+MPT-2纳米粒度及电位分析仪英国马尔文仪器有限公司;YYSX-1400光学显微镜上海仪圆仪器有限公司。
1.3.1 样品预处理
将鲜活鮰鱼击晕后去头、去尾、去皮,用超净水洗净,取背部肌肉切块,制备成4 cm×4 cm×1 cm、质量(15.0±0.1)g的鱼片。实验设计采用生物学重复原则,以个体为单位设置平行样本,共进行3 次独立重复实验。
1.3.2 HVEF处理条件
实验所用HVEF装置结构如图1所示,由实验室自主研发并装配完成,主要由全温多点对板电极、丙烯酸腔体(定制丙烯酸材料)、循环冷却器、80 kV电源和电流表(3 mA)组成。参考Huang Han等[3]的方法并稍作改动,将处理好的鱼肉放在圆形水分称量盘(铝箔,半径90 mm、高8 mm)上,置于放电板正下方。

图1 HVEF实验装置示意图
Fig. 1 Schematic diagram of HVEF device
基于Qi Mengyuan等[18]的研究结果,本研究中设置电场强度为6 kV/cm,以处理0 min为对照组,使用HVEF分别对鱼肉处理5、10、15、20、25 min,在4 ℃环境中测定下列指标。
1.3.3 微观结构观察
参考高天麒等[19]的方法,垂直于肌原纤维伸展方向为横切,水平于肌原纤维伸展方向为纵切,分别取0.1 cm×0.1 cm×0.1 cm横切、纵切鮰鱼背肌进行脱水、石蜡包埋、切片并染色。用光学显微镜观察鮰鱼样品的微观结构,扫描图像的放大倍数为1 500 倍。
1.3.4 分子间作用力测定
称取2.0 g鱼肉样品,加入10 mL 0.05 mol/L NaCl溶液,6 000 r/min均质后,于4 ℃环境静置1 h,10 000×g离心15 min,向沉淀中加入10 mL 0.6 mol/L NaCl溶液,混合后再次均质处理,重复4 ℃静置1 h后,在4 ℃条件下进行二次离心(10 000×g、15 min),取上清液,使用考马斯亮蓝比色法测定其蛋白质量浓度,用以表示离子键含量。二次离心后的沉淀部分经滤膜收集,向其中分别添加10 mL混合提取液1(0.6 mol/L NaCl、1.5 mol/L尿素)、混合提取液2(0.6 mol/L NaCl、8 mol/L尿素),6 000 r/min均质后,4 ℃环境静置1 h,10 000×g离心15 min,取上清液,测定蛋白质量浓度,分别用以表示氢键、疏水相互作用含量。
1.3.5 傅里叶变换红外光谱测定
根据郭兵兵等[20]的方法,将鱼肉冻干研磨成粉进行实验。发射光谱条件:扫描范围290~440 nm,激发和发射狭缝宽度均为5 nm,电压400 V,响应时间1 s。
1.3.6 SDS-PAGE
首先从鮰鱼鱼片中提取肌原纤维蛋白(myofibrillar protein,MP)。称取适量鱼肉样品,加入10 倍体积的低盐缓冲溶液A(含50 mmol/L NaCl、20 mmol/L Tris-HCl,pH 7.0)进行均质。随后,4 ℃、9 000 r/min离心10 min,弃上清液,重复上述操作2 次。之后,将沉淀物用5 倍体积的高盐缓冲溶液B(含0.6 mol/L NaCl、20 mmol/L Tris-HCl,pH 7.0)稀释并均质,4 ℃冷藏60 min,4 ℃、10 000 r/min离心30 min,所得上清液即为MP。采用双缩脲法测定蛋白质量浓度,以牛血清白蛋白作为标准品。
参考Laemmli[21]、郭兵兵[20]等的方法,使用高盐缓冲溶液B稀释MP至质量浓度为1.5 mg/mL,然后将其与蛋白上样缓冲液按体积比2∶1混合,将其质量浓度调整为1 mg/mL,沸水浴3 min,取出后放置于室温,得到SDS-PAGE待测样品。设置电压为60 V,浓缩胶质量分数4%,分离胶质量分数10%,在溴酚蓝到达底部之前,将胶从玻璃板上取下,倒入玻璃容器内,添加染色液(体积分数10%乙酸、50%甲醇和质量分数0.1%考马斯亮蓝R-250),染色过夜,然后使用洗脱液(体积分数50%甲醇、10%乙酸和40%纯水)脱色4 h,收集图像。
1.3.7 pH值测定
用刺入式pH计探头插入经HVEF处理后的鮰鱼片中,测定其pH值。
1.3.8 剪切力测定
参考高天麒等[19]的方法,将尺寸为2.0 cm×3.0 cm×3.0 cm的鱼片置于质构仪,探头选用MORS Blade,测前速率5.0 mm/s,测中速率1.0 mm/s,测后速率5 mm/s,测试距离25 mm,触发力5 g。
1.3.9 白度测定
使用色差仪测定鮰鱼肉块的亮度值(L*)、红度值(a*)、黄度值(b*),白度按式(1)计算:
1.3.10 质构特性测定
参考Qian Chenru等[22]的方法,采用质构仪对鱼肉的质构特性进行测定。选用P/36R圆柱形探头,应变40%,测前速率2.0 mm/s,测中速率1.0 mm/s、测后速率2.0 mm/s,触发力5 g。测得样品的硬度、弹性、内聚性、咀嚼性及胶黏性。
1.3.11 水分含量测定
使用GB 5009.3—2016《食品安全国家标准 食品中水分的测定》中的直接干燥法测定鱼肉水分含量。
1.3.12 持水力测定
使用离心法进行测定,取厚度为5 mm的鱼肉,4 ℃、3 000×g离心10 min,室温下测定6 次。持水力按式(2)计算:
式中:m为空离心管质量/g;m1为离心前样品和离心管总质量/g;m2为离心后样品和离心管总质量/g。
1.3.13 水分分布测定
参照周俊鹏等[23]的方法,使用LF-NMR仪分析鱼肉样品的水分分布情况。将新鲜鮰鱼样品切成2.0 cm×2.0 cm×2.0 cm的肉块,放入LF-NMR仪中进行测定,利用核磁共振成像(magnetic resonance imaging,MRI)软件及多旋回波序列采集样品质子密度像,成像系统分析参数:重复时间1 800 ms,回波时间18.2 ms,中心频率23.319 MHz,切片间隙1.0 mm,切片数4,切片宽度0.5 mm。
所有实验至少重复3 次,结果表示为平均值±标准偏差。采用Excel 2016、SPSS Statistics 27软件进行数据处理,Origin 2021软件绘图。
如图2所示,对照组背肌横切面和纵切面的肌纤维排列紧密且规则,未观察到明显的间隙。在5、10、15 min处理组中,背肌纵切面的肌纤维结构保持紧凑有序,细胞膜完整且弹性良好,纤维间的空隙分布均匀且相较于对照组更小。横切面图像显示,15、20 min处理组的肌纤维连接紧密,细胞质分布均匀。这可能源于电穿孔效应导致的肌原纤维膜通透性适度改变,从而有利于水分子更好地分布于肌纤维间,进而使肌纤维连接紧密、细胞质分布均匀。然而,25 min处理组由于过度的电场作用导致肌原纤维膜结构遭受严重破坏,离子通道无法恢复正常,水分大量流失,造成细胞间连接变得松散,出现明显的裂隙。研究结果表明,长时间的HVEF处理会导致肌纤维分离和结构破坏,而适度的处理则有助于维持组织结构的完整性。由于肉制品的微观结构变化与其品质特性密切相关,尤其影响持水能力,因此选择适当的处理时间至关重要。综合以上分析,5、10、15、20 min的HVEF处理在保持鱼肉组织结构稳定性方面效果最佳。

图2 不同HVEF处理时间对鮰鱼片微观结构的影响
Fig. 2 Effect of different HVEF treatment times on the microstructure of channel catfish muscle
维持蛋白质复杂网络结构的化学键主要包括氢键、离子键及疏水相互作用。氢键通过稳定结合水维持蛋白质二级结构,离子键由带有相反电荷的氨基酸残基依靠库仑力维持蛋白质的三、四级结构,疏水相互作用是推动蛋白质折叠的主要作用力[24]。如图3所示,随着处理时间的延长,离子键含量整体呈降低趋势,15、20、25 min处理组离子键含量相比于对照组显著降低(P<0.05)。此外,氢键和疏水相互作用含量随处理时间的延长呈略微下降趋势,但未出现显著差异。HVEF处理对鱼肉样本中分子间作用力的影响主要体现在离子键含量的显著变化上。结果表明,HVEF处理对维系蛋白质结构的分子间作用力影响较小。
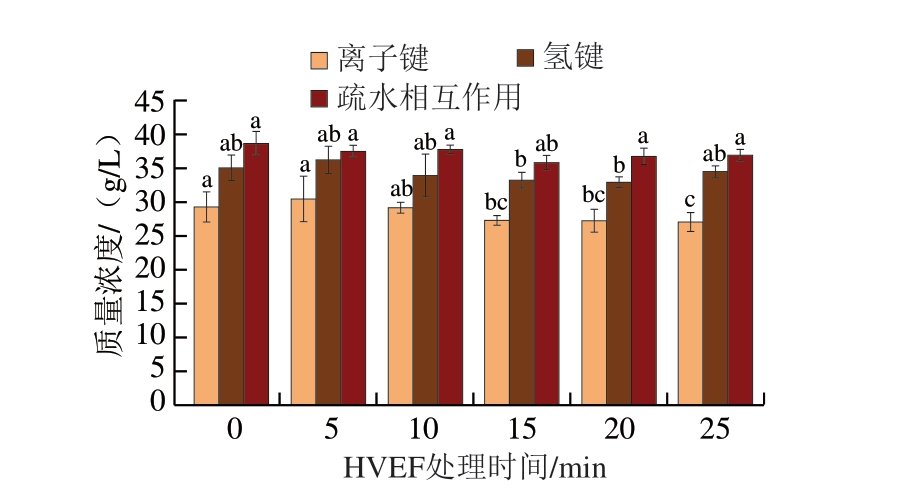
图3 不同HVEF处理时间对鮰鱼片分子间作用力的影响
Fig. 3 Effect of different HVEF treatment times on intermolecular interactions in channel catfish fillets
小写字母不同表示差异显著(P<0.05)。图7、8同。
如图4A所示,酰胺I带(1 600~1 700 cm-1)对应肽键的C=O伸缩振动,可分为4 个区域:α-螺旋(1 646~1 664 cm-1)、β-折叠(1 600~1 637 cm-1),无规卷曲(1 637~1 646 cm-1)和β-转角(1 660~1 700 cm-1)[25]。随着HVEF处理时间的延长,HVEF处理对肌肉组织特征吸收峰的强度变化造成影响,酰胺I带吸收强度的增加归因于C=O伸缩振动偶极矩的增大[26]。先前的研究[27]表明,由活性物质(特别是羟自由基和臭氧)引起的C=O伸缩振动的变化可归因于氨基酸侧链的氧化。由图4B可知,与对照组相比,各处理组的α-螺旋、β-折叠、β-转角及无规卷曲相对含量均无明显差异,但观察到α-螺旋相对含量随处理时间延长呈下降趋势,而β-折叠相对含量略有升高。通过Pearson相关性分析(图5)可知,离子键含量与α-螺旋相对含量相关系数为0.701,与β-折叠相对含量相关系数为-0.847,表明离子键的减少可能诱导α-螺旋结构向β-折叠转变。这一现象表明,HVEF可能通过削弱离子键等分子间作用力诱导部分α-螺旋结构解旋并转化为β-折叠,从而促进蛋白质分子的局部展开。值得注意的是,相较于高剂量的辐照会引起蛋白质的变性并影响产品品质[28],HVEF对蛋白质二级结构的扰动较小,更有利于维持其天然构象的稳定,这为HVEF技术在鱼肉保鲜方面的应用提供了潜在优势。
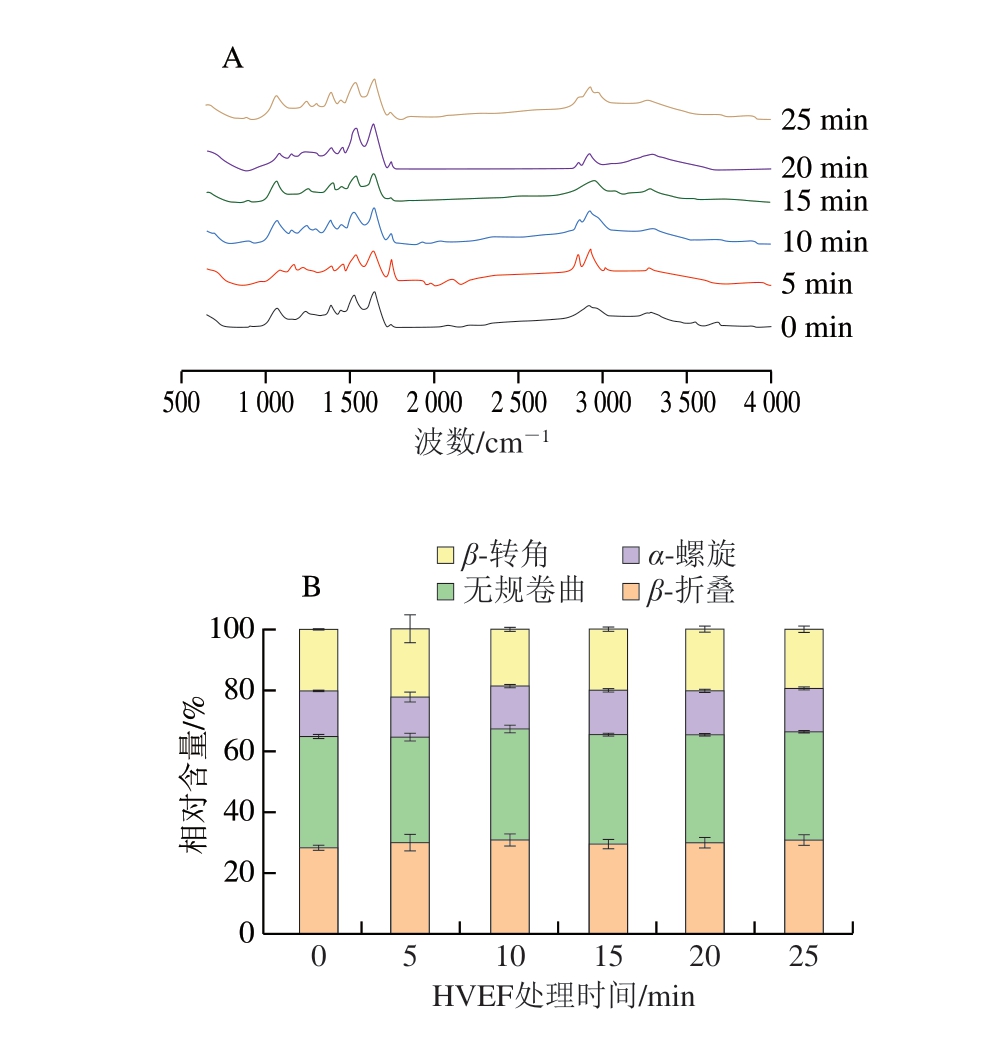
图4 不同HVEF处理时间对鮰鱼片傅里叶变换红外光谱(A)和二级结构相对含量(B)的影响
Fig. 4 Effect of different HVEF treatment times on Fourier transform infrared spectrum (A) and protein secondary structure relative content (B) of channel catfish fillets
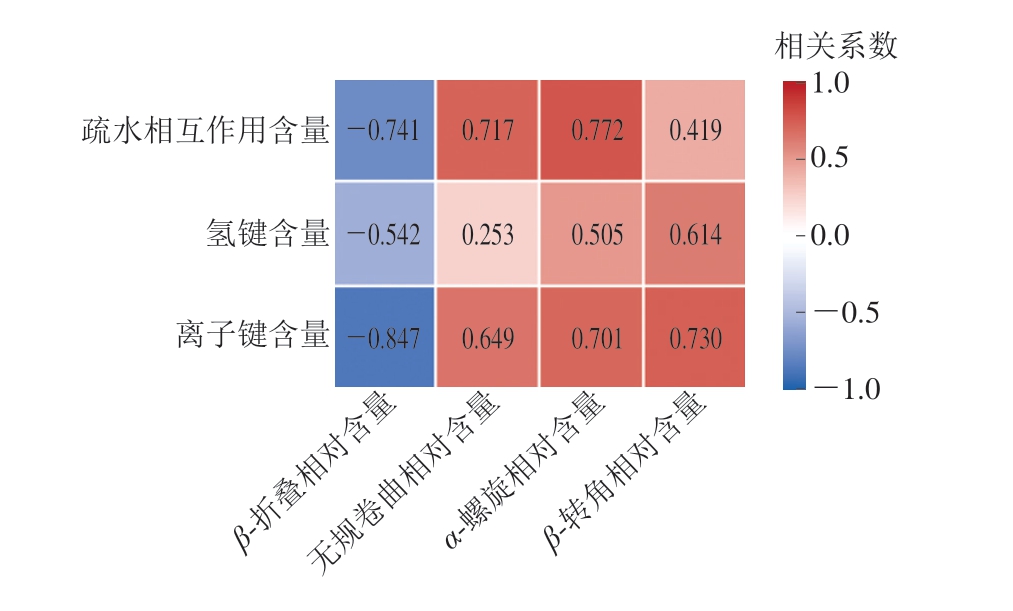
图5 鮰鱼片蛋白二级结构与分子间作用力的Pearson相关性分析
Fig. 5 Pearson correlation analysis between protein secondary structure and intermolecular interactions in channel catfish fillets
如图6所示,所有样品均表现出肌肉蛋白的特征,包括肌球蛋白重链(200 kDa)、肌动蛋白(43 kDa)、肌钙蛋白T(41 kDa)和原肌球蛋白(38 kDa)。此外,还观察到与肌球蛋白轻链(21 kDa)、肌钙蛋白I(18 kDa)和肌钙蛋白C(17 kDa)相对应的较轻条带[29]。对于还原和非还原凝胶,在对照组和经HVEF处理的样品之间没有观察到明显的条带变化,这与猪MP中等脉冲电场处理的研究结果[30]一致,表明在该条件下,HVEF处理不会改变MP分子质量或降解MP分子条带。
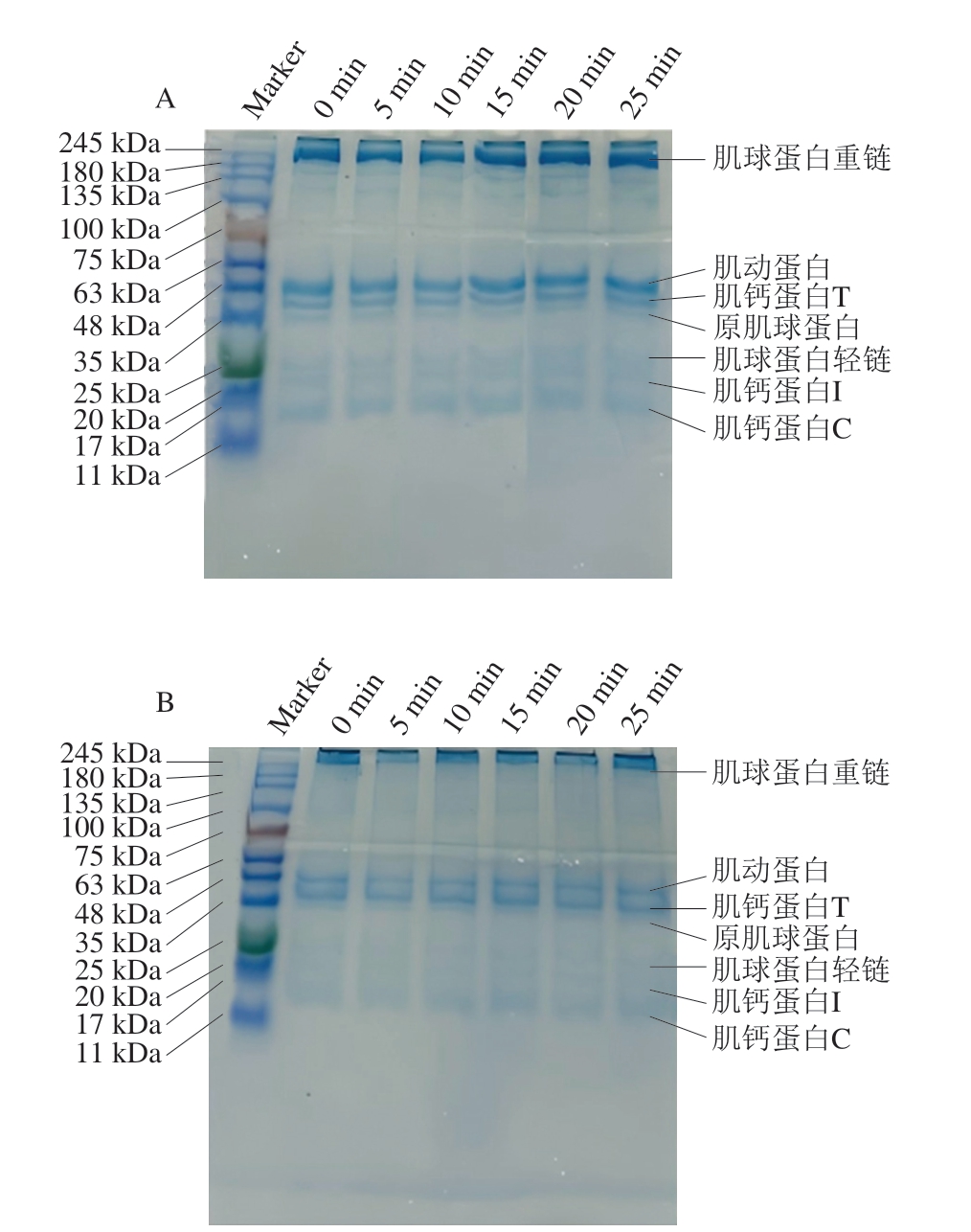
图6 不同HVEF处理时间对鮰鱼片MP SDS-PAGE图谱的影响
Fig. 6 Effects of different HVEF treatment times on sodium dodecyl sulfate-polyacrylamide gel electrophoresis patterns of myofibrillar protein in channel catfish fillets
A.溶解在含β-巯基乙醇蛋白上样缓冲液中的MP;B.溶解在不含β-巯基乙醇蛋白上样缓冲液中的MP。
在还原条件下,肌球蛋白重链条带的颜色在0~15 min处理期间略有变浅,而在15~25 min处理期间明显变深。相比之下,肌动蛋白和原肌球蛋白条带的颜色随着处理时间的延长明显变浅。肌球蛋白轻链、肌钙蛋白I和肌钙蛋白C条带的颜色随处理时间延长呈波动变浅趋势。这可能表明HVEF处理诱导蛋白质的结构修饰和聚集,导致不同类型蛋白质含量的变化。Ng等[31]研究发现,在还原条件下,随着火花放电处理时间的延长,酪蛋白条带的颜色略有变浅,而β-乳球蛋白条带的颜色略有加深。这种现象归因于通过二硫键形成、疏水和静电相互作用以及蛋白质间交联形成高分子质量聚集体。在本研究中,HVEF能量输入不足以改变MP的一级结构。然而,它足以通过影响分子内交联诱导构象变化。
pH值是反映鱼肉新鲜度的指标之一。如图7A所示,HVEF处理时间对鱼肉的pH值有显著影响(P<0.05),与对照组相比,10 min处理组pH值略有升高,而15、20 min处理组pH值显著降低(P<0.05)。这可能是由于HVEF处理诱导鱼肉中的脂质氧化,生成酸性物质,这些物质进一步降低鱼肉的pH值[32]。
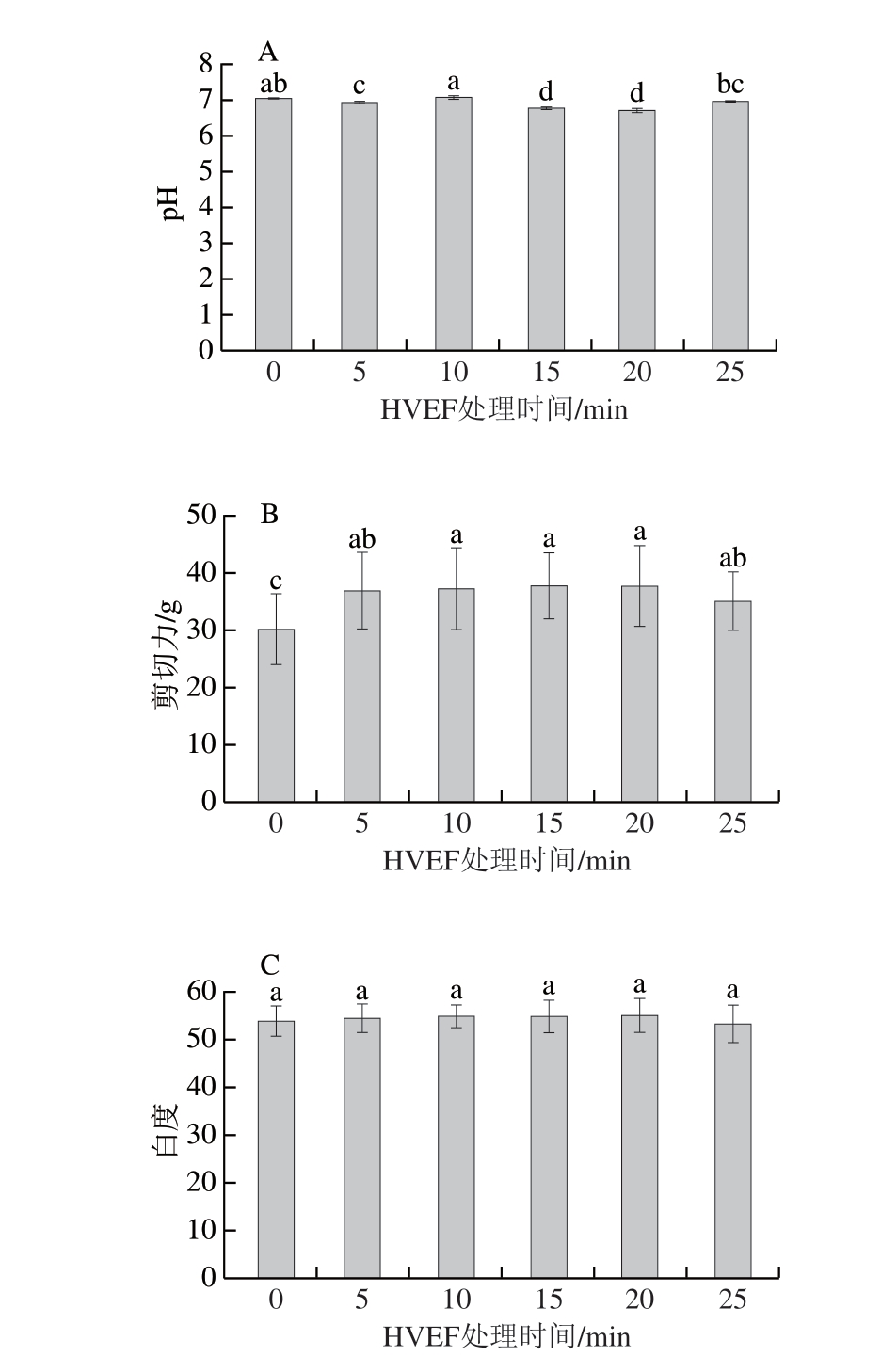
图7 不同HVEF处理时间对鮰鱼片pH值(A)、剪切力(B)和白度(C)的影响
Fig. 7 Effects of different HVEF treatment times on pH (A), shear force (B), and whiteness (C) of channel catfish fillets
剪切力是判断鱼肉品质的重要指标之一,通常用于评估食品的质地和嫩度[19]。如图7B所示,随着HVEF处理时间的延长,鮰鱼片的剪切力呈上升趋势。对照组的剪切力为(30.13±6.26)g,各处理组均显著高于对照组(P<0.05)。结果表明,HVEF处理会改变鱼肉的嫩度。
鱼肉的色泽能够直观反映其新鲜程度,是反映鱼肉产品品质的重要指标[33]。如图7C所示,与对照组(53.8)相比,各HVEF处理组的白度均无显著变化。随着HVEF处理时间延长,鮰鱼片的白度呈上升趋势,处理20 min时达最高值(54.91)。这可能是由于HVEF处理会改变鱼肉中水分的状态,使其更均匀地分布在组织中,减少水分对光的散射,从而提高白度[34]。研究结果表明,HVEF处理对鱼肉白度无显著影响。与之相比,超高压处理可能会导致鱼肉的色泽变暗。尚校兰等[35]研究发现,超高压处理会使海鲈鱼的肌节长度增加、肌纤维间空隙增大,导致鱼肉的持水力降低、色泽变暗。
鱼肉的硬度、胶黏性、弹性和咀嚼性等指标能在一定程度上反映其品质,可以作为评价鱼肉品质的依据[36]。如表1所示,经HVEF处理的鮰鱼片硬度、胶黏性、内聚力、弹性、咀嚼性与对照组均无显著差异。鱼肉硬度在处理10 min时达最大值(2 028.75 g),表明此时样品结构最为紧密,随处理时间进一步延长,硬度略有降低,但在处理25 min时略有回升。鱼肉胶黏性在处理5 min时达最大值(25.5)。随着处理时间延长,样品弹性均低于对照组(0.80),胶黏性、内聚力、咀嚼性变化无明显规律,表明样品内部结构稳定。结果表明,HVEF处理不会对鮰鱼品质造成负面影响。这与微冻保鲜技术相比具有明显优势,微冻保鲜虽然能在短期内较好地保持水产品品质,但容易受温度波动的影响,长时间的微冻贮藏还会形成重结晶,破坏水产品内部结构,引起汁液流失,影响其质构特性和持水力[37]。
表1 不同HVEF处理时间对鮰鱼片质构特性的影响
Table 1 Effects of different HVEF treatment times on textural properties of channel catfish fillets
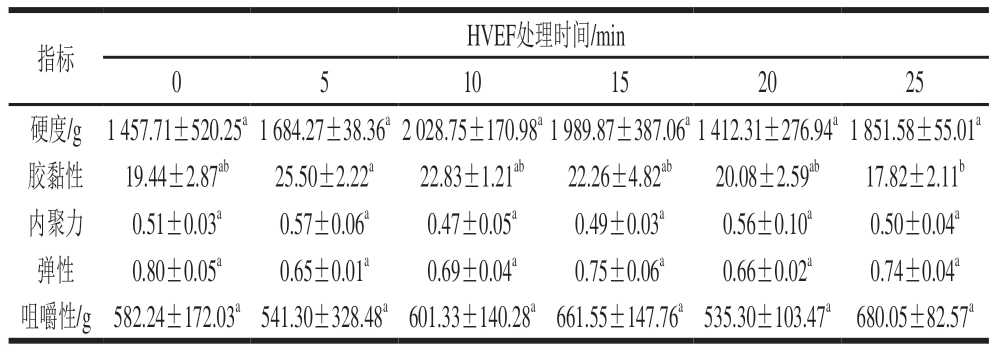
注:同行小写字母不同表示差异显著(P<0.05)。表2同。
指标HVEF处理时间/min 0 5 10152025硬度/g1 457.71±520.25a1 684.27±38.36a2 028.75±170.98a1 989.87±387.06a1 412.31±276.94a1 851.58±55.01a胶黏性19.44±2.87ab25.50±2.22a22.83±1.21ab22.26±4.82ab20.08±2.59ab17.82±2.11b内聚力0.51±0.03a0.57±0.06a0.47±0.05a0.49±0.03a0.56±0.10a0.50±0.04a弹性0.80±0.05a0.65±0.01a0.69±0.04a0.75±0.06a0.66±0.02a0.74±0.04a咀嚼性/g582.24±172.03a541.30±328.48a601.33±140.28a661.55±147.76a535.30±103.47a680.05±82.57a
持水力作为评估鱼类肌肉组织完整性的重要指标,可以反映肌间蛋白截留不易流动水、自由水和抑制水分流失的能力[38]。如图8A所示,与对照组(64.72%)相比,各HVEF处理组鮰鱼片持水力均有所上升。25 min处理组持水力上升至68.80%,显著高于对照组(P<0.05)。Amiri等[13]同样发现,HVEF处理可使牛肉MP的持水能力提高,并解释为电场诱导的电荷重新分布增强了蛋白质与水分子的结合能力。结果表明,HVEF处理能有效抑制鮰鱼的水分流失。
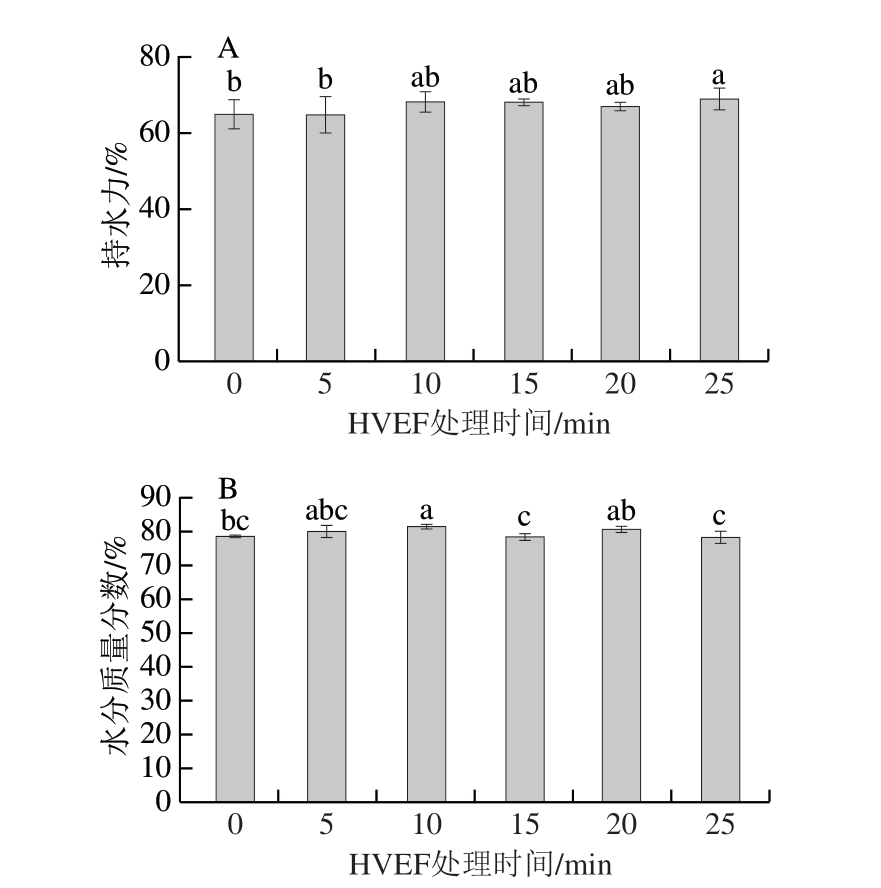
图8 不同HVEF处理时间对鮰鱼片持水力(A)和水分含量(B)的影响
Fig. 8 Effects of different HVEF treatment times on water-holding capacity (A) and moisture content (B) of channel catfish fillets
水分含量同样是衡量鱼肉品质的重要指标。如图8B所示,对照组鮰鱼片水分质量分数为78.64%,随着HVEF处理时间的延长,各处理组水分质量分数分别为80.06%、81.68%、78.45%、80.84%和78.34%。25 min处理组水分含量有所降低,可能是HVEF处理导致鱼肉组织结构发生变化。已有研究[39]表明,长时间的HVEF处理会影响鱼肉的品质,该结果与微观结构观察结果(图2)一致。
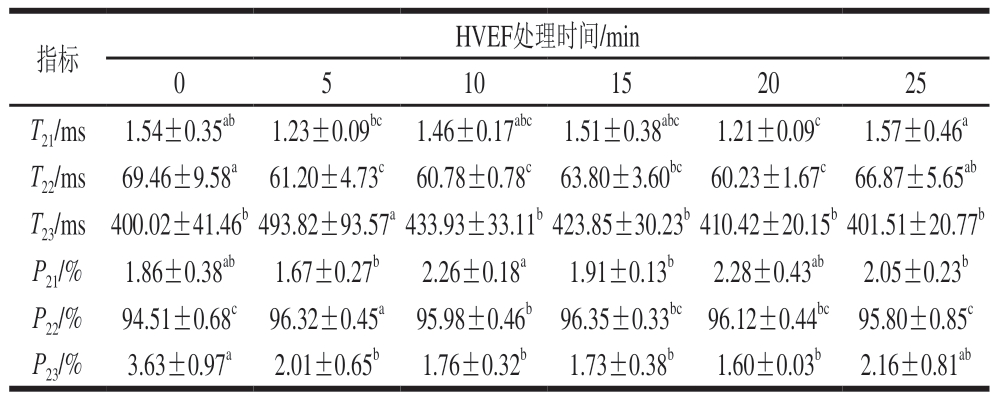
LF-NMR技术中多以氢核(1H)为研究对象,1H以非辐射的方式从高能态转变为低能态的过程称为弛豫[40]。在肉和肉制品中,横向弛豫时间(T2)是一个关键参数,用于分析样品中水分的状态和自由度。T2反映了水分子与周围环境(如蛋白质、脂肪等)的相互作用程度[41]。因此,依据样品中水分子的T2,可以对肉与肉制品中水分的不同状态进行区分[42]。如图9所示,3 个峰对应3 种形态的水分:T21(0~10 ms)代表与大分子紧密结合的结合水;T22(10~100 ms)代表不易流动水,位于肌原纤维网络中;T23(>100 ms)代表容易流失的自由水,主要存在于肌原纤维束之间[43]。如图9和表2所示,随着HVEF处理时间的延长,T21发生小范围波动,这可能由鮰鱼的个体差异引起。相较于对照组,经HVEF处理后,T22缩短,T23有所延长,表明HVEF能够有效调控鱼肉内部水分子状态,延缓水分迁移过程,增强结合水稳定性和鱼肉对自由水的束缚能力。这与2.1节研究结果一致,适当的HVEF处理时间(5~20 min)内,膜通透性的适度改变有利于水分子更好地分布于肌纤维间。其中,T22的缩短与HVEF处理对鱼肉持水力的增强(图8)相关,持水力的增强减少了鱼肉中的水分损失。由表2可知,P22超过90%,说明鱼肉中大部分水分主要是以不易流动水的形式存在[44]。HVEF处理使鱼肉样品T23延长,P21增加,P23降低,表明HVEF处理会促进鱼肉中的蛋白质与水结合,阻碍结合水向自由水转移。且HVEF处理20 min能够更有效地减少鱼肉中的水分损失,使其具有更好的商业价值。
表2 不同HVEF处理时间对鮰鱼片不同状态水分T2及相对含量(P2)的影响
Table 2 Effects of different HVEF treatment times on transverse relaxation time (T2) and relative contents (P2) of different types of water in channel catfish fillets treated with HVEF for different times
指标HVEF处理时间/min 0 5 10152025 T21/ms1.54±0.35ab1.23±0.09bc1.46±0.17abc1.51±0.38abc1.21±0.09c1.57±0.46a T22/ms69.46±9.58a61.20±4.73c60.78±0.78c63.80±3.60bc60.23±1.67c66.87±5.65ab T23/ms400.02±41.46b493.82±93.57a433.93±33.11b423.85±30.23b410.42±20.15b401.51±20.77b P21/%1.86±0.38ab1.67±0.27b2.26±0.18a1.91±0.13b2.28±0.43ab2.05±0.23b P22/%94.51±0.68c96.32±0.45a95.98±0.46b96.35±0.33bc96.12±0.44bc95.80±0.85c P23/%3.63±0.97a2.01±0.65b1.76±0.32b1.73±0.38b1.60±0.03b2.16±0.81ab
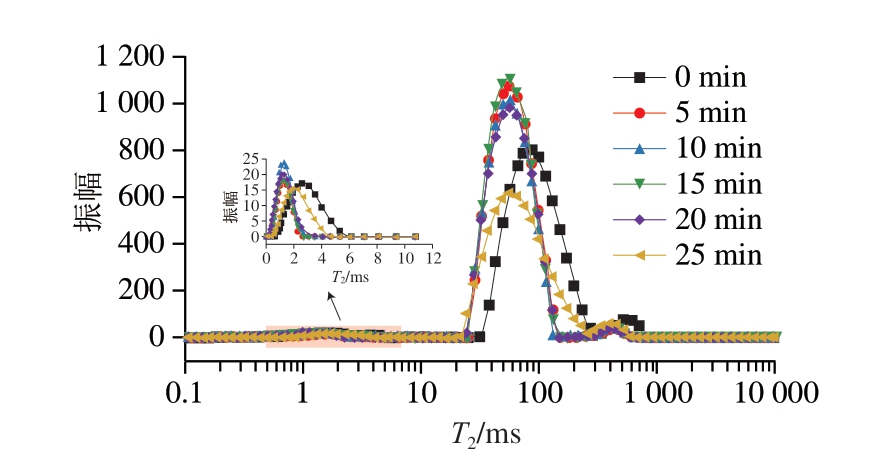
图9 不同HVEF处理时间对鮰鱼片水分分布的影响
Fig. 9 Effects of different HVEF treatment times on water distribution of channel catfish fillets
通过MRI技术获得的高分辨率图像能直观反映水分的分布。若信号强则显红色,无信号则显蓝色,同时其质子密度越大,图像中亮度越强,样品中水分含量越高[45]。如图10所示,所有鮰鱼样品均呈黄、红色,表明各组样品水分含量均处于较高水平。对照组样品颜色分布均匀,25 min处理组鱼肉的颜色分布相较于对照组变得不均匀,水分含量也有所降低,15、20 min处理组则表现出均匀且大量的黄、红色。这种现象与长时间HVEF处理导致肌纤维分离和结构破坏密切相关,进一步印证了适度的HVEF处理能够通过改变肌原纤维膜通透性优化水分分布,维持鱼肉的品质。结果表明,HVEF处理能够有效抑制鮰鱼片水分含量的下降,且在处理20 min时效果最佳。
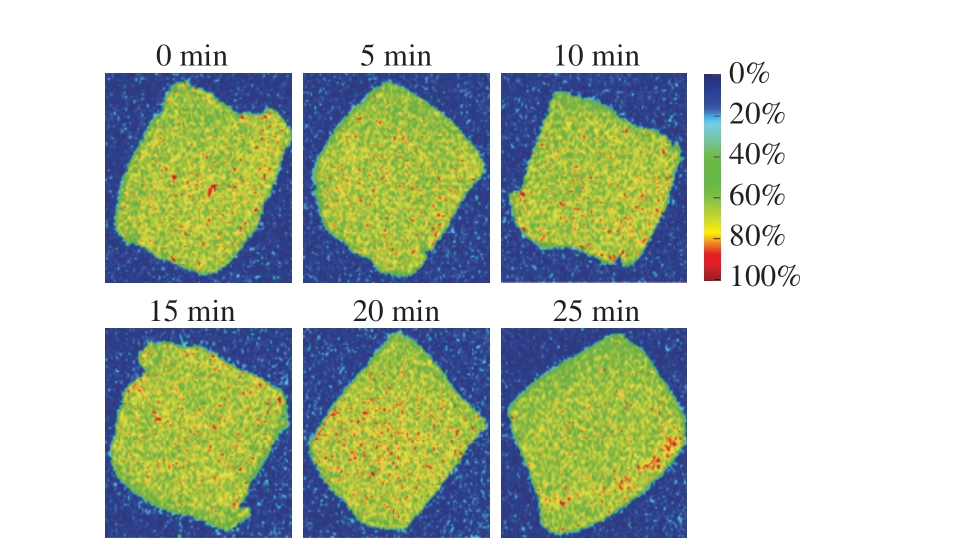
图10 不同HVEF处理时间鮰鱼片的MRI
Fig. 10 Magnetic resonance images of channel catfish fillets treated with HVEF for different times
本研究探讨了HVEF处理时间对鮰鱼片肌肉品质和水分分布的影响。研究结果表明,适度HVEF处理保鲜可有效维持肌肉组织结构完整性,抑制水分流失,并提升鱼肉嫩度,而过度处理则因肌原纤维收缩导致组织结构劣变。综合考虑,电场强度6 kV/cm、处理时间20 min为最优HVEF处理参数。
[1] 高天麒, 汪超, 汪兰, 等. 冷藏鮰鱼中腐败菌的分离鉴定及腐败能力测定[J]. 肉类研究, 2023, 37(3): 1-6. DOI:10.7506/rlyj1001-8123-20230110-005.
[2] 农业农村部渔业渔政管理司. 2023中国渔业统计年鉴[M]. 北京: 中国农业出版社, 2023.
[3] HUANG H, SUN W Q, XIONG G Q, et al. Effects of HVEF treatment on microbial communities and physicochemical properties of catfish fillets during chilled storage[J]. LWT-Food Science and Technology,2020, 131: 109667. DOI:10.1016/j.lwt.2020.109667.
[4] 姜启兴, 聂程芳, 高沛, 等. 斑点叉尾鮰鱼软罐头杀菌工艺研究[J].食品与生物技术学报, 2021, 40(3): 97-102. DOI:10.3969/j.issn.1673-1689.2021.03.012.
[5] 周明珠, 熊光权, 乔宇, 等. 不同干燥方式下鮰鱼片的干燥特性及风味变化[J]. 现代食品科技, 2021, 37(4): 242-251. DOI:10.13982/j.mfst.1673-9078.2021.4.0905.
[6] HATAB S, KODDY J K, MIAO W H, et al. Atmospheric cold plasma:a new approach to modify protein and lipid properties of myofibrillar protein isolate from hairtail (Trichiurus lepturus) fish[J]. Journal of the Science of Food and Agriculture, 2022, 102(5): 2041-2049.DOI:10.1002/jsfa.11543.
[7] 杨汝晴, 陈玉磊, 孙乐常, 等. 鲈鱼在4 ℃冷藏过程中的肌肉品质变化[J]. 食品科学, 2023, 44(1): 239-245. DOI:10.7506/spkx1002-6630-20211210-126.
[8] GITERU S G, OEY I, ALI M A. Feasibility of using pulsed electric fields to modify biomacromolecules: a review[J]. Trends in Food Science &Technology, 2018, 72: 91-113. DOI:10.1016/j.tifs.2017.12.009.
[9] 马宇乔, 陈小娥, 方旭波, 等. 高压静电场处理对鳀鱼发酵液品质的影响[J]. 食品科学, 2024, 45(19): 182-191. DOI:10.7506/spkx1002-6630-20240109-089.
[10] HUANG J, QUE F, XIONG G Q, et al. Physicochemical and functional properties changes in myofibrillar protein extracted from channel catfish by a high-voltage electrostatic field[J]. Food and Bioprocess Technology, 2023, 16(2): 395-403. DOI:10.1007/s11947-022-02937-7.
[11] CIAMPA A, PICONE G, LAGHI L, et al. Changes in the amino acid composition of Bogue (Boops boops) fish during storage at different temperatures by 1H-NMR spectroscopy[J]. Nutrients, 2012, 4(6): 542-553. DOI:10.3390/nu4060542.
[12] 杨娇, 于洪剑, 白爱枝, 等. 高压电场干燥和热风干燥对马铃薯蛋白质二级结构的影响[J]. 保鲜与加工, 2020, 20(3): 85-89.DOI:10.3969/j.issn.1009-6221.2020.03.013.
[13] AMIRI A, MOUSAKHANI-GANJEH A, SHAFIEKHANI S, et al.Effect of high voltage electrostatic field thawing on the functional and physicochemical properties of myofibrillar proteins[J]. Innovative Food Science & Emerging Technologies, 2019, 56: 102191. DOI:10.1016/j.ifset.2019.102191.
[14] QI M Y, YAN H Y, ZHANG Y, et al. Impact of high voltage prick electrostatic field (HVPEF) processing on the quality of ready-to-eat fresh salmon (Salmo salar) fillets during storage[J]. Food Control,2022, 137: 108918. DOI:10.1016/j.foodcont.2022.108918.
[15] KO W C, YANG S Y, CHANG C K, et al. Effects of adjustable parallel high voltage electrostatic field on the freshness of tilapia (Orechromis niloticus) during refrigeration[J]. LWT-Food Science and Technology,2016, 66: 151-157. DOI:10.1016/j.lwt.2015.10.019.
[16] 杜金, 韦锦梅, 王丽, 等. 高压静电场协同臭氧解冻对冷鲜猪肉品质特性的影响[J]. 肉类研究, 2024, 38(4): 43-50. DOI:10.7506/rlyj1001-8123-20240324-065.
[17] LIU J, ZHU F X, YANG J, et al. Effects of high-voltage electrostatic field (HVEF) on frozen shrimp (Solenocera melantho) based on UPLC-MS untargeted metabolism[J]. Food Chemistry, 2023, 411:135499. DOI:10.1016/j.foodchem.2023.135499.
[18] QI M Y, ZHAO R Q, LIU Q Y, et al. Antibacterial activity and mechanism of high voltage electrostatic field (HVEF) against Staphylococcus aureus in medium plates and food systems[J]. Food Control, 2021, 120: 107566. DOI:10.1016/j.foodcont.2020.107566.
[19] 高天麒, 夏雨婷, 吴伟伦, 等. 高压静电场联合食盐腌制对鮰鱼冷藏品质的影响[J]. 包装工程, 2023, 44(7): 138-148. DOI:10.19554/j.cnki.1001-3563.2023.07.016.
[20] 郭兵兵, 胡澳, 阙凤, 等. 添加不同分子量酶解魔芋葡甘聚糖的冻藏肌原纤维蛋白氧化和结构特性变化[J]. 现代食品科技, 2024, 40(6):158-168. DOI:10.13982/j.mfst.1673-9078.2024.6.0659.
[21] LAEMMLI U K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4[J]. Nature, 1970, 227: 680-685.DOI:10.1038/227680a0.
[22] QIAN C R, PAN H J, SHAO H T, et al. Effects of HVEF treatment on the physicochemical properties and bacterial communities of Larimichthys crocea fillets during refrigerated storage[J]. International Journal of Food Science & Technology, 2022, 57(12): 7691-7700.DOI:10.1111/ijfs.16115.
[23] 周俊鹏, 朱萌, 章蔚, 等. 不同冷冻方式对淡水鱼品质的影响[J].食品科学, 2019, 40(17): 247-254. DOI:10.7506/spkx1002-6630-20180913-137.
[24] 龙康源, 张思瑾, 尹涛, 等. 多糖疏水性对鱼糜凝胶特性的影响[J].肉类研究, 2024, 38(7): 15-21. DOI:10.7506/rlyj1001-8123-20240417-086.
[25] WEI P Y, ZHU K X, CAO J, et al. The inhibition mechanism of the texture deterioration of tilapia fillets during partial freezing after treatment with polyphenols[J]. Food Chemistry, 2021, 335: 127647.DOI:10.1016/j.foodchem.2020.127647.
[26] ZOJAJI I, ESFANDIARIAN A, TAHERI-SHAKIB J. Toward molecular characterization of asphaltene from different origins under different conditions by means of FT-IR spectroscopy[J]. Advances in Colloid and Interface Science, 2021, 289: 102314. DOI:10.1016/j.cis.2020.102314.
[27] MAHDAVIAN MEHR H, KOOCHEKI A. Effect of atmospheric cold plasma on structure, interfacial and emulsifying properties of Grass pea (Lathyrus sativus L.) protein isolate[J]. Food Hydrocolloids, 2020,106: 105899. DOI:10.1016/j.foodhyd.2020.105899.
[28] 张晗, 高星, 宣仕芬, 等. 电子束辐照对鲈鱼肉肌原纤维蛋白生化特性及其构象的影响[J]. 食品科学, 2019, 40(13): 81-86. DOI:10.7506/spkx1002-6630-20180518-265.
[29] EKEZIE F C, CHENG J H, SUN D W. Effects of atmospheric pressure plasma jet on the conformation and physicochemical properties of myofibrillar proteins from king prawn (Litopenaeus vannamei)[J]. Food Chemistry, 2019, 276: 147-156. DOI:10.1016/j.foodchem.2018.09.113.
[30] WANG Q L, WEI R R, HU J, et al. Moderate pulsed electric fieldinduced structural unfolding ameliorated the gelling properties of porcine muscle myofibrillar protein[J]. Innovative Food Science &Emerging Technologies, 2022, 81: 103145. DOI:10.1016/j.ifset.2022.103145.
[31] NG S W, LU P, RULIKOWSKA A, et al. The effect of atmospheric cold plasma treatment on the antigenic properties of bovine milk casein and whey proteins[J]. Food Chemistry, 2021, 342: 128283.DOI:10.1016/j.foodchem.2020.128283.
[32] 黄琪, 王世哲, 胡传峰, 等. 苯乳酸处理对鮰鱼低温贮藏品质的影响[J]. 肉类研究, 2023, 37(11): 35-41. DOI:10.7506/rlyj1001-8123-20231122-104.
[33] 李亚俐, 王雪莉, 石柳, 等. 壳聚糖-绿原酸复合保鲜剂对冷藏鮰鱼片食用品质的影响[J]. 肉类研究, 2025, 39(1): 42-50. DOI:10.7506/rlyj1001-8123-20240909-237.
[34] XU Y Q, ZHANG D Q, XIE F F, et al. Changes in water holding capacity of chilled fresh pork in controlled freezing-point storage assisted by different modes of electrostatic field action[J]. Meat Science, 2023, 204: 109269. DOI:10.1016/j.meatsci.2023.109269.
[35] 尚校兰, 刘安军. 超高压处理与添加复合磷酸盐对海鲈鱼保水性的比较[J]. 食品科学, 2013, 34(6): 56-59. DOI:10.7506/spkx1002-6630-201306012.
[36] 陈方雪, 周明珠, 邓祎, 等. 电子束辐照处理对鮰鱼冷藏期间品质的影响[J]. 肉类研究, 2021, 35(6): 57-62. DOI:10.7506/rlyj1001-8123-20210401-090.
[37] 梁释介, 孙晓悦, 李晴, 等. 预冻后冻藏温度对金鲳鱼品质的影响[J].肉类研究, 2023, 37(11): 28-34. DOI:10.7506/rlyj1001-8123-20231213-109.
[38] 邹灿敏, 刘梦遥, 钟榕斌, 等. 不同包装方式对清蒸大黄鱼贮藏过程中品质及菌群的影响[J]. 肉类研究, 2024, 38(7): 38-47.DOI:10.7506/rlyj1001-8123-20240522-123.
[39] LI D P, JIA S L, ZHANG L T, et al. Effect of using a high voltage electrostatic field on microbial communities, degradation of adenosine triphosphate, and water loss when thawing lightly-salted, frozen common carp (Cyprinus carpio)[J]. Journal of Food Engineering,2017, 212: 226-233. DOI:10.1016/j.jfoodeng.2017.06.003.
[40] CAMPELO S N, HUANG P H, BUIE C R, et al. Recent advancements in electroporation technologies: from bench to clinic[J]. Annual Review of Biomedical Engineering, 2023, 25: 77-100. DOI:10.1146/annurev-bioeng-110220-023800.
[41] PEARCE K L, ROSENVOLD K, ANDERSEN H J, et al. Water distribution and mobility in meat during the conversion of muscle to meat and ageing and the impacts on fresh meat quality attributes:a review[J]. Meat Science, 2011, 89(2): 111-124. DOI:10.1016/j.meatsci.2011.04.007.
[42] 王春晓, 周凯, 张健, 等. 松乳菇对低脂乳化肠质构品质的影响[J].肉类研究, 2022, 36(5): 42-48. DOI:10.7506/rlyj1001-8123-20220214-008.
[43] LI X X, FAN M C, HUANG Q L, et al. Effect of micro- and nanostarch on the gel properties, microstructure and water mobility of myofibrillar protein from grass carp[J]. Food Chemistry, 2022, 366:130579. DOI:10.1016/j.foodchem.2021.130579.
[44] 王睿, 王琦, 周敏, 等. 茶多酚和EGCG对风干金鲳鱼品质相关理化指标的改善效果比较[J]. 食品科学, 2023, 44(2): 54-63.DOI:10.7506/spkx1002-6630-20220224-207.
[45] 蓝蔚青, 张炳杰, 周大鹏, 等. 超声联合微酸性电解水处理对真空包装海鲈鱼冷藏期间品质变化的影响[J]. 食品科学, 2022, 43(5): 62-68. DOI:10.7506/spkx1002-6630-20210118-198.