表1 不同蛋白酶的最适水解条件
Table 1 Optimal hydrolysis conditions for different proteases
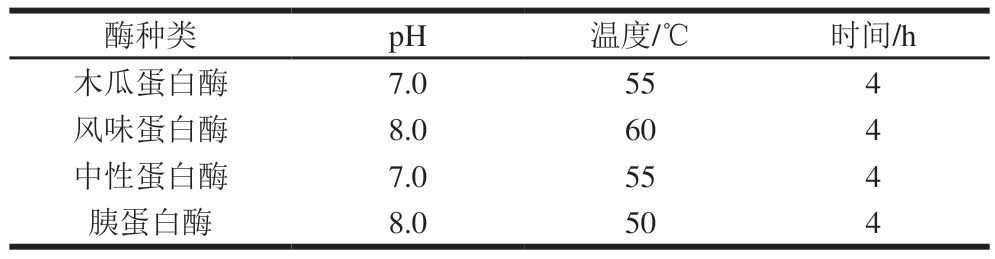
酶种类pH温度/℃时间/h木瓜蛋白酶7.0554风味蛋白酶8.0604中性蛋白酶7.0554胰蛋白酶8.0504
Preparation and Structural Characterization of Lüeyang Black-Bone Chicken Peptide-Calcium Chelate
陈黎维, 陈锐, 李海成, 等. 略阳乌鸡肽-钙螯合物制备与结构表征[J]. 肉类研究, 2026, 40(5): 19-26.DOI:10.7506/rlyj1001-8123-20250617-188. http://www.rlyj.net.cn
CHEN Liwei, CHEN Rui, LI Haicheng, et al. Preparation and structural characterization of Lüeyang black-bone chicken peptide-calcium chelate[J]. Meat Research, 2026, 40(5): 19-26. (in Chinese with English abstract) DOI:10.7506/rlyj1001-8123-20250617-188. http://www.rlyj.net.cn
钙是人体必需的矿物元素,在维持生理稳态和健康调控中发挥重要作用[1]。钙摄入不足可导致儿童发育迟缓和老年人骨质疏松等疾病[2]。当前主流钙补充剂(碳酸钙、葡萄糖酸钙等)虽可改善钙缺乏状况,但仍存在胃肠刺激和吸收阈值限制问题[3]。相比之下,肽-钙螯合物具有生物利用度高、溶解性好、胃肠道刺激小等优势[4-6]。例如,糖基化核桃肽-钙螯合物可通过激活瞬时受体电位香草酸亚型6/电压门控钙通道1.3提高Caco-2细胞的钙吸收效率[7];脱盐鸭蛋清肽-钙可促进肠上皮细胞的钙吸收能力,从而降低骨质疏松风险[8]。由此可见,肽-钙螯合物凭借其优越的理化性质和良好的生理功能,可能成为开发高效钙补充制品的理想选择。目前,研究者已在动植物中鉴定出多种具有钙结合能力的肽,如鸡血红蛋白肽-钙螯合物[9]、罗非鱼鳞钙结合肽[10]和薏米肽螯合钙[11]等。钙螯合肽的构效关系与多肽分子质量、氨基酸组成及钙结合特性密切相关[12-14]。
略阳乌鸡作为秦岭山地特色禽种,具有肉质细嫩、营养丰富等特点,其品种特性的形成源于独特的地理气候条件与半集约化养殖模式的协同作用[15]。与普通肉鸡肽相比,乌鸡肽生物活性较强[16],且具有改善贫血、抗氧化、抗疲劳、免疫调节等重要的生理功能[17]。鸡肉蛋白资源虽具有较高经济价值,但当前仍以粗加工为主,高附加值产品开发不足,导致资源浪费;另外,针对地方特色鸡种的基础研究较少,制约了特色资源的开发利用。
酶水解法因其反应条件温和、高效且安全性高而被广泛应用,常用水解酶包括木瓜蛋白酶、风味蛋白酶等[1]。Liu Xiaochen等[18]研究表明,木瓜蛋白酶和风味蛋白酶复合水解鸡肉蛋白后,通过乙醇逐级分离酶解产物,可将肽螯合能力提高至(68.6±0.6)mg/g。陈树泓[19]以木瓜蛋白酶酶解崇仁麻鸡鸡肉蛋白得到的崇仁麻鸡肽-钙螯合能力为76.95 mg/g。木瓜蛋白酶可将鸡肉蛋白内部的精氨酸解离至肽链末端,为Ca2+提供充足的螯合位点[20-21]。风味蛋白酶作为外肽酶和内肽酶的混合物,能通过剪切疏水性氨基酸提高肽的螯合能力[22]。
本研究以略阳乌鸡为原料,通过酶法制备略阳乌鸡肽(black-bone chicken peptide,BCP)。采用单因素试验考察肽-钙质量比、螯合时间、pH值、温度对肽-钙螯合能力的影响,并运用响应面法优化BCP-钙螯合物(BCP-Ca)的制备工艺。在此基础上,对螯合物进行结构表征,以期为略阳乌鸡的综合运用提供理论支撑。
略阳乌鸡(6 月龄,平均体质量约2.0 kg) 陕西同辉农业发展有限公司;木瓜蛋白酶、风味蛋白酶、中性蛋白酶、胰蛋白酶 合肥千盛生物科技有限公司;CaCl2、乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)、钙红指示剂(均为分析纯) 天津基准化学试剂有限公司。
DF-101S型恒温磁力搅拌器 上海力辰邦西仪器科技有限公司;FA3204B型电子分析天平 上饶鸿翔实业有限公司;LGJ-40E型真空冷冻干燥机 北京四环科学仪器厂有限公司;X-30R型台式高速离心机 贝克曼库尔特商贸有限公司;D&Advance型X射线衍射仪、Vertex70型傅里叶变换红外光谱仪 德国Bruker公司;EVOLUTION 201型紫外-可见分光光度计 赛默飞世尔(中国)科技公司;F-4500型荧光分光光度计 日本Hitachi公司;Sigma 360型扫描电子显微镜 德国Zeiss公司。
1.3.1 略阳乌鸡预处理
参考陈树泓[19]的方法并稍作修改。取略阳乌鸡胸肉和腿肉,用去离子水清洗,绞碎匀浆,加入适量水煮沸约30 min,均质后冷却、离心(4 500 r/min、15 min),保留下层液料,冷冻干燥后备用。
1.3.2 最适蛋白酶筛选
参考魏新颜等[21]的方法并根据实际情况对酶解条件进行适当调整。单酶(木瓜蛋白酶、风味蛋白酶、中性蛋白酶、胰蛋白酶)酶解体系(总加酶量6 000 U/g):底物质量浓度3 g/100 mL,调节温度及pH值至目标蛋白酶最适条件(表1),酶解时间4 h。双酶复合体系(总加酶量6 000 U/g,双酶比例1∶1)分为2 类:1)同步酶解:双酶共同酶解4 h;2)分步酶解:木瓜蛋白酶酶解4 h,灭酶后调节体系pH值至8.0,加入风味蛋白酶,60 ℃酶解4 h。所有样品置于沸水中灭酶15 min、冷却、离心(4 500 r/min、15 min),将上清液冷冻干燥即得BCP粉末,以水解度与钙螯合能力为指标筛选最适蛋白酶。
表1 不同蛋白酶的最适水解条件
Table 1 Optimal hydrolysis conditions for different proteases

酶种类pH温度/℃时间/h木瓜蛋白酶7.0554风味蛋白酶8.0604中性蛋白酶7.0554胰蛋白酶8.0504
1.3.3 螯合物制备
参考Hu Guanhua等[23]的方法并作适当修改。准确称取BCP溶于去离子水,配制成质量浓度为3 g/100 mL的溶液,调节体系温度至55 ℃并维持pH 7.0,按肽-钙质量比1∶1加入CaCl2混匀,螯合反应1 h后加入5 倍体积的无水乙醇,沉淀3 h后离心(4 500 r/min、20 min),收集沉淀并冷冻干燥,得到BCP-Ca粉末。
1.3.4 水解度测定
采用中性甲醛滴定法[24]测定水解产物中游离氨基氮含量,参照GB 5009.5—2025《食品安全国家标准 食品中蛋白质的测定》[25]测定样品总氮含量。水解度按下式计算:
1.3.5 钙螯合能力测定
参照GB 5009.5—2025[25]凯氏定氮法测定酶解产物的蛋白质含量/(g/kg),再采用GB 5009.92—2016《食品安全国家标准 食品中钙的测定》[26] EDTA滴定法测定螯合物中的Ca2+含量/(mg/kg),以Ca2+含量与蛋白质含量比值表征钙螯合能力,结果以每克蛋白质螯合钙的毫克数(mg/g)表示[20]。
1.3.6 单因素试验
以CaCl2为钙源,通过单因素试验优化BCP-Ca制备工艺。具体操作:向3 g/100 mL BCP溶液中加入CaCl2,使肽-钙质量比达到1∶2、1∶1、2∶1、4∶1、6∶1,调整pH值至5.0、6.0、7.0、8.0、9.0,在30、40、50、60、70 ℃下反应30、40、50、60、70 min,使BCP与Ca2+发生螯合反应。其余条件同1.3.3节。
1.3.7 响应面优化试验
在单因素试验基础上,依据Design-Expert 13软件中的Box-Behnken设计原理,选取肽-钙质量比(A)、螯合pH值(B)、螯合时间(C)3 个因素,以钙螯合能力为指标进行响应面优化。响应面试验因素和水平设置如表2所示。
表2 响应面试验因素和水平
Table 2 Codes and levels of independent variables used for response surface design

因素水平-101 A 1∶21∶12∶1 B 6.07.08.0 C 405060
1.3.8 BCP与BCP-Ca结构表征
1.3.8.1 紫外吸收光谱测定
分别将BCP和BCP-Ca溶于去离子水,配制成0.1 mg/mL的溶液,采用紫外-可见分光光度计在190~400 nm波长范围内扫描,以去离子水为空白进行基线校正[27]。
1.3.8.2 荧光光谱测定
将BCP溶于去离子水,配制成0.05 mg/mL的溶液,加入CaCl2,使反应体系中Ca2+浓度为0、25、50、100 mmol/L。采用荧光分光光度计进行光谱扫描,发射波长290~500 nm,激发波长280 nm[28]。
1.3.8.3 傅里叶变换红外光谱测定
分别将2 mg BCP和BCP-Ca与200 mg预干燥KBr粉末混合,经充分研磨后压制成透明薄片,采用傅里叶变换红外光谱仪在4 000~400 cm-1波数范围内扫描[29]。
1.3.8.4 X射线衍射图谱测定
取适量CaCl2、BCP和BCP-Ca,在X射线衍射仪上进行10°~80°连续扫描[30]。
1.3.8.5 扫描电子显微镜观察
取适量BCP和BCP-Ca均匀涂抹在样品板上,喷涂镀金膜后,采用扫描电子显微镜在5 kV加速电压下观察并采集显微图像[31]。
所有实验均设置3 次平行,数据均以平均值±标准差表示。利用SPSS 27.0软件对实验数据进行单因素方差分析和邓肯多重比较,利用Origin 2021软件绘图。
由图1可知,对于单酶体系,风味蛋白酶酶解产物的钙螯合能力最强,达到(51.08±0.62)mg/g,其次为木瓜蛋白酶,胰蛋白酶和中性蛋白酶酶解产物的钙螯合能力相对较低。风味蛋白酶可高效水解蛋白质生成游离氨基酸,从而暴露更多Ca2+螯合位点[32]。木瓜蛋白酶酶解产物水解度为(17.16±0.19)%,显著高于其他单酶(P<0.05)。Nawae等[33]采用5 种蛋白酶水解冷冻鸡肉,发现木瓜蛋白酶对鸡肉样品具有良好的消化效果,水解度达18%,与本研究结果一致。基于单酶筛选结果,选取木瓜蛋白酶与风味蛋白酶进行双酶酶解,分步酶解时,样品钙螯合能力和水解度均显著提高(P<0.05)。钙螯合能力达到(57.17±1.55)mg/g,水解度达(20.29±0.25)%。因此,本研究选取木瓜蛋白酶和风味蛋白酶进行双酶分步酶解制备BCP。
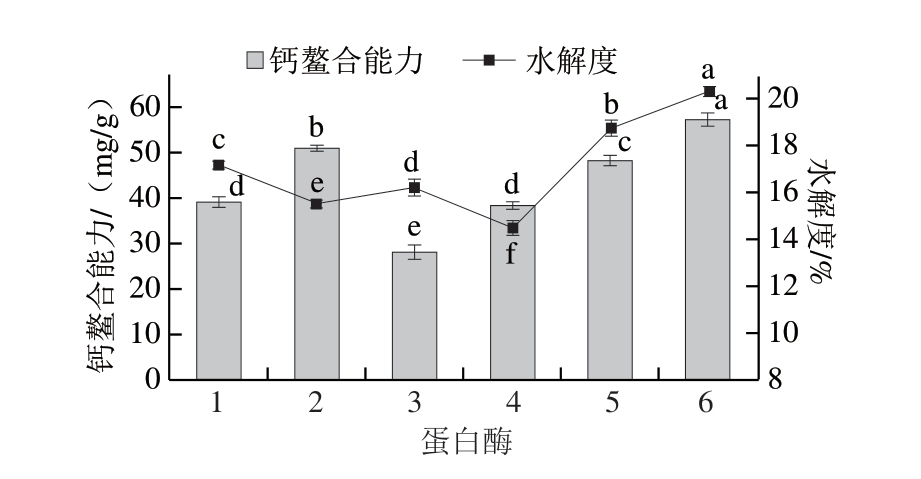
图1 不同蛋白酶对BCP水解度及钙螯合能力的影响
Fig. 1 Effect of different proteases on the hydrolysis degree and calcium-chelating ability of BCP
1.木瓜蛋白酶;2.风味蛋白酶;3.中性蛋白酶;4.胰蛋白酶;5.木瓜蛋白酶和风味蛋白酶同步酶解;6.木瓜蛋白酶和风味蛋白酶分步酶解;小写字母不同表示组间差异显著(P<0.05),图2同。
2.2.1 不同因素对BCP钙螯合能力的影响
由图2A可知,BCP的钙螯合能力随肽-钙质量比的增加呈现先增大后减小的变化趋势,当肽-钙质量比为1∶2时,体系中存在过量未螯合Ca2+;当肽-钙质量比为1∶1时,BCP与Ca2+的螯合达到饱和状态,继续增加肽-钙质量比,BCP的钙螯合能力反而下降。因此当肽-钙质量比为1∶1时,BCP的钙螯合能力最强,为(57.52±1.01)mg/g。
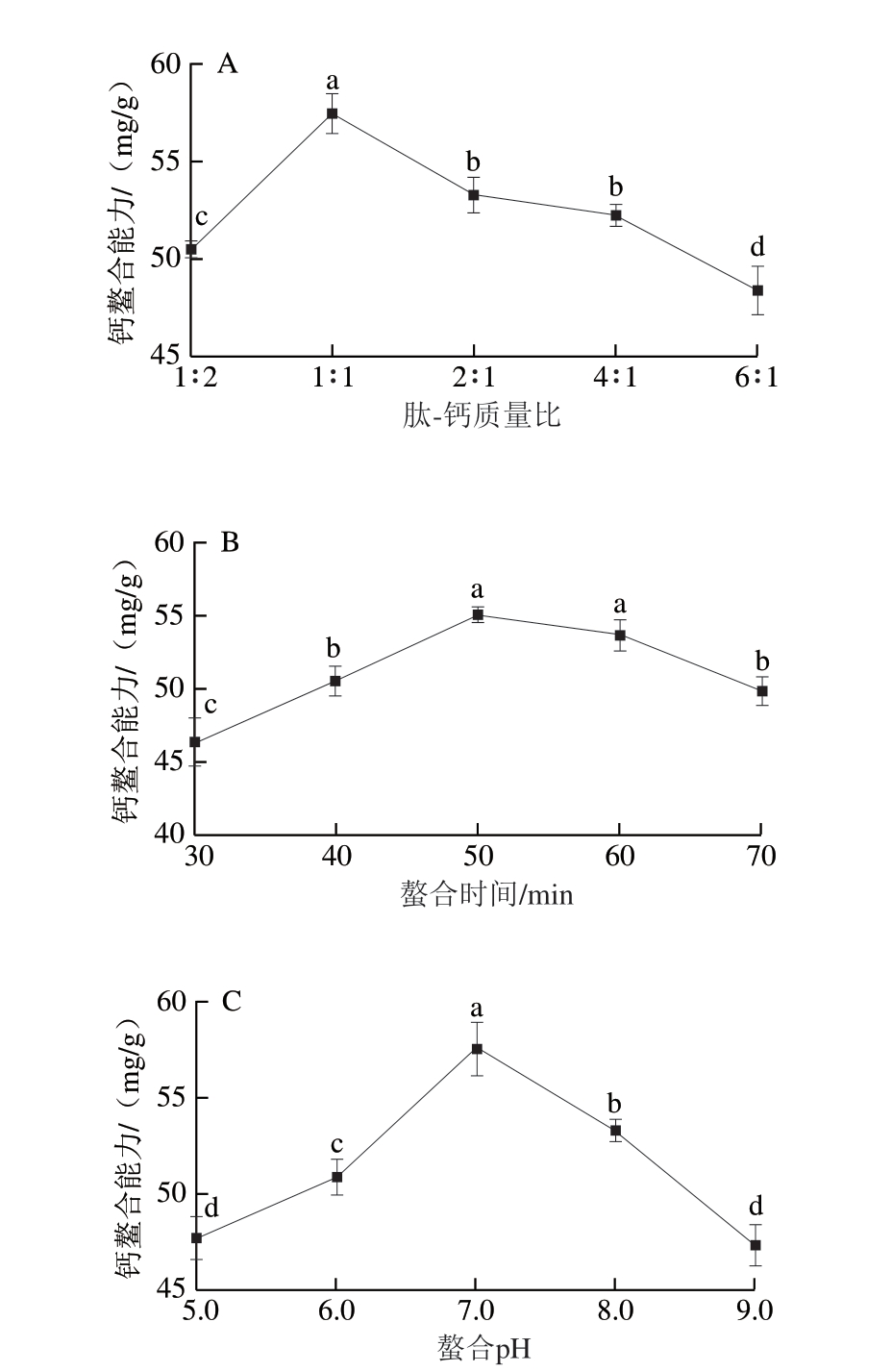
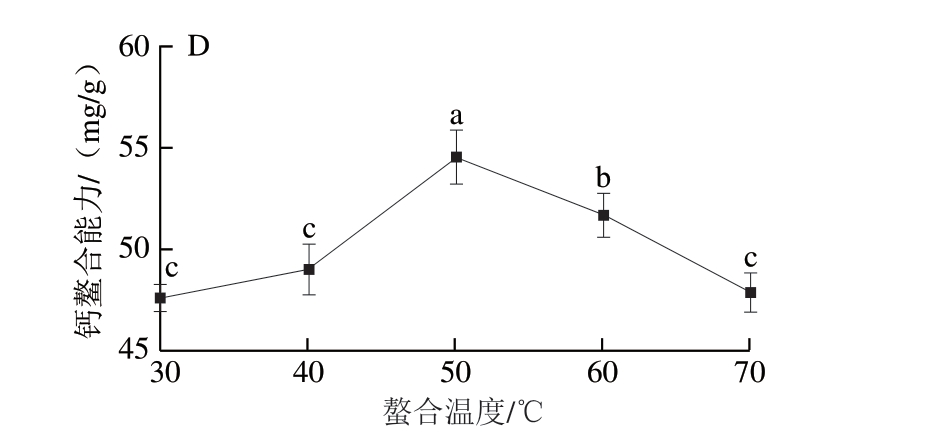
图2 肽-钙质量比(A)、螯合时间(B)、螯合pH值(C)、螯合温度(D)对BCP钙螯合能力的影响
Fig. 2 Effects of peptide-calcium mass ratio (A), chelation time (B),pH (C), and temperature (D) on the calcium-chelating ability of BCP
由图2B可知,随着螯合时间的延长,BCP的钙螯合能力呈现先增大后减小的变化趋势,当螯合时间为50 min时,钙螯合能力达到最强,为(55.08±0.54)mg/g;继续延长螯合时间至超过60 min时,钙螯合能力开始降低,可能归因于反应时间过长,螯合物不稳定而发生分解。
由图2C可知,随着pH值的升高,BCP的钙螯合能力先升高后下降,pH值为7.0时,钙螯合能力最强,达(57.52±1.38)mg/g,这是由于酸性条件下高浓度H+会竞争Ca2+配位位点,而碱性条件下过量OH-会与Ca2+形成Ca(OH)2沉淀,均会抑制螯合反应。
由图2D可知,BCP的钙螯合能力随温度的升高先增加后减小,当螯合温度为50 ℃时,BCP的钙螯合能力最强,可达(54.73±1.34)mg/g,温度过高或过低均会影响配位构象,导致钙螯合能力下降。
2.2.2 响应面试验结果及方差分析
2.2.2.1 响应面优化试验结果
基于单因素试验结果,选取肽-钙质量比(A)、螯合pH值(B)和螯合温度(C)3 个因素,依据Design-Expert 13软件中的Box-Behnken设计3因素3水平试验,试验设计及结果如表3所示。
表3 Box-Behnken试验设计及结果
Table 3 Box-Behnken design with experimental results
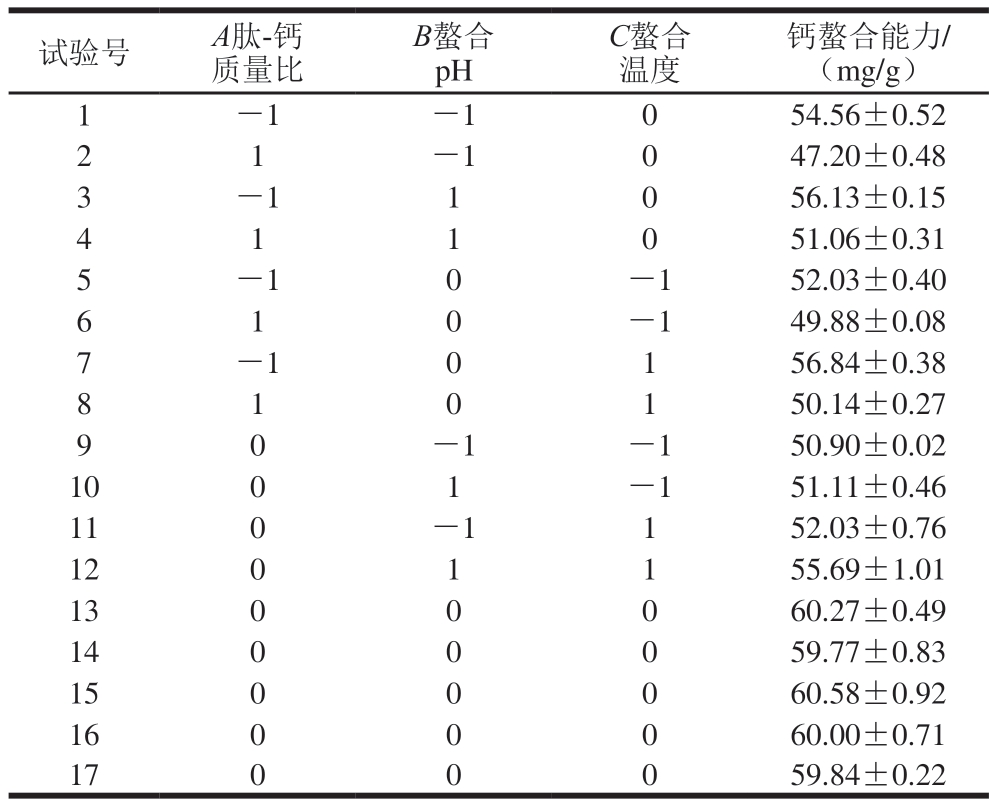
试验号A肽-钙质量比B螯合pH C螯合温度钙螯合能力/(mg/g)1-1-1054.56±0.52 2 1-1047.20±0.48 3-11056.13±0.15 4 1 1 051.06±0.31-10-152.03±0.40 6 1 0-149.88±0.08 5 7-10156.84±0.38 8 1 0 150.14±0.27-1-150.90±0.02 1001-151.11±0.46 110-1152.03±0.76 1201155.69±1.01 1300060.27±0.49 1400059.77±0.83 1500060.58±0.92 1600060.00±0.71 1700059.84±0.22 9 0
2.2.2.2 回归模型构建及方差分析
使用Design-Expert 13软件建立肽-钙质量比(A)、螯合pH值(B)、螯合温度(C)与钙螯合能力(Y)之间的多元二次回归模型,其方程为Y=60.10-2.66A+1.16B+1.35C+0.5721AB-1.14AC+0.8632BC-4.03A2-3.82B2-3.84C2。对建立的模型进行方差分析,结果见表4。模型极显著(F=99.22、P<0.01);失拟项不显著(P=0.060 8>0.05),表明模型拟合较好;R2=0.992 2、R2 Adj=0.982 2,表明模型拟合度较好,可用于分析和预测BCP-Ca制备工艺参数。在该模型中,A、B、C、AC、BC、A2、B2、C2均对钙螯合能力存在显著影响(P<0.05、P<0.01),且AC、BC交互作用显著。
表4 Box-Behnken回归模型方差分析
Table 4 Analysis of variance of Box-Behnken regression model
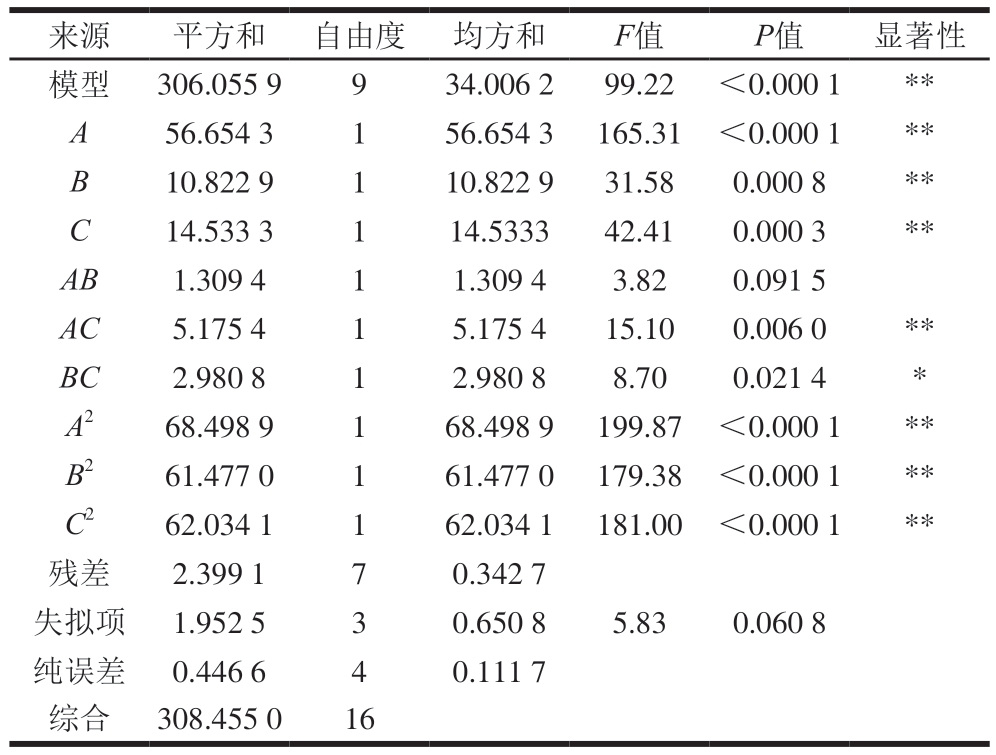
注:*.显著(P<0.05);**.极显著(P<0.01)。
来源平方和自由度均方和F值P值显著性模型306.055 9934.006 299.22<0.000 1**A56.654 3156.654 3165.31<0.000 1**B10.822 9110.822 931.580.000 8**C14.533 3114.5333 42.410.000 3**AB1.309 411.309 43.820.091 5 AC5.175 415.175 415.100.006 0**BC2.980 812.980 88.700.021 4*A268.498 9168.498 9199.87<0.000 1**B261.477 0161.477 0179.38<0.000 1**C262.034 1162.034 1181.00<0.000 1**残差2.399 170.342 7失拟项1.952 530.650 85.830.060 8纯误差0.446 640.111 7综合308.455 016
2.2.2.3 响应面交互作用分析
响应面图中,曲面陡峭且等高线密集呈椭圆形时,表明因素交互作用对响应值影响显著[34]。由图3可知,肽-钙质量比与螯合温度、螯合pH值和螯合温度交互作用的响应曲面均陡峭,表明2 组交互作用对钙螯合能力的影响均显著。肽-钙质量比和螯合pH值交互作用的等高线图近似圆形,表明交互作用较弱,与方差分析结果一致。
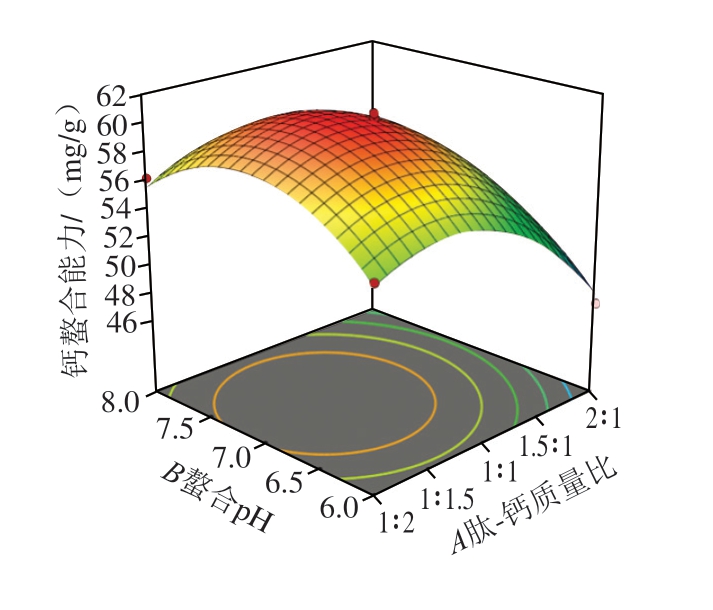
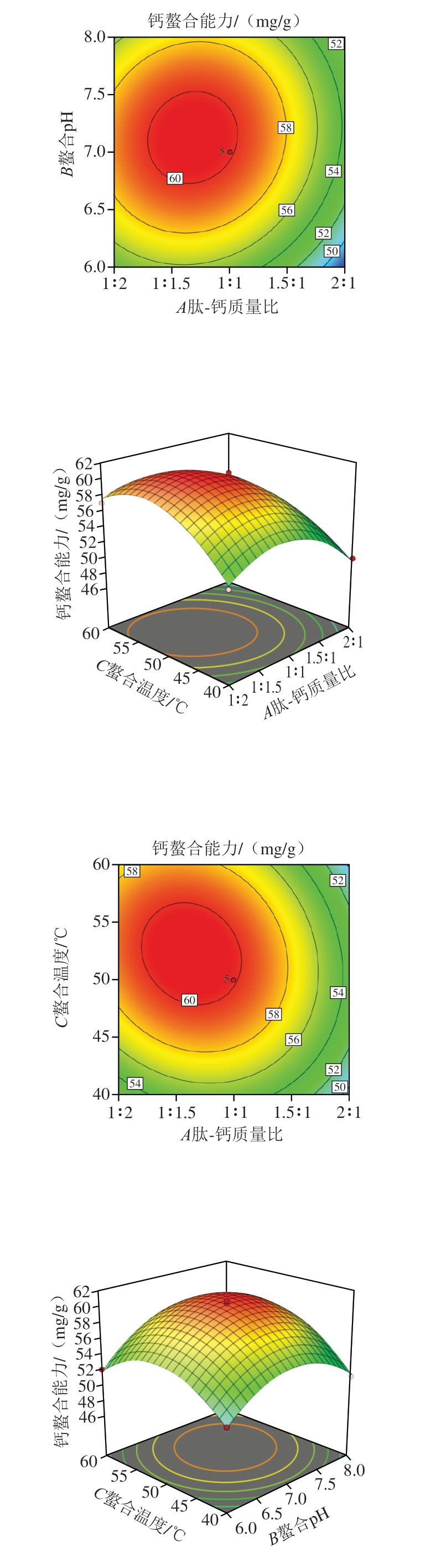
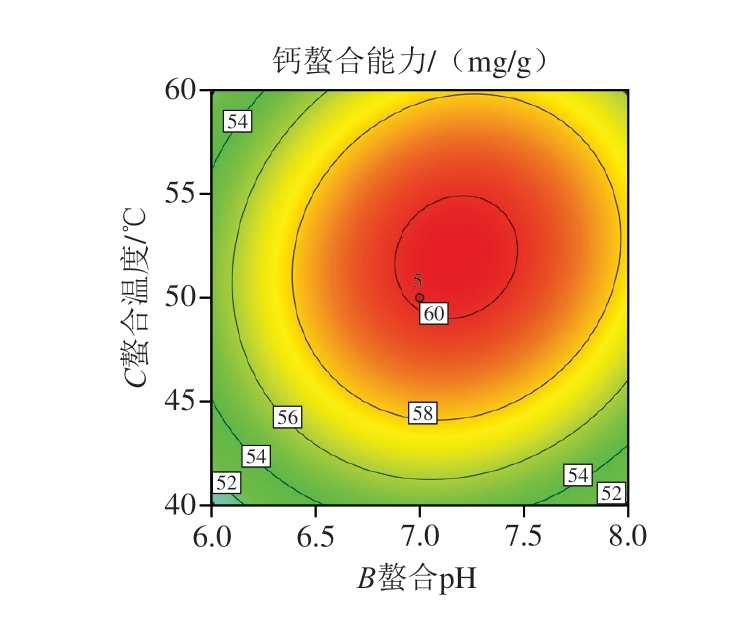
图3 各因素交互作用对钙螯合能力影响的响应面图和等高线图
Fig. 3 Response surface and contour plots showing the interactive effects of variables on calciul-chelating ability
2.2.2.4 验证实验结果
通过Design-Expert 13软件对多元二次回归方程进行分析,预测BCP-Ca制备工艺的最优条件为:肽-钙质量比1∶1、螯合pH 7.0、螯合温度51 ℃,在此条件下,BCP的钙螯合能力为60.66 mg/g。3 次验证实验结果表明,BCP的钙螯合能力为(60.19±0.35)mg/g,与模型预测值无显著差异(P>0.05),因此该模型具有可行性。齐立伟等[30]运用响应面法优化牛骨肽-钙螯合物制备条件,牛骨肽的钙螯合能力达55.65 μg/mg;龙芳[35]利用正交试验优化汉麻肽-钙螯合物制备工艺,在最佳条件下钙螯合能力为47.61 mg/g。相比之下,本研究制备的BCP具有较高的钙螯合能力。
2.3.1 紫外吸收光谱
金属离子与有机配体的配位作用可诱导配体特征吸收峰发生位移或强度变化[36]。如图4所示,BCP和BCP-Ca在200 nm附近均呈现特征性强吸收峰,归因于肽链酰胺键C=O的n→π*跃迁[37]。螯合后,最大吸光度从2.84降至2.42,吸收峰位从198 nm蓝移至195 nm,表明BCP分子结构发生改变并形成新物质。
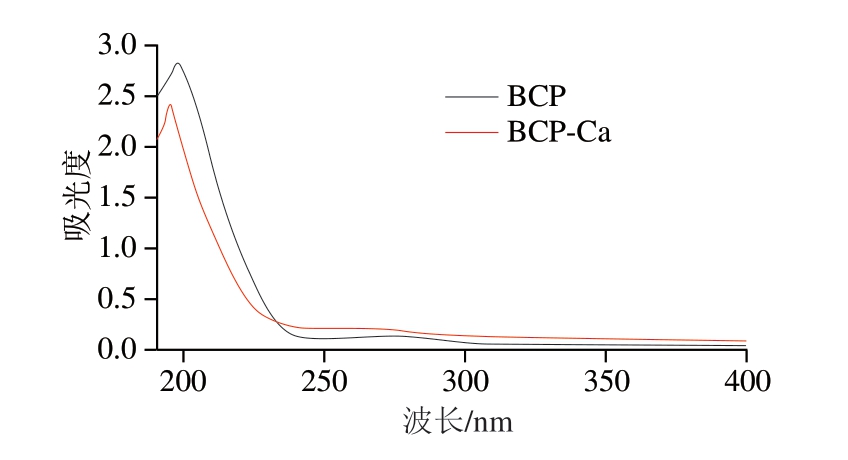
图4 BCP和BCP-Ca的紫外吸收光谱
Fig. 4 UV absorption spectra of BCP and BCP-Ca
2.3.2 荧光光谱
荧光强度变化可有效表征金属离子与配体的配位状态[9]。由图5可知,当BCP溶液中加入CaCl2后,荧光强度明显下降,且随着CaCl2浓度的增加,荧光强度逐渐降低,这与陈树泓[19]的研究结果类似。BCP与Ca2+的配位作用可能引起其分子内基团构象变化,导致荧光猝灭效应。荧光光谱分析证实,BCP-Ca的荧光特性明显区别于原始BCP,表明螯合作用改变了其分子性质。
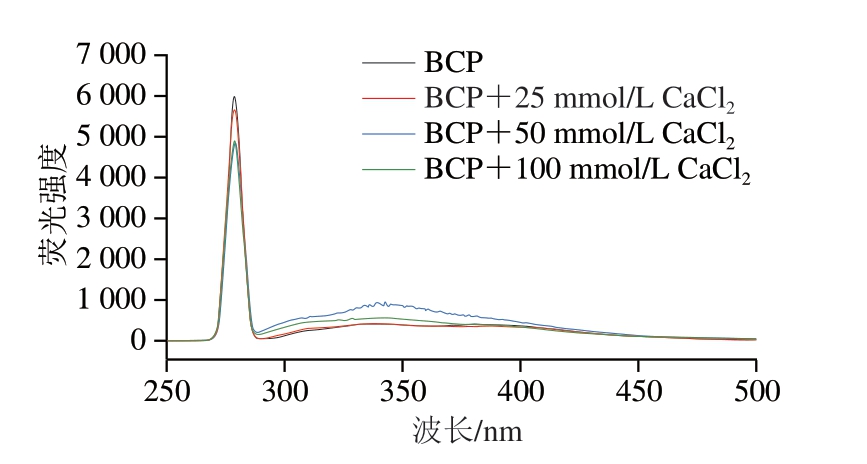
图5 BCP和BCP-Ca的荧光光谱
Fig. 5 Fluorescence spectra of BCP and BCP-Ca
2.3.3 傅里叶变换红外光谱
如图6所示,螯合反应引起官能团特征吸收峰位移。其中,3 291 cm-1处的特征峰对应肽键N—H的伸缩振动,螯合反应后其移至3 415 cm-1,表明氨基参与Ca2+螯合作用;2 868 cm-1附近的吸收峰对应C—H键的伸缩振动,螯合反应后其移至2 859 cm-1,表明C—H键环境改变;—COO-的吸收峰从1 401 cm-1移至1 465 cm-1,表明—COO-参与BCP与Ca2+的螯合;1 000 cm-1附近的吸收峰由—CO伸缩引起,1 081 cm-1处的C—O吸收峰发生蓝移,与玉米血管紧张素转化酶抑制肽-铁复合物中观察到的C—O吸收峰蓝移趋势[38]一致。此外,BCP-Ca在1 639 cm-1处出现的新吸收峰可能与COO-—Ca2+振动有关,该峰与鹿茸骨BCP-Ca COO-—Ca2+的振动峰位一致[39]。傅里叶变换红外光谱证实,BCP与Ca2+发生作用并形成一种新的化合物,推测—COO-和—NH是Ca2+的主要螯合反应位点。类似研究表明,钙的主要结合位点为核桃肽[40]和磷酸化鱼骨胶原肽[41]中的—COO-和—NH。
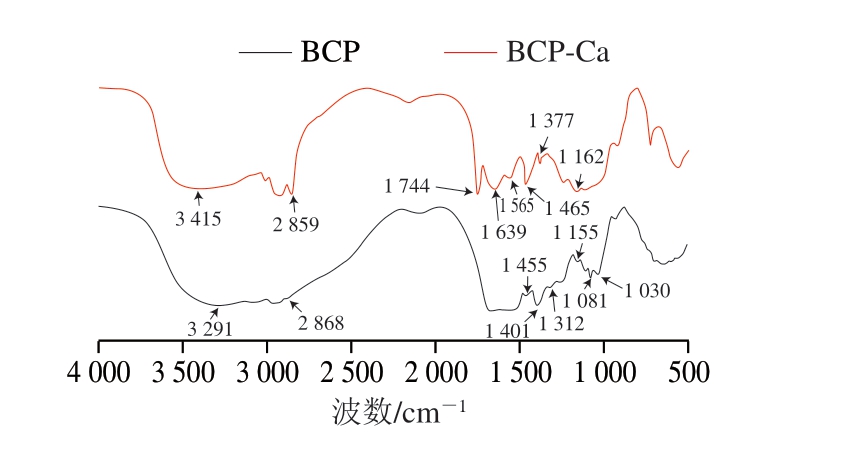
图6 BCP和BCP-Ca的傅里叶变换红外光谱
Fig. 6 FTIR spectra of BCP and BCP-Ca
2.3.4 X射线衍射图谱
X射线衍射图谱可用于评估分子晶体的形态变化和空间结构特点。由图7可知,BCP在2θ 20°附近出现强衍射峰,与蛋清多肽[42]特征峰位置一致,螯合后,该峰强度减弱,表明BCP肽链结构发生改变。而BCP-Ca在2θ 31.85°处有明显的吸收峰,且与CaCl2特征峰位置相一致,提示Ca2+与BCP功能基团发生配位或反应,形成含钙结晶相。
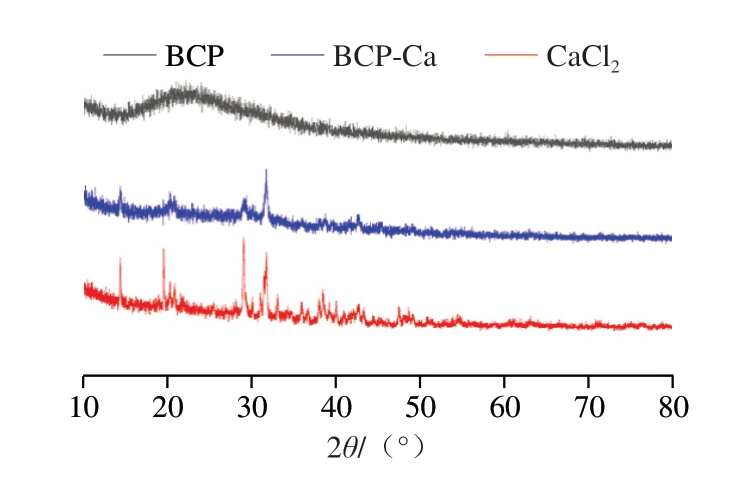
图7 BCP和BCP-Ca的X射线衍射图谱
Fig. 7 XRD patterns of BCP and BCP-Ca
2.3.5 扫描电子显微镜图
由图8可知,BCP表面光滑,整体呈片状结构,表面平整且颗粒分布相对较少,颗粒间结合较弱;而BCP-Ca结构变得粗糙,大量颗粒团簇附着于表面且分布均匀,整体呈团聚状形貌,这与Bao Zhijie等[43]的研究结果相似。这种形貌差异表明Ca2+的引入对BCP的微观结构产生显著影响,可能促进表面成核和颗粒团聚,并增强粒子间的相互作用,进一步证实BCP-Ca的形成。

图8 BCP(A)和BCP-Ca(B)的扫描电子显微镜图
Fig. 8 SEM images of BCP (A) and BCP-Ca (B)
本研究系统优BCP-Ca制备工艺,并初步探究BCP与Ca2+的螯合机制。结果表明,风味蛋白酶和木瓜蛋白酶的双酶分步酶解可有效提高BCP的水解度和钙螯合能力,优于单酶酶解。BCP-Ca最佳制备工艺条件为:肽-钙质量比1∶1、螯合pH 7.0、螯合温度51 ℃,在此条件下钙螯合能力达60.19 mg/g,与模型预测值(60.66 mg/g)无显著差异(P>0.05)。多种光谱与结构表征技术共同证实,螯合过程中BCP的化学结构与微观形貌均发生显著改变。紫外吸收光谱与荧光光谱显示肽链构象变化及荧光猝灭;傅里叶变换红外光谱表明,Ca2+与—COO-及—NH基团发生配位;X射线衍射与扫描电子显微镜进一步揭示晶体重构与表面形貌转变。这些结果一致表明,BCP与Ca2+通过配位作用形成结构重构的新型含钙物质。综上,BCP作为一种优良的钙载体,其螯合物具有潜在的应用价值。未来研究可进一步探讨BCP-Ca的稳定性和促进钙吸收作用,为其在功能性食品和营养补充剂中的应用提供更全面的科学依据。本研究结果可为新型补钙剂的研制和略阳乌鸡的高值化利用提供理论依据,有助于特色禽肉加工产业链的延伸与发展。
[1] 石景, 邹烨, 马晶晶, 等. 食源肽螯合钙的研究进展[J]. 食品工业科技, 2023, 44(11): 460-467. DOI:10.13386/j.issn1002-0306.2022070380.
[2] 黄春林, 林文静, 谢星, 等. 鮰鱼骨胶原蛋白肽-钙螯合物促进钙转运和成骨细胞分化作用[J]. 食品科学, 2024, 45(17): 35-41.DOI:10.7506/spkx1002-6630-20231205-031.
[3] 宫瑞林, 刘伯业, 陈复生, 等. 小麦蛋白肽钙螯合物的制备工艺及结构表征[J]. 河南工业大学学报(自然科学版), 2023, 44(6): 1-8; 43.DOI:10.16433/j.1673-2383.2023.06.001.
[4] 张昊彤, 周雪巍, 乔凯娜, 等. 肽-钙螯合方式及吸收机制研究现状[J]. 食品工业科技, 2024, 45(19): 383-391. DOI:10.13386/j.issn1002-0306.2023080325.
[5] 吴晗硕, 任杰, 付少委, 等. 玉米肽钙螯合物的结构表征和螯合机制[J]. 中国食品学报, 2024, 24(10): 115-123. DOI:10.16429/j.1009-7848.2024.10.011.
[6] SHI W, TAN C Y. Preparation of chickpea peptide-calcium chelates with antioxidant activity[J]. International Food Research Journal,2023, 30(6): 1471-1480. DOI:10.47836/ifrj.30.6.10.
[7] WANG Z L, JIANG H F, DAI J H, et al. Glycated walnut peptidecalcium chelates: structural properties, calcium absorption enhancement mechanism, and osteogenic effects[J]. Food Chemistry,2025, 489: 145039. DOI:10.1016/j.foodchem.2025.145039.
[8] ZHAO M G, HE H, GUO D J, et al. Chitosan oligosaccharidestripolyphosphate microcapsules as efficient vehicles for desalted duck egg white peptides-calcium: fabrication, entrapment mechanism and in vivo calcium absorption studies[J]. LWT-Food Science and Technology, 2022, 154: 112869. DOI:10.1016/j.lwt.2021.112869.
[9] YANG J, SHI J, ZHOU Y, et al. Preparation, characterization and stability of calcium-binding peptides derived from chicken blood[J].Foods, 2024, 13(15): 2368. DOI:10.3390/foods13152368.
[10] 黄文, 余可楠, 廖婉雯, 等. 响应面法优化罗非鱼鳞钙结合肽酶解工艺及其特性表征[J]. 食品工业科技, 2021, 42(21): 190-196.DOI:10.13386/j.issn1002-0306.2021020099.
[11] 胡香莲, 郦萍, 周柳莎, 等. 薏米多肽-钙、锌螯合物制备及结构表征[J]. 中国食品学报, 2024, 24(7): 229-240. DOI:10.16429/j.1009-7848.2024.07.023.
[12] BAO X L, YUAN X Y, FENG G X, et al. Structural characterization of calcium-binding sunflower seed and peanut peptides and enhanced calcium transport by calcium complexes in Caco-2 cells[J]. Journal of the Science of Food and Agriculture, 2021, 101(2): 794-804.DOI:10.1002/jsfa.10800.
[13] 刘卫震, 王冠华, 袁延佩, 等. 酪蛋白磷酸肽-钙螯合物的分级、表征及持钙特性[J]. 食品工业科技, 2024, 45(10): 93-100. DOI:10.13386/j.issn1002-0306.2023070209.
[14] 苑贤伟, 石梦园, 颜如玉, 等. 胶束酪蛋白复酶水解肽与钙形成螯合物的制备、表征及螯合机制[J]. 食品科学, 2024, 45(20): 57-64.DOI:10.7506/spkx1002-6630-20231120-143.
[15] 陈怡博, 刘媛, 陈锐, 等. 高效液相色谱法测定略阳乌鸡肌肉中的肌苷酸[J]. 食品与发酵工业, 2021, 47(6): 228-233. DOI:10.13995/j.cnki.11-1802/ts.025479.
[16] 方磊, 李诒光, 陈亮, 等. 乌鸡肽中潜在功能活性肽段的研究[J].食品与发酵工业, 2023, 49(15): 160-165. DOI:10.13995/j.cnki.11-1802/ts.033590.
[17] 崔林梅. 略阳乌鸡活性肽的制备及其功能特性研究[D]. 汉中: 陕西理工大学, 2024. DOI:10.27733/d.cnki.gsxlg.2024.000389.
[18] LIU X C, WEI X Y, SKIBSTED L H, et al. Investigation of the peptides with calcium chelating capacity in hydrolysate derived from spent hen meat[J]. Journal of Food Science, 2024, 89(4): 2277-2291.DOI:10.1111/1750-3841.17023.
[19] 陈树泓. 崇仁麻鸡肽螯合钙的制备及螯合性质研究[D]. 南昌: 南昌大学, 2023. DOI:10.27232/d.cnki.gnchu.2023.001522.
[20] 程钰, 胡蓉, 李强, 等. 复合蛋白酶水解菲律宾蛤蜊及产物的生物学活性研究[J]. 食品科技, 2024, 49(6): 134-141. DOI:10.13684/j.cnki.spkj.2024.06.020.
[21] 魏新颜, 苏国万, 孙为正. 鸡肉蛋白钙离子螯合肽酶解工艺的优化研究[J]. 现代食品科技, 2019, 35(8): 168-173; 330. DOI:10.13982/j.mfst.1673-9078.2019.8.025.
[22] 李朋泰, 刘亚慧, 孙少康, 等. 酶解法制备鸡骨抗氧化肽的工艺优化[J].食品科技, 2025, 50(3): 130-139.
[23] HU G H, WANG D B, SU R N, et al. Calcium-binding capacity of peptides obtained from sheep bone and structural characterization and stability of the peptide-calcium chelate[J]. Journal of Food Measurement and Characterization, 2022, 16(6): 4934-4946.DOI:10.1007/s11694-022-01580-2.
[24] 后鹏飞, 黄静, 罗丹, 等. 响应面法优化南方大口鲶鱼骨多肽酶解工艺及其风味分析[J]. 食品科技, 2023, 48(12): 127-134.DOI:10.13684/j.cnki.spkj.2023.12.039.
[25] 国家市场监督管理总局, 国家卫生健康委员会. 食品安全国家标准食品中蛋白质的测定: GB 5009.5—2025[S]. 北京: 中国标准出版社,2025.
[26] 国家卫生和计划生育委员会, 国家食品药品监督管理总局. 食品安全国家标准 食品中钙的测定: GB 5009.92—2016[S]. 北京: 中国标准出版社, 2016.
[27] QIN X Y, ZHANG J T, LI G M, et al. Structure and composition of a potential antioxidant obtained from the chelation of pea oligopeptide and sodium selenite[J]. Journal of Functional Foods, 2020, 64: 103619.DOI:10.1016/j.jff.2019.103619.
[28] 张春芝, 王明清, 黄国清, 等. 花生蛋白钙螯合肽的制备、富集及表征[J]. 中国粮油学报, 2023, 38(11): 83-91. DOI:10.20048/j.cnki.issn.1003-0174.000623.
[29] 刘俊霞, 吴艳, 赵世博, 等. 响应面法优化大鲵肽-硒螯合物制备工艺及其性质研究[J]. 食品与发酵工业, 2024, 50(11): 185-194.DOI:10.13995/j.cnki.11-1802/ts.035888.
[30] 齐立伟, 张鸿儒, 郭玉杰, 等. 牛骨肽钙螯合物制备、表征及其促MC3T3-E1细胞成骨活性[J]. 食品科学, 2023, 44(6): 107-115.DOI:10.7506/spkx1002-6630-20220319-226.
[31] DING Q Z, SHEIKH A R, ZHU Y Q, et al. Preparation and characterization of ultrasound-assisted novel peptide-calcium chelates from nannocholoropsis oceanica[J]. Food and Bioprocess Technology,2025, 18(3): 2820-2839. DOI:10.1007/s11947-024-03634-3.
[32] 张祎. 商业大豆分离蛋白酶解产物分析及其对肌原纤维蛋白凝胶特性的影响[D]. 广州: 华南理工大学, 2021. DOI:10.27151/d.cnki.ghnlu.2021.002123.
[33] NAWAE W, SUNTORNSUK W. Animal growth stimulation by enzymatic protein hydrolysate of chicken residues[J]. The Journal of Animal and Plant Sciences, 2020, 31(2): 369-376. DOI:10.36899/japs.2021.2.0224.
[34] 王一全, 刘慈坤, 李学鹏, 等. 响应面法优化预制虾饼的加工工艺[J].肉类研究, 2024, 38(12): 34-41. DOI:10.7506/rlyj1001-8123-20240722-189.
[35] 龙芳. 汉麻肽钙螯合物的制备及其结构表征和稳定性[J]. 中国油脂,2021, 46(9): 33-39. DOI:10.19902/j.cnki.zgyz.1003-7969.200626.
[36] SUN N, CUI P B, LIN S Y, et al. Characterization of sea cucumber(Stichopus japonicus) ovum hydrolysates: calcium chelation, solubility and absorption into intestinal epithelial cells[J]. Journal of the Science of Food and Agriculture, 2017, 97(13): 4604-4611. DOI:10.1002/jsfa.8330.
[37] WU W M, HE L C, LIANG Y H, et al. Preparation process optimization of pig bone collagen peptide-calcium chelate using response surface methodology and its structural characterization and stability analysis[J]. Food Chemistry, 2019, 284: 80-89. DOI:10.1016/j.foodchem.2019.01.103.
[38] QU W J, FENG Y T, XIONG T, et al. Preparation of corn ACE inhibitory peptide-ferrous chelate by dual-frequency ultrasound and its structure and stability analyses[J]. Ultrasonics Sonochemistry, 2022,83: 105937. DOI:10.1016/j.ultsonch.2022.105937.
[39] WANG Z G, ZHAI X R, XIAO X Y, et al. Novel peptides with calciumbinding capacity from antler bone hydrolysate, its bioactivity on MC3T3-E1 cells, and the possible chelating mode[J]. Food Science &Nutrition, 2024, 12(11): 9069-9084. DOI:10.1002/fsn3.4441.
[40] ZHENG W Z, WANG J N, YAO X Y, et al. Preparation, structural characterisation, absorption and calcium transport studies of walnut peptide calcium chelate[J]. Food & Function, 2025, 16(2): 461-474.DOI:10.1039/D4FO04403G.
[41] 黄海, 付满, 宁恒孙. 鱼骨胶原肽磷酸化及其肽-钙螯合物的制备[J]. 中国食品添加剂, 2023, 34(8): 87-93. DOI:10.19804/j.issn1006-2513.2023.08.011.
[42] 王晴晴, 蔡为荣, 汪玉玲, 等. 蛋清多肽-铁螯合物的制备、表征及对Caco-2细胞的促增殖作用[J]. 食品与发酵工业, 2024, 50(4): 197-203. DOI:10.13995/j.cnki.11-1802/ts.034297.
[43] BAO Z J, ZHANG P L, SUN N, et al. Elucidating the calciumbinding site, absorption activities, and thermal stability of egg white peptide-calcium chelate[J]. Foods, 2021, 10(11): 2565. DOI:10.3390/foods10112565.