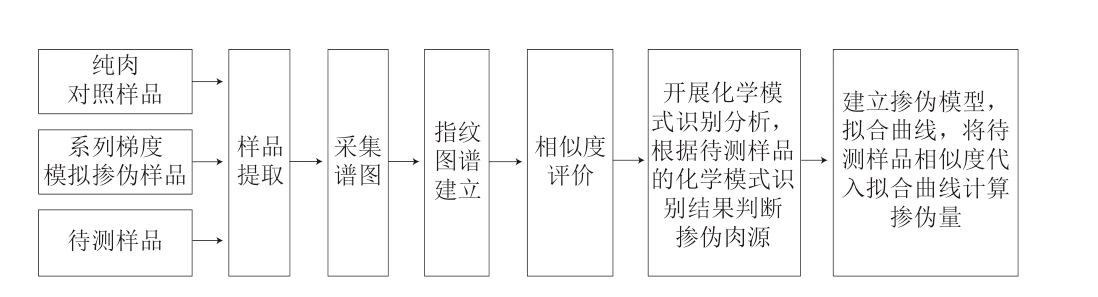
图1 待测样品检测技术路线
Fig. 1 Technical route for detection of test samples
High Performance Liquid Chromatographic Fingerprinting Combined with Chemical Pattern Recognition for Meat Adulteration Identification
张雅莉, 陈修红, 刘佳, 等. 高效液相色谱指纹图谱结合化学模式识别在肉类掺伪鉴别中的应用[J]. 肉类研究, 2026,40(4): 69-75. DOI:10.7506/rlyj1001-8123-20250429-129. http://www.rlyj.net.cn
ZHANG Yali, CHEN Xiuhong, LIU Jia, et al. High performance liquid chromatographic fingerprinting combined with chemical pattern recognition for meat adulteration identification[J]. Meat Research, 2026, 40(4): 69-75. DOI:10.7506/rlyj1001-8123-20250429-129. http://www.rlyj.net.cn
牛羊肉营养价值高且味道鲜美,颇受消费者喜爱[1]。近年来,牛羊肉价格不断上涨,为谋取更大利益,部分不法商贩在牛羊肉中掺入或直接使用廉价肉源(如猪肉、鸭肉等)压制后冒充优等牛羊肉[1-6]。肉类掺伪现象可能引发宗教冲突等问题,甚至可能给消费者带来健康风险,如食物过敏和中毒等[1,4,7]。
目前,肉类掺伪鉴别方法主要有感官法、免疫法、聚合酶链式反应(polymerase chain reaction,PCR)法、光谱法、质谱法等[3,8-10]。感官法操作简单,不需要复杂的检测设备且成本较低,但对检测人员要求很高,且准确度不高[9];免疫法特异性高,不需要大型仪器设备,但该法易受到外界干扰,因此应用并不广泛[3,11];PCR法具有高灵敏度、高特异性和高分辨率,但该法较为复杂,且对仪器设备要求较高,成本较高[9-10,12];光谱法具有无损、快速和便携等优点,但该法目前在肉类掺伪检测中的应用较少,相关的数据信息有限[8,10];质谱法具有高准确性和高灵敏度,但该法设备价格昂贵,且对操作人员的技术水平要求较高[8,13]。
不同物种的肉类具有不同的风味[14],核苷酸是肉类风味的主要贡献前体,如胞苷酸、尿苷酸、鸟苷酸、肌苷酸、腺苷酸、次黄嘌呤、肌苷等[15-17]。研究[18-19]表明,不同物种肉质中呈味核苷酸的比例存在一定的差异,这种差异可以作为鉴别肉质掺伪的依据。指纹图谱和化学模式识别技术是近年来发展迅速的分析方法,在中药、食品分析等领域取得了显著成果[20-24]。指纹图谱能够全面反映样品的化学成分信息,而化学模式识别技术则能对这些信息进行高效处理和分析[25],从而实现掺伪鉴别的目的。
本研究旨在利用高效液相色谱(high performance liquid chromatography,HPLC)指纹图谱结合化学模式识别技术,选择羊肉和猪肉体系、牛肉和鸭肉体系,基于呈味核苷酸成分的分析建立一种快速、准确的掺伪鉴别方法,为我国肉类市场的监管提供技术支持。
5 批次纯羊肉(记为M-1~M-5)、5 批次纯猪肉(记为P-1~P-5)、4 批次纯牛肉(记为B-1~B-4)、4 批次纯鸭肉(记为D-1~D-4)、2 批次未知羊肉、3 批次未知牛肉样品均采购自当地市场。
肌苷(CAS 58-63-9,纯度99.4%)、5’-肌苷酸二钠(CAS 4691-65-0,纯度99.9%)、5’-鸟苷酸二钠(CAS 5550-12-9,纯度92.5%)、5’-腺苷酸(CAS 61-19-8,纯度98.9%)、次黄嘌呤(CAS 68-94-0,纯度99.9%)标准品 天津阿尔塔科技有限公司;甲醇(色谱纯)、高氯酸(纯度70%~72%) 上海安谱实验科技股份有限公司;磷酸二氢钾、磷酸氢二钾(均为分析纯) 国药集团化学试剂有限公司;氢氧化钠(分析纯) 西陇科学股份有限公司;实验用水为超纯水。
LC-20AD HPLC仪(配备紫外检测器) 日本岛津公司;AB135-S分析天平(感量0.01 mg)、AB204-S分析天平(感量0.1 mg) 瑞士Mettler Toledo公司;FW-100粉碎机 天津市泰斯特仪器有限公司;JXFSTPRPMiniCL-AUTO全自动浸入式液氮冷冻研磨仪 上海净信实业发展有限公司;KQ-500DB超声波清洗机 昆山市超声仪器有限公司;T-50.2L砂芯过滤装置、滤膜(尼龙,0.22 μm) 天津市津腾实验设备有限公司;T25均质机 德国IKA公司;4-20R离心机 湖南可成仪器设备有限公司;Milli-Q超纯水系统 美国Millipore公司。
1.3.1 标准溶液配制
分别准确称取适量5’-鸟苷酸二钠、5’-肌苷酸二钠、次黄嘌呤、5’-腺苷酸、肌苷标准品,加水溶解并定容,分别配制成质量浓度1 000、1 000、400、1 000、1 000 μg/mL的标准储备液,4 ℃保存,有效期3 个月。分别量取适量标准储备液,加水稀释并定容,配制成质量浓度分别为20、160、20、20、80 μg/mL的混合标准溶液,现配现用。
1.3.2 样品制备
纯羊肉、纯猪肉、纯牛肉和纯鸭肉样品制备:取适量样品,加液氮研磨粉碎后置于-80 ℃冰箱备用。
羊肉模拟掺伪样品制备:取适量纯羊肉和纯猪肉样品按质量比3∶1、2∶1、1∶1、1∶2、1∶3混合,搅打均匀,加液氮研磨粉碎后置于-80 ℃冰箱备用,分别记为M+P(3∶1)、M+P(2∶1)、M+P(1∶1)、M+P(1∶2)、M+P(1∶3),羊肉中猪肉质量分数分别为25%、33%、50%、67%、75%。
牛肉模拟掺伪样品制备:取适量纯牛肉和纯鸭肉样品按质量比3∶1、2∶1、1∶1、1∶2、1∶3混合,搅打均匀,加液氮研磨粉碎后置于-80 ℃冰箱备用,分别记为B+D(3∶1)、B+D(2∶1)、B+D(1∶1)、B+D(1∶2)、B+D(1∶3),牛肉中鸭肉质量分数分别为25%、33%、50%、67%、75%。
1.3.3 样品提取
称取2 g样品,置于50 mL离心管中,用20 mL 5 g/100 mL高氯酸溶液分3 次匀浆,匀浆液4 ℃、4 000 r/min离心10 min,将上清液转移至50 mL烧杯中,合并上清液,用5 mol/L氢氧化钠溶液调整pH值至7左右,转移至50 mL容量瓶中,用水定容,摇匀,经滤膜过滤后待测。
1.3.4 仪器条件
参考黎琪等[26]的方法并进行优化。色谱柱:ChromCore AQ C18(250 mm×4.6 mm,5 μm);柱温40 ℃;进样体积10 μL;流速1 mL/min;流动相A为50 mmol/L磷酸二氢钾溶液(用8 g/100 mL磷酸氢二钾调整pH值至5.4),流动相B为30%甲醇溶液,梯度洗脱:0~14 min,100% A;14~15 min,100%~0% A;15~19 min,0% A;19~20 min,0%~100% A;20~26 min,100% A;数据采集时间2~22 min;检测波长254 nm。
1.3.5 指纹图谱方法学考察
1.3.5.1 仪器精密度
称取同一批次样品,按照1.3.3节描述的方法进行处理,按照1.3.4节描述的方法进行分析,连续进样6 次,选择7号峰作为参照峰,并分别计算共有峰的相对峰面积和相对保留时间,计算相对标准偏差(relative standard deviation,RSD)[27-28]。
1.3.5.2 重复性
称取同一批次样品6 份,按照1.3.3节描述的方法进行处理,按照1.3.4节描述的方法进行分析,选择7号峰作为参照峰,并分别计算共有峰的相对峰面积和相对保留时间,计算RSD。
1.3.5.3 稳定性
称取同一批次样品,按照1.3.3节描述的方法进行处理,按照1.3.4节描述的方法进行分析,分别在0、2、4、8、12、24 h时间点进行检测,选择7号峰作为参照峰,并分别计算共有峰的相对峰面积和相对保留时间,计算RSD。
1.3.6 指纹图谱分析
将各样品按照1.3.3节描述的方法进行处理,按照1.3.4节描述的方法进行分析,采集谱图,以cdf格式导入中药色谱指纹图谱相似度评价系统(2012版),分别以M-1和B-1样品谱图作为参照图谱,设定时间窗宽度为0.1 min,进行多点校正后与mark峰匹配,建立指纹图谱,标定共有峰,并进行相似度分析。
1.3.7 化学模式识别分析
将各样品的共有峰相关数据导入SIMCA 18软件进行化学模式识别分析,包括聚类分析(hierarchical clustering analysis,HCA)和主成分分析(principal component analysis,PCA)。HCA以“ward”模式为距离计算方式,以“size”为分类方式,对数据进行系统聚类。PCA采用无监督模式识别,选择前2 个PC进行区分。
1.3.8 掺伪模型建立
结合掺伪量及对应的相似度,分别拟合绘制相似度与掺伪量的关系曲线,并得出对应的拟合方程。
1.3.9 样品检测和方法比对
基于以下技术路线(图1)对市场采购的未知羊肉和牛肉样品进行检测,并与实时荧光PCR法[29]检测结果进行比对。

图1 待测样品检测技术路线
Fig. 1 Technical route for detection of test samples
指纹图谱方法学考察结果显示,精密度、重复性和稳定性实验的各共有峰相对保留时间和相对峰面积的RSD均小于3%,表明精密度、重复性和稳定性良好,符合指纹图谱研究的技术要求[30]。羊肉和猪肉相关样品及牛肉和鸭肉相关样品指纹图谱叠加如图2A、B所示。
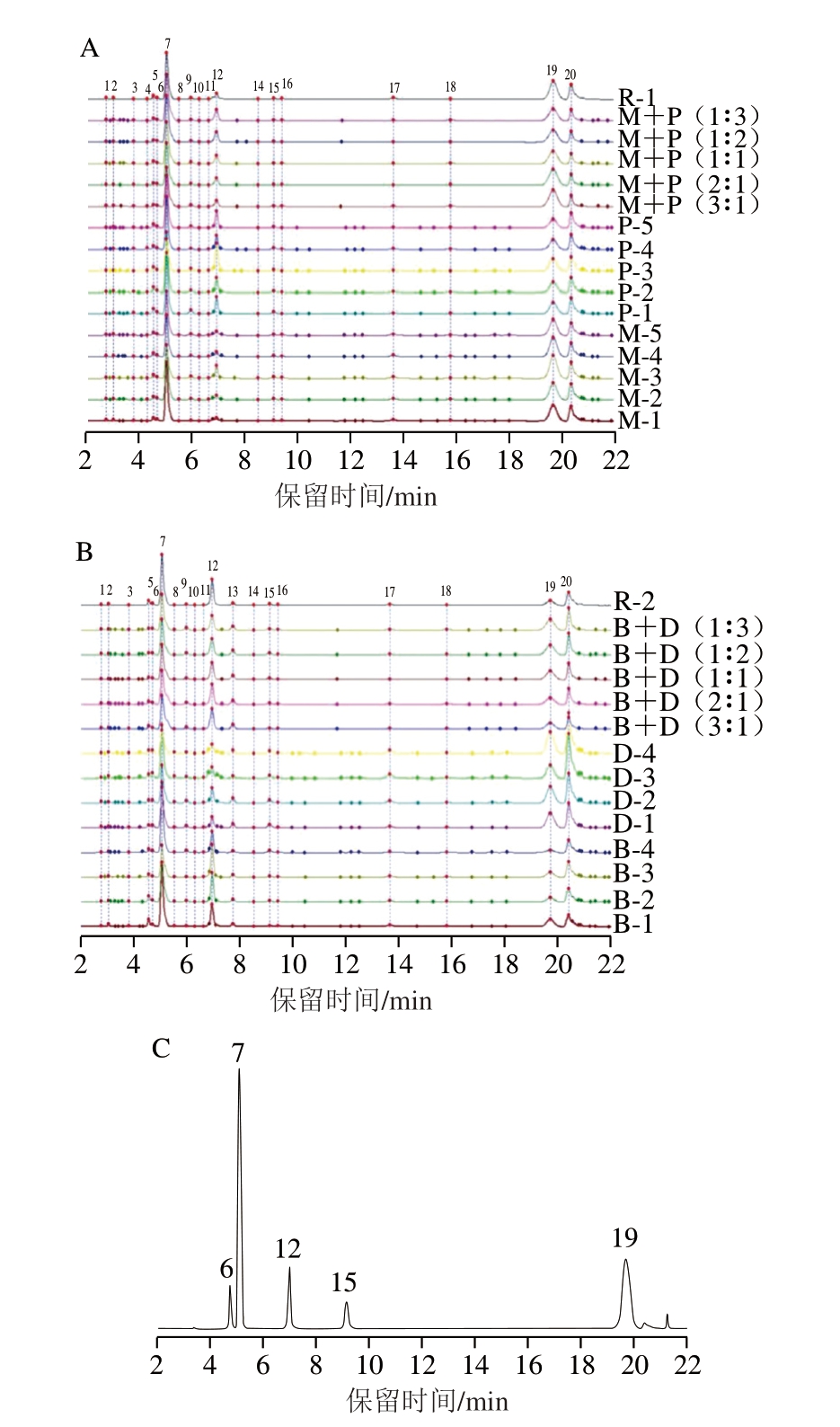
图2 羊肉和猪肉相关样品指纹图谱叠加(A)、牛肉和鸭肉相关样品指纹图谱叠加(B)和混合标准溶液谱图(C)
Fig. 2 Overlapping fingerprints of mutton and pork samples (A),overlapping fingerprints of beef and duck samples (B), and chromatogram of mixed standard solution (C)
R-1、R-2.分别为以中位数法生成的羊肉、牛肉对照指纹图谱。
通过羊肉和猪肉及牛肉和鸭肉谱峰匹配,均标定了19 个共有峰(峰号标记为1~12、14~20),其中6、7、12、15、19号峰经与对照品(图2C)进行比对,分别确认为5’-鸟苷酸、5’-肌苷酸、次黄嘌呤、5’-腺苷酸和肌苷。
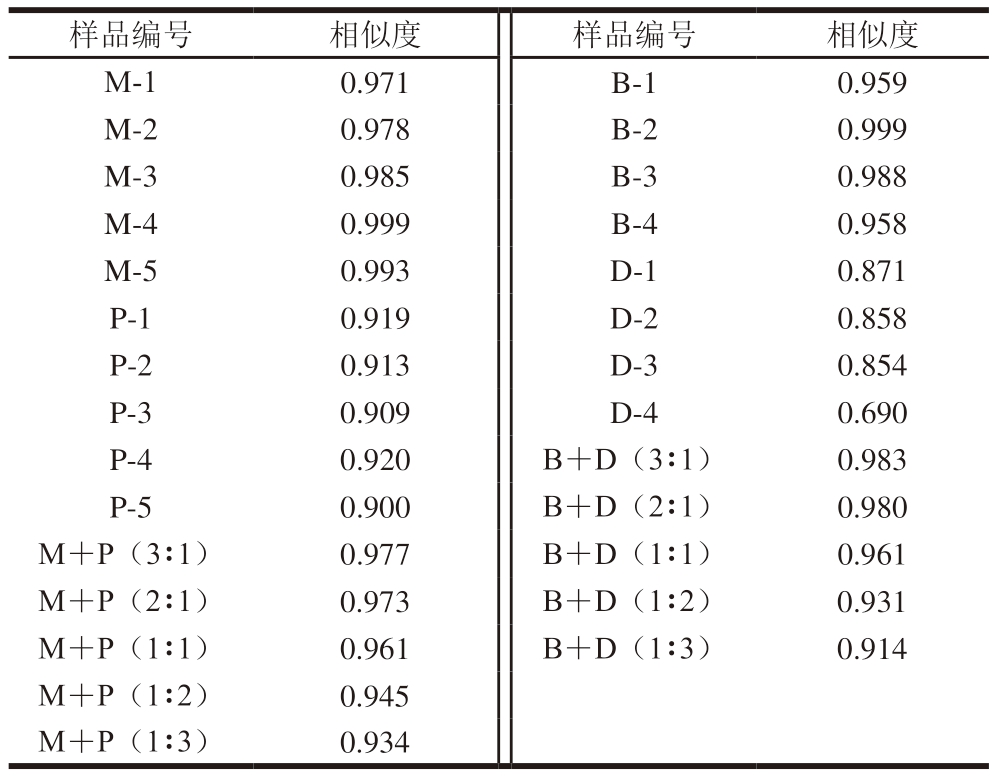
指纹图谱的2 个基本属性为整体性和模糊性。前者强调的是待测样品和对照样品的相似性,而不是完全相同;后者则强调要完整地比较指纹图谱的特征,而不是将图谱“肢解”。利用相似度描述指纹图谱之间的相似情况,即把指纹图谱看作一个整体来考虑,不局限于某一种成分的含量高低[31]。常用的相似度计算方法包括夹角余弦法和相关系数法等,本研究使用中药色谱指纹图谱相似度评价系统(2012版),采用夹角余弦法。相似度评价是指纹图谱法质量评价的重要环节,相似度是评价指纹图谱之间相似程度的一个重要量化指标。相似度越高,说明待测样品图谱与对照指纹图谱越相似、差异性越小[31-33]。将羊肉样品(M-1~M-5)以中位数法生成羊肉对照指纹图谱(R-1),牛肉样品(B-1~B-4)以中位数法生成牛肉对照指纹图谱(R-2),并将羊肉和猪肉相关样品与R-1进行比较,将牛肉和鸭肉相关样品与R-2进行比较,得到各样品的相似度评价。如表1所示,羊肉样品(M-1~M-5)的相似度为0.971~0.999,猪肉样品(P-1~P-5)的相似度为0.900~0.920,羊肉和猪肉混合样品(M+P(3∶1)、M+P(2∶1)、M+P(1∶1)、M+P(1∶2)、M+P(1∶3))的相似度为0.934~0.977,且随着猪肉掺入比例的提高,相似度逐渐下降;牛肉样品(B-1~B-4)的相似度为0.958~0.999,鸭肉样品(D-1~D-4)的相似度为0.690~0.871,牛肉和鸭肉混合样品(B+D(3∶1)、B+D(2∶1)、B+D(1∶1)、B+D(1∶2)、B+D(1∶3))的相似度为0.914~0.983,且随着鸭肉掺入比例的提高,相似度逐渐下降。以上结果说明,羊肉和猪肉、牛肉和鸭肉的呈味核苷酸种内差异较小、种间差异较大,且掺入比例和相似度存在一定的相关性,因此可以相似度作为评价指标,评价羊肉中猪肉、牛肉中鸭肉的掺伪情况。
表1 各样品相似度评价结果
Table 1 Similarity evaluation results of samples
样品编号相似度样品编号相似度M-10.971 B-10.959 M-20.978 B-20.999 M-30.985 B-30.988 M-40.999 B-40.958 M-50.993 D-10.871 P-10.919 D-20.858 P-20.913 D-30.854 P-30.909 D-40.690 P-40.920 B+D(3∶1)0.983 P-50.900 B+D(2∶1)0.980 M+P(3∶1)0.977 B+D(1∶1)0.961 M+P(2∶1)0.973 B+D(1∶2)0.931 M+P(1∶1)0.961 B+D(1∶3)0.914 M+P(1∶2)0.945 M+P(1∶3)0.934
通过HCA可直观观察不同肉类及肉类混合样品的分类特征。如图3A所示,当聚类距离为10时,羊肉样品(M-1~M-5)、猪肉样品(P-1~P-5)及羊肉和猪肉混合样品(M+P(3∶1)、M+P(2∶1)、M+P(1∶1)、M+P(1∶2)、M+P(1∶3))分别聚为一类;如图3B所示,当聚类距离为20时,牛肉样品(B-1~B-4)、鸭肉样品(D-1~D-4)及牛肉和鸭肉混合样品(B+D(3∶1)、B+D(2∶1)、B+D(1∶1)、B+D(1∶2)、B+D(1∶3))分别聚为一类。以上结果说明,同种肉类的呈味核苷酸组成高度相似,且不同肉类基于共有峰数据具有较高的区分度。
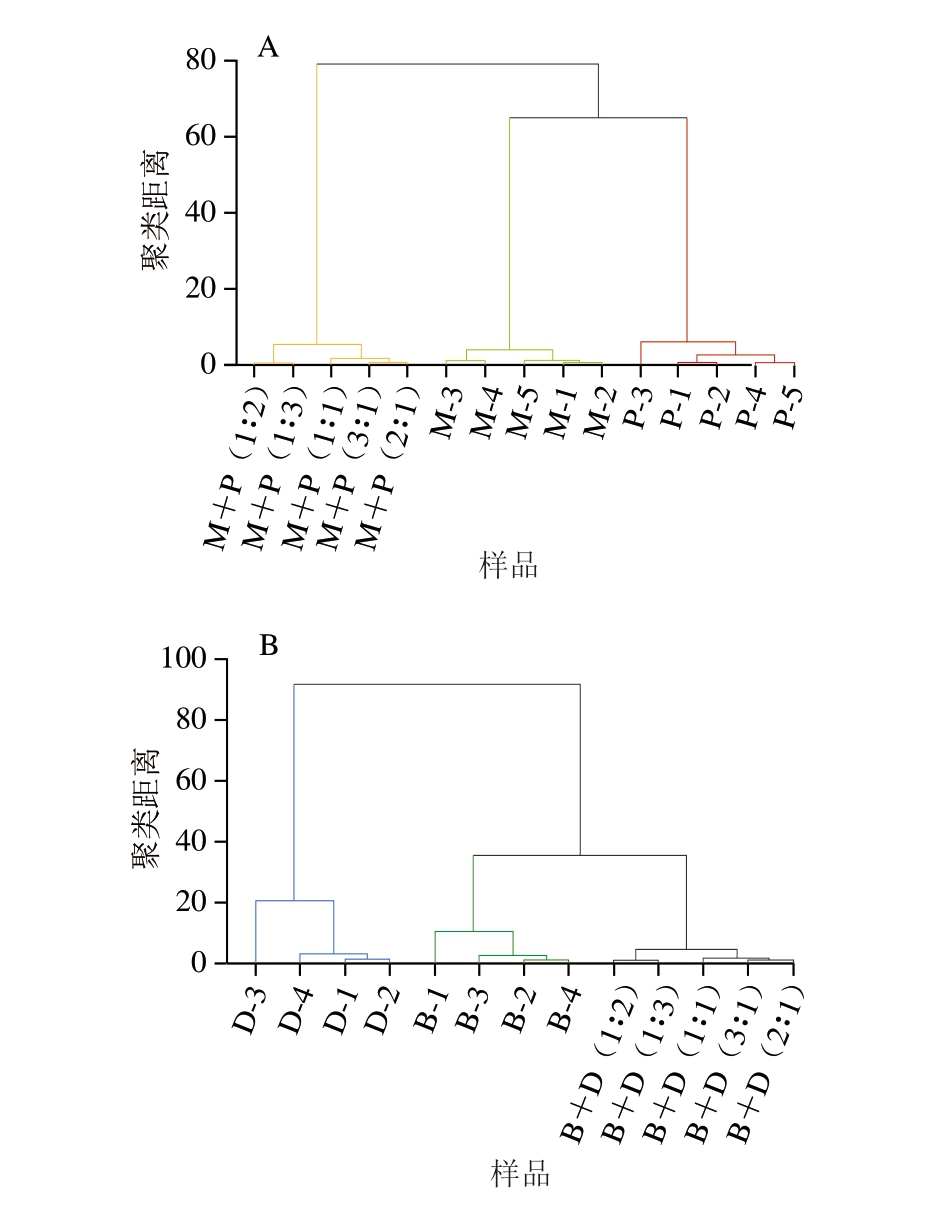
图3 羊肉、猪肉及混合样品(A)、牛肉、鸭肉及混合样品(B)的HCA图
Fig. 3 HCA plots of mutton, pork and mixed samples (A) and beef,duck and mixed samples (B)
采用PCA进一步验证不同肉类及肉类混合样品的分类规律。如图4A所示,样品聚为3 类,羊肉样品(M-1~M-5)为一类,猪肉样品(P-1~P-5)为一类,羊肉和猪肉混合样品(M+P(3∶1)、M+P(2∶1)、M+P(1∶1)、M+P(1∶2)、M+P(1∶3))为一类;如图4B所示,样品聚为3 类,牛肉样品(B-1~B-4)为一类,鸭肉样品(D-1~D-4)为一类,牛肉和鸭肉混合样品(B+D(3∶1)、B+D(2∶1)、B+D(1∶1)、B+D(1∶2)、B+D(1∶3))为一类。这与2.4节分析结果基本一致。
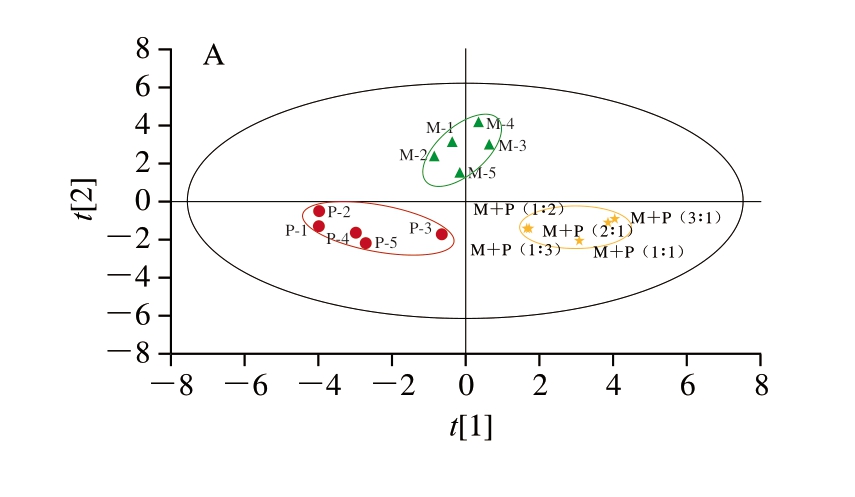
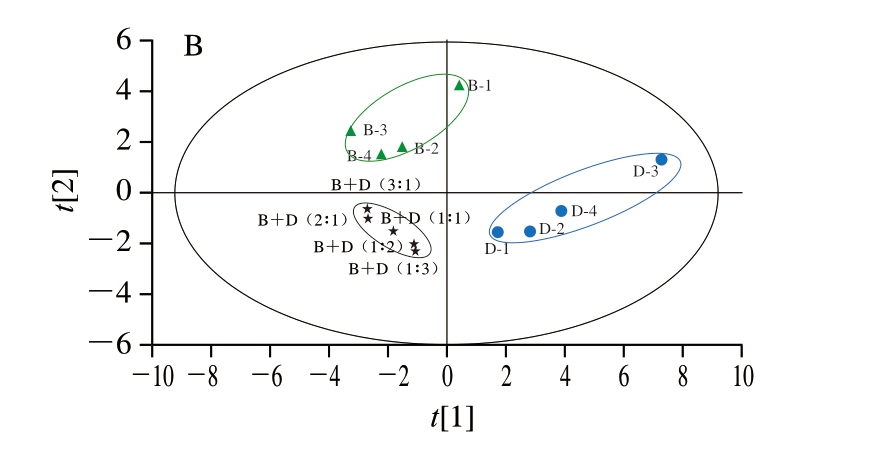
图4 羊肉、猪肉及混合样品(A)、牛肉、鸭肉及混合样品(B)的PCA得分图
Fig. 4 PCA score plots of mutton, pork and mixed samples (A) and beef, duck and mixed samples (B)
结合羊肉中猪肉、牛肉中鸭肉的掺伪量及对应的相似度,分别拟合绘制相似度与掺伪量的关系曲线,并得出对应的拟合方程分别为y1=![]() 0.986 6
0.986 6![]() 和y2=
和y2=![]() 0.984 0
0.984 0![]() =0.996 1),如图5所示。羊肉中猪肉、牛肉中鸭肉的相似度与掺伪量呈负相关(R2≥0.99),即掺伪量升高,相似度下降。因此,可根据指纹图谱相似度分析结合HCA及PCA对羊肉中猪肉、牛肉中鸭肉进行掺伪鉴别,并根据拟合方程进一步对掺伪量进行量化。
=0.996 1),如图5所示。羊肉中猪肉、牛肉中鸭肉的相似度与掺伪量呈负相关(R2≥0.99),即掺伪量升高,相似度下降。因此,可根据指纹图谱相似度分析结合HCA及PCA对羊肉中猪肉、牛肉中鸭肉进行掺伪鉴别,并根据拟合方程进一步对掺伪量进行量化。
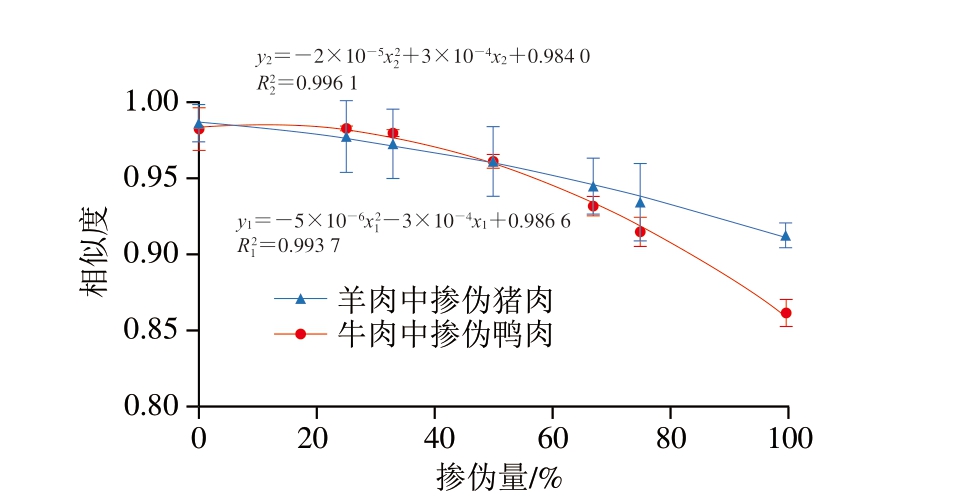
图5 相似度与掺伪量的关系曲线(n=3)
Fig. 5 Relationship curve between similarity and the amount of adulteration (n = 3)
样品检测和方法比对结果如表2所示,本研究方法与实时荧光PCR法的掺伪肉源鉴定结果一致,进一步使用本研究方法对各样品掺伪量进行分析,结果为34%~66%。
表2 市售未知羊肉、牛肉样品的方法比对结果
Table 2 Comparison of results of detection of adulteration by different methods in unknown samples

本研究方法检测结果掺伪肉源掺伪量/%市售羊肉样品1猪肉猪肉34市售羊肉样品2猪肉猪肉66市售牛肉样品1鸭肉鸭肉34市售牛肉样品2鸭肉鸭肉49市售牛肉样品3鸭肉鸭肉49样品实时荧光PCR法的掺伪肉源检测结果
现有研究表明,基于特征谱图采集与化学计量学分析相结合的肉类掺伪鉴别方法已取得显著进展。李倩等[34]采用表面解吸常压化学电离质谱法结合PCA可实现羊肉真伪快速鉴别;蒲科源等[35]采用蛋白质组学非靶向性质谱分析结合化学计量学,可对生熟牛肉掺伪进行初筛;方志娟等[36]基于基质辅助激光解吸电离飞行时间质谱技术,构建不同禽肉蛋白质分子指纹图谱,结合化学计量学分析对不同禽肉进行鉴别;Shi Zihe等[37]基于N-聚糖图谱,通过PCA对牛肉、鸡肉、猪肉、鸭肉和羊肉进行鉴别。虽然上述研究在目标分析成分方面与本研究存在差异,但特征谱图采集与化学计量学分析相结合可有效鉴别肉类掺伪这一核心结论与本研究结果高度一致,这进一步验证了该技术路线的科学性和普适性。
通过建立不同肉类样品的呈味核苷酸HPLC指纹图谱,羊肉和猪肉体系、牛肉和鸭肉体系均标定了19 个共有峰,前者羊肉和猪肉样品的相似度分别为0.971~0.999和0.900~0.920,后者牛肉和鸭肉样品的相似度分别为0.958~0.999和0.690~0.871,说明羊肉相比于猪肉、牛肉相比于鸭肉的呈味核苷酸成分存在较大差异;HCA和PCA结果从不同维度说明基于呈味核苷酸共有峰数据可以很好地区分羊肉、猪肉及掺入猪肉的羊肉、牛肉、鸭肉及掺入鸭肉的牛肉。
除掺伪鉴别外,本研究还通过拟合牛羊肉指纹图谱相似度与掺伪量的关系,得到对应的拟合方程(R2均≥0.99),从而根据某一样品的相似度对其掺伪量进行定量计算。对未知样品的检测结果显示,与实时荧光PCR法相比,本研究鉴定出的掺假肉源与其一致。后续研究会继续提高样品数量,丰富更多部位和种类肉的样品数据,以提高检测准确性,适应更多不同样品的掺伪鉴别和定量,并将该方法应用到大批量样品检测中,为我国肉类掺伪的管控提供数据储备和技术支持。
[1] 马小玉, 徐慧丽, 王正亮, 等. 基于微滴式数字PCR定量牛肉中的鸭源性成分[J]. 中国食品学报, 2024, 24(12): 343-350. DOI:10.16429/j.1009-7848.2024.12.031.
[2] 何东宇. 基于深度学习的添加剂作用下羊肉掺假移动端检测研究[D]. 石河子: 石河子大学, 2023. DOI:10.27332/d.cnki.gshzu.2023.000342.
[3] 杜丽丽. 羊肉产品中肉种来源的PCR检测方法研究[D]. 哈尔滨:哈尔滨商业大学, 2018. DOI:10.27787/d.cnki.ghrbs.2018.000066.
[4] 谭慧敏, 樊兰艳, 朱斌, 等. 南宁市市场肉类产品成分调查[J]. 现代食品, 2022, 28(18): 207-212. DOI:10.16736/j.cnki.cn41-1434/ts.2022.18.053.
[5] 刘敏, 李升升, 张艳, 等. 牛肉掺假鉴别技术研究进展[J].食品工业科技, 2023, 44(7): 477-489. DOI:10.13386/j.issn1002-0306.2022060044.
[6] LU Y X, ZHAI R, CHU Z Y, et al. LC-MS/MS-based quantitative method and metrological traceability technology for measuring components of animal origin in beef and lamb and their products[J]. Food Chemistry, 2025, 464: 141600. DOI:10.1016/j.foodchem.2024.141600.
[7] 王桐萱, 于志军, 刘敬泽. 人类红肉过敏的发生原因和防治概述[J].生物学教学, 2020, 45(12): 55-56.
[8] 路宇轩, 翟睿, 吴帆, 等. 肉类掺假检测方法及研究进展[J]. 计量学报, 2023, 44(6): 1000-1008. DOI:10.3969/j.issn.1000-1158.2023.06.24.
[9] 刘达玉, 肖龙泉, 李云成, 等. 羊肉的鉴别方法及其应用现状[J]. 食品工程, 2019(1): 1-3; 21. DOI:10.3969/j.issn.1673-6044.2019.01.001.
[10] 赵静远, 张俊芹, 孙梅, 等. 基于高光谱成像的羊肉掺假可视化无损定量检测[J]. 食品与机械, 2022, 38(10): 61-68. DOI:10.13652/j.spjx.1003.5788.2022.90174.
[11] 马永征, 马冬, 白娣斯, 等. 免疫学检测肉类制品掺假研究进展[J].肉类研究, 2012, 26(9): 26-29. DOI:10.7506/rlyj1001-8123-201209007.
[12] 施姿鹤. 肉中蛋白质N-糖基化分析及其在常见肉类掺假鉴别中的应用[D]. 南京: 南京农业大学, 2020. DOI:10.27244/d.cnki.gnjnu.2020.000424.
[13] 康超娣, 王守伟, 张颖颖, 等. 液相色谱-串联质谱法对牛肉中掺假成分的相对定量分析[J]. 食品科学, 2022, 43(4): 270-276.DOI:10.7506/spkx1002-6630-20210410-135.
[14] 于梓洇, 吴冬蕊, 孔佑梦, 等. 美拉德反应对肉类风味物质形成影响的研究进展[J]. 中国调味品, 2024, 49(12): 209-214. DOI:10.3969/j.issn.1000-9973.2024.12.033.
[15] RAMALINGAM V, SONG Z, HWANG I. The potential role of secondary metabolites in modulating the flavor and taste of the meat[J].Food Research International, 2019, 122: 174-182. DOI:10.1016/j.foodres.2019.04.007.
[16] 张莺莺, 刁玉段, 张佳杰, 等. 风味前体物质在肉类风味形成中的作用及其影响因素[J]. 上海畜牧兽医通讯, 2024(4): 1-9; 89.DOI:10.14170/j.cnki.cn31-1278/s.2024.04.008.
[17] 周泓畅. 鸡肝-鱼骨泥呈味肽的制备及其呈鲜机制研究[D]. 镇江: 江苏大学, 2023. DOI:10.27170/d.cnki.gjsuu.2023.001398.
[18] 陈柔含, 张维谊, 马颖清, 等. 高效液相色谱法同时测定畜禽产品中9 种呈味核苷酸方法的建立和应用[J]. 农产品质量与安全, 2024(3):41-48. DOI:10.3969/j.issn.1674-8255.2024.03.006.
[19] TERASAKI M, KAJIKAWA M, FUJITA E, et al. Studies on the flavor of meats[J]. Agricultural and Biological Chemistry, 1965, 29(3): 208-215. DOI:10.1080/00021369.1965.10858377.
[20] ZHUO Z H, XU D P, LI Y P, et al. Fingerprint analysis of Zanthoxylum armatum DC. by HPLC[J]. Journal of Food Composition and Analysis,2021, 96: 103736. DOI:10.1016/j.jfca.2020.103736.
[21] HERNADI E, ROHAETI E, RAFI M, et al. HPLC fingerprinting coupled with linear discriminant analysis for the detection of adulteration in Orthosiphon aristatus[J]. Journal of Liquid Chromatography & Related Technologies, 2019, 42(15/16): 513-520.DOI:10.1080/10826076.2019.1629956.
[22] AMINIANFAR A, FATEMI M H, AZIMI F. Comprehensive characterization of volatile compounds in Iranian black teas using chemometric analysis of GC-MS fingerprints[J]. Food Chemistry: X,2024, 24: 101859. DOI:10.1016/j.fochx.2024.101859.
[23] YANG L, DAI L, QIN W H, et al. Chemical constituent characterization and determination of Quisqualis fructus based on UPLC-Q-TOF-MS and HPLC combined with fingerprint and chemometric analysis[J]. Frontiers in Plant Science, 2024, 15:1418480. DOI:10.3389/fpls.2024.1418480.
[24] 康帅, 任晓镤, 彭增起. 羊肉的产地溯源和鉴别技术研究进展[J]. 肉类研究, 2023, 37(4): 48-53. DOI:10.7506/rlyj1001-8123-20230206-011.
[25] 郭瑛, 张秋兰, 王勇, 等. 化学计量学在食品质量控制和食品安全机理研究中的应用[C]//中国化学会第14届全国计算(机)化学学术会议暨分子模拟国际论坛会议手册. 北京: 中国化学会, 2017: 64.
[26] 黎琪, 李晓敏, 姜德铭, 等. 高效液相色谱法检测熟制猪肉中呈味核苷酸[J]. 肉类研究, 2022, 36(3): 26-31. DOI:10.7506/rlyj1001-8123-20211213-237.
[27] 苏改兰, 樊丛照, 邱远金, 等. 基于指标成分及指纹图谱多模式识别的不同品种红花质量评价[J]. 中国现代中药, 2024, 26(6): 989-996.DOI:10.13313/j.issn.1673-4890.20231031001.
[28] 翟红伟, 赵玉婷, 林露, 等. 指纹图谱和多成分定量结合化学模式识别法评价清肺达原颗粒质量[J]. 亚太传统医药, 2024, 20(8): 43-48.DOI:10.11954/ytctyy.202408009.
[29] 国家市场监督管理总局, 国家标准化管理委员会. 常见畜禽动物源性成分检测方法 实时荧光PCR法: GB/T 38164—2019[S]. 北京:中国标准出版社, 2019.
[30] 毕继全, 王希通, 陈林伟, 等. 萌芽黑青稞喷干粉的主要成分测定及HPLC指纹图谱的建立[J]. 中国食品学报, 2022, 22(9): 293-303.DOI:10.16429/j.1009-7848.2022.09.031.
[31] 耿洁. 中药指纹图谱的相似度评价方法[D]. 太原: 山西大学, 2012.
[32] 刘永锁, 孟庆华, 蒋淑敏, 等. 相似系统理论用于中药色谱指纹图谱的相似度评价[J]. 色谱, 2005, 23(2): 158-163. DOI:10.3321/j.issn:1000-8713.2005.02.009.
[33] 徐妍, 杨华蕊, 杨永寿, 等. 中药指纹图谱研究现状及展望[J].世界最新医学信息文摘, 2018, 18(76): 91-94. DOI:10.19613/j.cnki.1671-3141.2018.76.040.
[34] 李倩, 王姜, 陈焕文, 等. 表面解吸常压化学电离质谱法快速鉴别羊肉真伪[J]. 质谱学报, 2014, 35(6): 502-508. DOI:10.7538/zpxb.youxian.2014.0022.
[35] 蒲科源, 丘嘉敏, 刘柏霖, 等. 蛋白质组学非靶向性质谱分析结合化学计量学在牛肉掺假初筛中的应用[J]. 食品与发酵工业, 2023,49(3): 290-295. DOI:10.13995/j.cnki.11-1802/ts.031690.
[36] 方志娟, 李晓芹, 张雪婧, 等. MALDI-TOF MS在不同禽肉动物源性成分检测中的研究[J]. 安徽农业科学, 2023, 51(7): 189-192; 195.DOI:10.3969/j.issn.0517-6611.2023.07.043.
[37] SHI Z H, YIN B R, LI Y Q, et al. N-Glycan profile as a tool in qualitative and quantitative analysis of meat adulteration[J]. Journal of Agricultural and Food Chemistry, 2019, 67(37): 10543-10551.DOI:10.1021/acs.jafc.9b03756.