周光宏(1960—)(ORCID: 0000-0002-8960-2141),男,教授,博士,研究方向为肉品加工与质量控制。E-mail: guanghong.zhou@hotmail.com
王冲(1990—)(ORCID: 0000-0002-2715-4718),男,副教授,博士,研究方向为肉品加工与质量控制。E-mail: chong.wang@njau.edu.cn
Effect of Transportation under Different Temperature Conditions on the Sales Quality of Hot-Boned Pork in Summer
宋歌, 王晓明, 王嘉昕, 等. 不同运输温度对热鲜猪肉夏季销售品质的影响[J]. 肉类研究, 2026, 40(4): 54-60.DOI:10.7506/rlyj1001-8123-20250506-138. http://www.rlyj.net.cn
SONG Ge, WANG Xiaoming, WANG Jiaxin, et al. Effect of transportation under different temperature conditions on the sales quality of hot-boned pork in summer[J]. Meat Research, 2026, 40(4): 54-60. (in Chinese with English abstract)DOI:10.7506/rlyj1001-8123-20250506-138. http://www.rlyj.net.cn
热鲜肉是指屠宰后未经充分人工冷却处理的肉类产品,通常于清晨宰杀后直接上市销售[1]。受消费习惯影响,我国南方地区消费者仍普遍倾向于选购热鲜肉[2]。由于热鲜肉特殊的生产加工方式、较高水分含量及丰富营养特性,其品质对温度变化具有高度敏感性[3]。在贮藏、运输和零售过程中,温度波动易引起热鲜肉发生品质劣变[4-5]。夏季气温升高时,肉品质量问题尤为突出。高温环境可加速猪胴体内生化反应速率并促进微生物生长繁殖,导致肉品色泽、口感及风味等感官特性发生变化,影响肉品的品质和食用安全性[6-7]。其中,肉色作为重要的感官评价指标,直接影响消费者的购买行为。因此,在夏季高温条件下维持肉色稳定性、延缓肉品内源性生化反应及抑制微生物生长成为热鲜肉加工和销售环节亟待解决的关键问题。
适宜的温度控制能有效提高肉品品质并延长其货架期[8-9]。Wang Su等[10]研究表明,冷链物流全程低温控制可有效减少碱性物质生成、抑制微生物活动并延缓猪肉pH值升高。林珩迅等[11]研究表明,冰温环境可有效抑制猪肉品质劣变进程。刘婷婷等[12]研究表明,低于7 ℃的环境温度有利于延缓冷鲜猪肉优势腐败微生物增殖。然而,低温可能对肉品品质(尤其是肉色)产生负面影响。虽然冷鲜肉嫩度优于热鲜肉,其色泽相对较浅。在冷冻过程中,肌红蛋白会因细胞结构破坏而发生变性,加速氧化为高铁肌红蛋白,导致肉品红度值(a*)下降[13]。-20 ℃贮藏肉品解冻后,脂质氧化速率加快并伴随表面颜色不均匀现象[14]。
近年来,通过控制运输温度维持猪肉品质的技术已在生产加工环节有所应用。然而,针对夏季热鲜猪肉运输至销售端的品质变化规律仍缺乏系统性定量研究,难以为实际购销活动提供理论指导。因此,本研究以宰后热鲜肉为研究对象,通过测定其色泽、菌落总数、氧合肌红蛋白(oxymyoglobin,OxyMb)相对含量、糖原含量及水分分布等指标,系统解析不同运输温度对夏季销售期间热鲜肉品质的影响。
猪胴体取自广东某屠宰场,选用同一养殖场饲养的三元猪,体质量约80 kg,经检疫检验合格后集中屠宰。
平板计数琼脂培养基 青岛高科技工业园海博生物技术有限公司;蛋白胨 北京奥博星生物技术有限责任公司;硫酸 南京化学试剂股份有限公司;三氯甲烷上海凌峰化学试剂有限公司;糖原含量检测试剂盒、ATP含量检测试剂盒 北京索莱宝科技有限公司。
PL601-L电子天平 瑞士梅特勒-托利多有限公司;CR-400色差仪 日本柯尼卡美能达公司;Testo205便携式pH计 德图仪器国际贸易(上海)有限公司;BCM-1600A超净工作台 苏州安泰空气技术有限公司;ICP 260低温培养箱 德国美墨尔特公司;SIM-F124制冰机 日本三洋公司;MUL-9000系列纯水机 美国Millipore公司;SpectraMax M2e低温高速离心机 德国Eppendorf公司;WH-2微型旋涡混合仪上海沪西分析仪器厂有限公司;PQ001-12-040V低场核磁共振成像分析仪 苏州纽迈分析仪器股份有限公司;NanoDrop ND-2000微量紫外分光光度计 美国赛默飞生物公司。
1.3.1 样品制备
本实验于7—8月进行,在不同温度条件下运输猪胴体,对照组(Con)采用敞篷车运输,实验组采用冷链车运输,运输温度分别为5(T1)、10(T2)、15 ℃(T3),运输全程往返里程150 km,在运输终点处取15 条背最长肌肉样,立即运回实验室。每条背最长肌样品分割为若干10 cm×10 cm×5 cm肉块,置于托盘中,模拟广东地区夏季市场销售环境进行贮藏。市场调研显示,个体经营户通常将热鲜肉于凌晨3时左右运输至市场并开始分割,并于下午5时前完成销售。因此,分别在贮藏0、3、6、9、12 h时取样,测定其色泽、菌落总数、OxyMb相对含量、糖原含量、ATP含量和水分分布。
1.3.2 色泽测定
采用色差仪测定样品的亮度值(L*)和a*。测定前使用白色标准板校正仪器,每个肉样选取3~5 个测定点,取平均值。
1.3.3 菌落总数测定
参照GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数》测定样品的菌落总数。
1.3.4 OxyMb相对含量测定
参考Viriyarattanasak等[15]的方法并稍作修改,取5 g样品,加入25 mL磷酸缓沖液(0.04 mol/L、pH 6.8),于匀浆机中10 000 r/min均质25 s(室温),冰水浴静置1 h,4 ℃、3 500 r/min离心20 min,取上清液过滤,采用紫外分光光度计分别测定525、545、565、572 nm波长处的吸光度,OxyMb相对含量按下式计算:
式中:R1=A572 nm/A525 nm;R2=A565 nm/A525 nm;R3=A545 nm/A525 nm。
1.3.5 糖原、ATP含量测定
糖原、ATP含量按试剂盒说明书进行测定。
1.3.6 水分分布测定
参照Han Minyi等[16]的方法并根据实际情况稍作修改。切取(2.00±0.05)g猪背最长肌肉样,置于低场核磁共振成像分析仪专用样品管中,采用CPMG(Carr-Purcell-Meiboom-Gill)脉冲序列进行测定。测定参数:温度32 ℃、采样频率100 kHz、回波数5 000,每次重复扫描16 次。
实验数据采用SPSS 27软件进行统计分析,结果以平均值±标准差表示。通过单因素方差分析与Duncan多重比较进行显著性分析,利用GraphPad Prism 7.00软件绘图。
肉色作为猪肉品质的关键评价指标之一,其变化直接影响产品的新鲜度等级和消费者接受度[17]。如图1A所示,随着贮藏时间的延长,a*呈现持续上升趋势,这可能是由于宰后猪肉中的肌红蛋白与氧气结合形成OxyMb,促使肉色由暗红转变为鲜红色[18-19]。值得注意的是,由于样品在运输阶段经历了150 km不同温度条件的处理,导致各组a*在贮藏初期即存在显著差异(P<0.05)。具体而言,15 ℃运输组a*在整个贮藏期间始终显著高于其他组(P<0.05),经12 h贮藏后,a*较敞篷运输组、5 ℃运输组和10 ℃运输组分别提高13.71%、7.29%和6.36%,表明适度提高环境温度可有效促进肌红蛋白向OxyMb的转化速率,从而有效改善肉品色泽,这一发现与金鑫等[20]关于温度对热鲜肉色泽的影响结果具有一致性,进一步验证了温度调控对热鲜肉色泽形成和改善的重要作用。另外,贮藏结束时,敞篷运输组a*显著低于其他组(P<0.05),这可能是由于较高的环境温度干扰了肌红蛋白的氧化转化,反而抑制了理想肉色的形成,肉品a*相对较低。
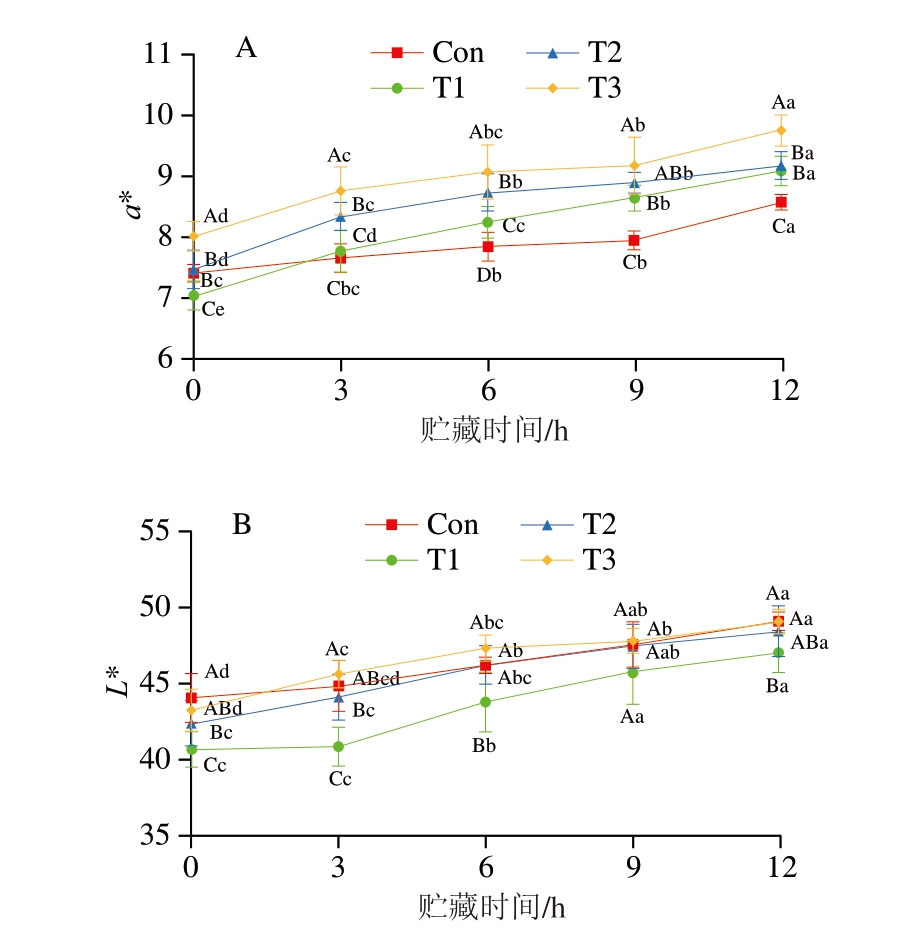
图1 不同运输温度与贮藏时间对猪肉a*(A)和L*(B)的影响
Fig. 1 Effect of transportation temperature and storage time on the a* (A) and brightness value (B) of pork
小写字母不同表示不同贮藏时间之间差异显著(P<0.05);大写字母不同表示不同运输条件之间差异显著(P<0.05)。图2、3同。
如图1B所示,贮藏期间样品L*呈现显著上升趋势(P<0.05)。随着贮藏时间的延长,猪肉表面渗出水分导致光学反射特性发生变化,引起L*升高[21]。值得注意的是,15 ℃运输组与敞篷运输组L*无显著差异(P>0.05),但两者均显著高于5 ℃运输组(P<0.05),这可能是由于运输与贮藏过程的持续高温加速了猪肉肌纤维蛋白降解,导致猪肉持水力下降[22]。
微生物通过分解肉中的蛋白质、脂肪和糖类等成分,导致肉品腐败变质[23-24]。如图2所示,随着贮藏时间的延长,各组菌落总数均呈现显著上升趋势(P<0.05)。在不同温度条件下经150 km运输后,各组菌落总数在贮藏初期即存在显著差异(P<0.05)。贮藏过程中,敞篷运输组菌落总数均显著高于各温控运输组(P<0.05),贮藏结束时,其菌落总数较5、10、15 ℃运输组分别增加22.51%、18.07%、14.23%,这可能是由于敞篷运输过程中猪胴体直接暴露于外界环境,空气中的灰尘、微生物和污染物附着导致猪胴体表面微生物数量增加,同时较高的环境温度为微生物生长繁殖提供有利条件。根据2073/2005/EC《食品微生物标准》规定,猪胴体菌落总数的满意水平为4.0(lg(CFU/cm2)),可接受水平为5.0((lg(CFU/cm2))[25]。贮藏结束时,相较于各温控运输组,敞篷运输组菌落总数为5.17(lg(CFU/cm2)),已超出可接受水平;5 ℃运输组菌落总数为4.22(lg(CFU/cm2)),虽未超过可接受阈值,但已不在满意水平。综上,温控运输可有效抑制微生物增殖,延缓肉品腐败进程。
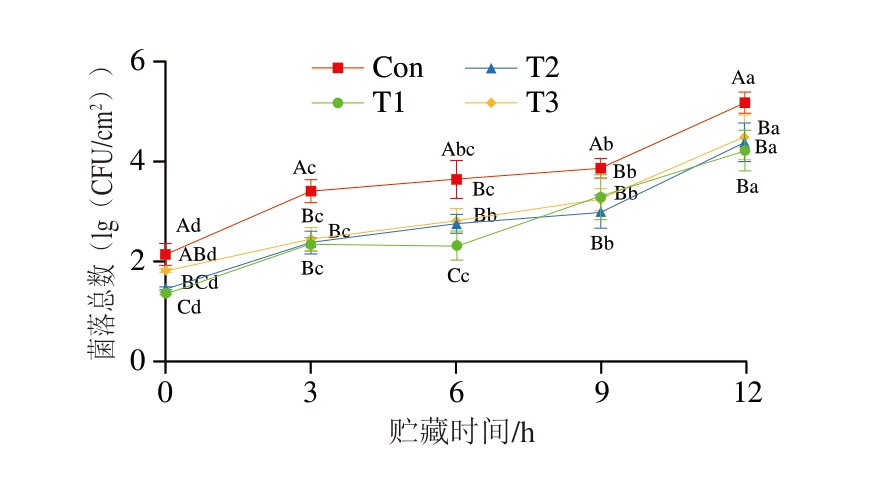
图2 不同运输温度与贮藏时间对猪肉菌落总数的影响
Fig. 2 Effect of transportation temperature and storage time on the total bacterial count of pork
肉色作为猪肉品质的重要指标,主要由肌红蛋白含量及其氧化还原状态决定[26]。如图3所示,随着贮藏时间的延长,各组OxyMb相对含量均呈波动上升趋势。在不同温度条件下经150 km运输后,各组OxyMb相对含量在贮藏初期即存在显著差异(P<0.05)。贮藏3 h时,15 ℃运输组样品OxyMb相对含量显著高于5 ℃与10 ℃运输组(P<0.05);贮藏9 h时,各温控运输组OxyMb相对含量均高于敞篷运输组;贮藏12 h时,15 ℃运输组OxyMb相对含量显著高于敞篷运输组和5 ℃运输组(P<0.05),与10 ℃运输组无显著差异(P>0.05)。温度可控条件下,运输温度越高,肌红蛋白向OxyMb转化速率越快,与Mir等[27]的研究结果一致。值得注意的是,敞篷运输条件下,OxyMb相对含量始终维持在较低水平,推测可能是由于贮藏期间需氧微生物的快速繁殖降低了肉品表面的氧分压,从而加快了OxyMb向高铁肌红蛋白的转化过程[28]。
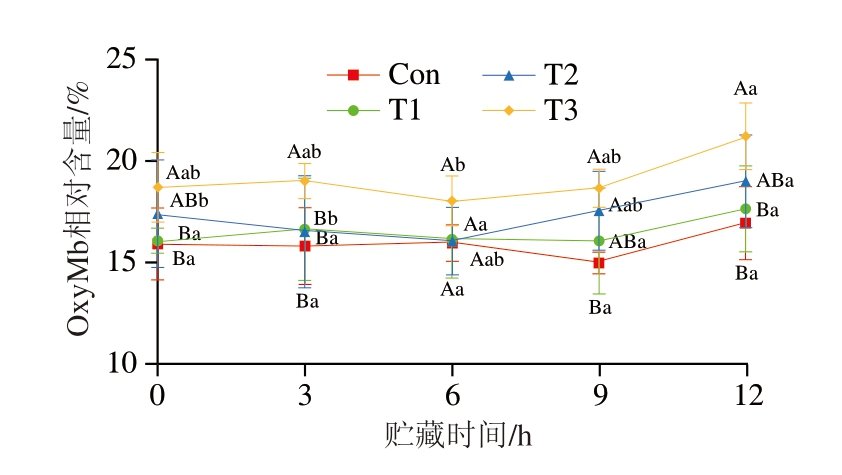
图3 不同运输温度与贮藏时间对猪肉OxyMb相对含量的影响
Fig. 3 Effect of transportation temperature and storage time on the OxyMb relative content of pork
糖原作为动物体内主要的能量储存物质,主要分布于肌肉组织中。宰后由于血液供应中断,肌肉组织转为无氧代谢状态,糖原成为其主要能量来源[29]。如图4所示,随着贮藏时间的延长,各组糖原含量均呈现持续下降趋势并逐渐趋于一致,与邹波[30]的研究结果一致。不同温度条件下经150 km运输后,各组糖原含量在贮藏初期即存在显著差异(P<0.05)。贮藏3 h时,敞篷运输组糖原含量显著低于5 ℃和10 ℃运输组(P<0.05);贮藏6 h时,10 ℃运输组糖原含量显著高于敞篷运输组与5 ℃运输组(P<0.05),分别比敞篷运输组、5 ℃运输组、15 ℃运输组高19.04%、12.78%、8.37%。运输与贮藏过程中的持续高温可显著增强糖酵解酶活性,从而加速糖原降解为乳酸。值得注意的是,贮藏期间5 ℃运输组糖原含量在贮藏期间迅速下降,可能与运输至销售环节的温度骤升有关,这种温度波动会显著促进糖酵解反应进程,进而加速糖原消耗,这与Wang Su等[10]的研究结果较相对为一致。
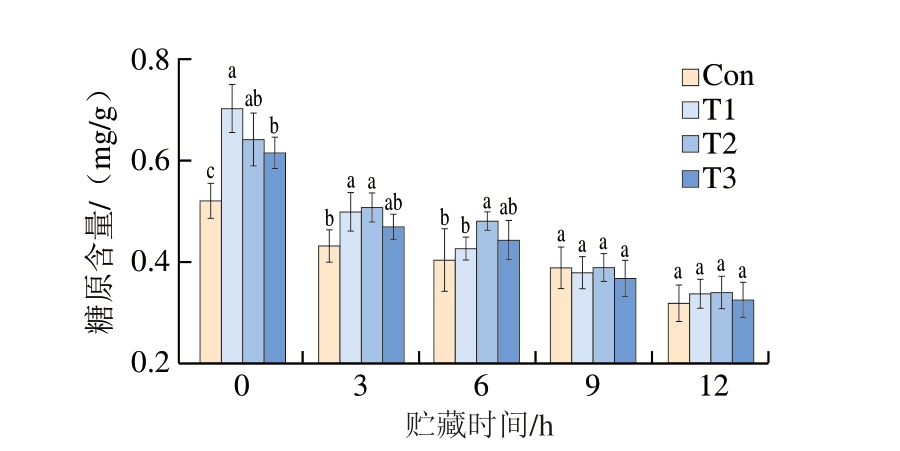
图4 不同运输条件对猪肉贮藏期间糖原含量的影响
Fig. 4 Effects of different transportation conditions on the glycogen content of pork during storage
小写字母不同表示不同运输条件之间差异显著(P<0.05)。图5同。
ATP作为能量代谢的重要物质,其含量水平可准确反映机体的生理状态、营养水平及应激反应程度等,并直接影响肉品的嫩度、风味特性、货架期及感官品质。合理调制宰后和贮藏过程中ATP的降解过程有助于提高猪肉的整体品质[31]。如图5所示,随着贮藏时间的延长,各组ATP含量均呈现持续下降趋势并逐渐趋于一致,这一现象可能源于宰后猪胴体糖酵解途径产生的ATP有限,在肌肉收缩和酶促反应过程中被迅速消耗直至耗尽[32]。不同运输温度对ATP代谢过程具有显著影响(P<0.05)。其中,5 ℃运输组ATP含量呈现快速下降趋势。一方面,可能是由于运输至销售环节的温度骤升促进内源酶活性增强,导致ATP降解速率升高,该结果与Chen Bohan等[33]的研究结果一致;另一方面,温度波动加速糖原分解,加剧ATP消耗。值得注意的是,贮藏3、6 h时,10 ℃运输组ATP含量均显著高于其他运输组(P<0.05),其中贮藏6 h时,ATP含量分别较敞篷运输组、5 ℃运输组、15 ℃运输组高34.45%、28.35%、31.75%,表明10 ℃运输能有效延缓贮藏期间ATP的降解。
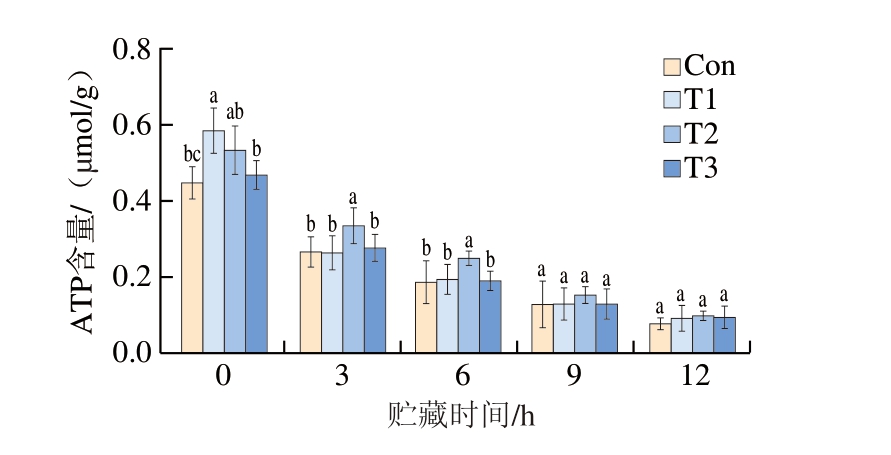
图5 不同运输条件对猪肉贮藏期间ATP含量的影响
Fig. 5 Effect of different transportation conditions on the ATP content of pork during storage
猪肉中主要存在3 个水分信号峰,分别为结合水(T21,0.01~10 ms)、不易流动水(T22,10~100 ms)、自由水(T23,100~1 000 ms)[34]。各组猪肉样品中水分的横向弛豫时间曲线如图6所示。
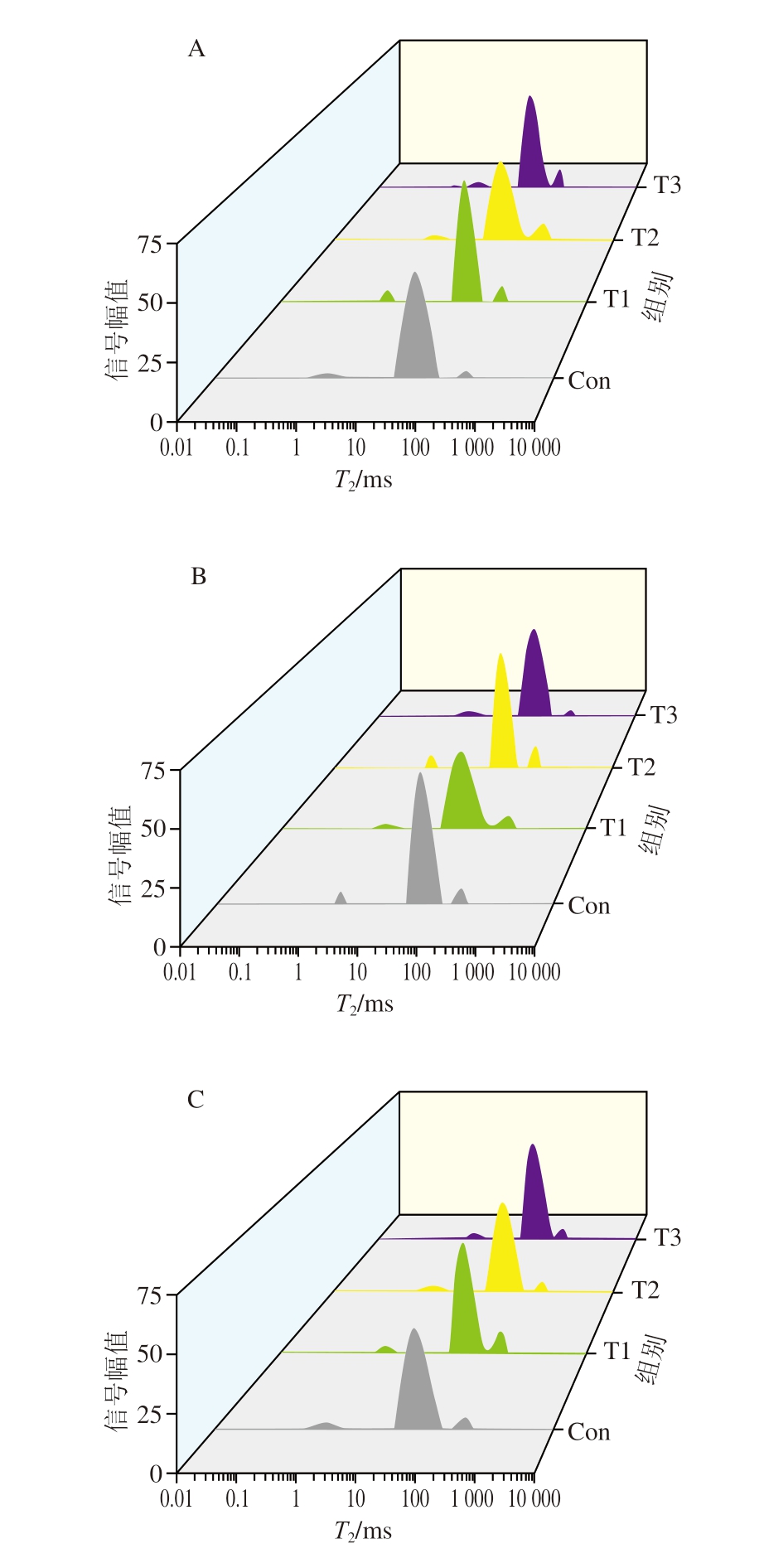
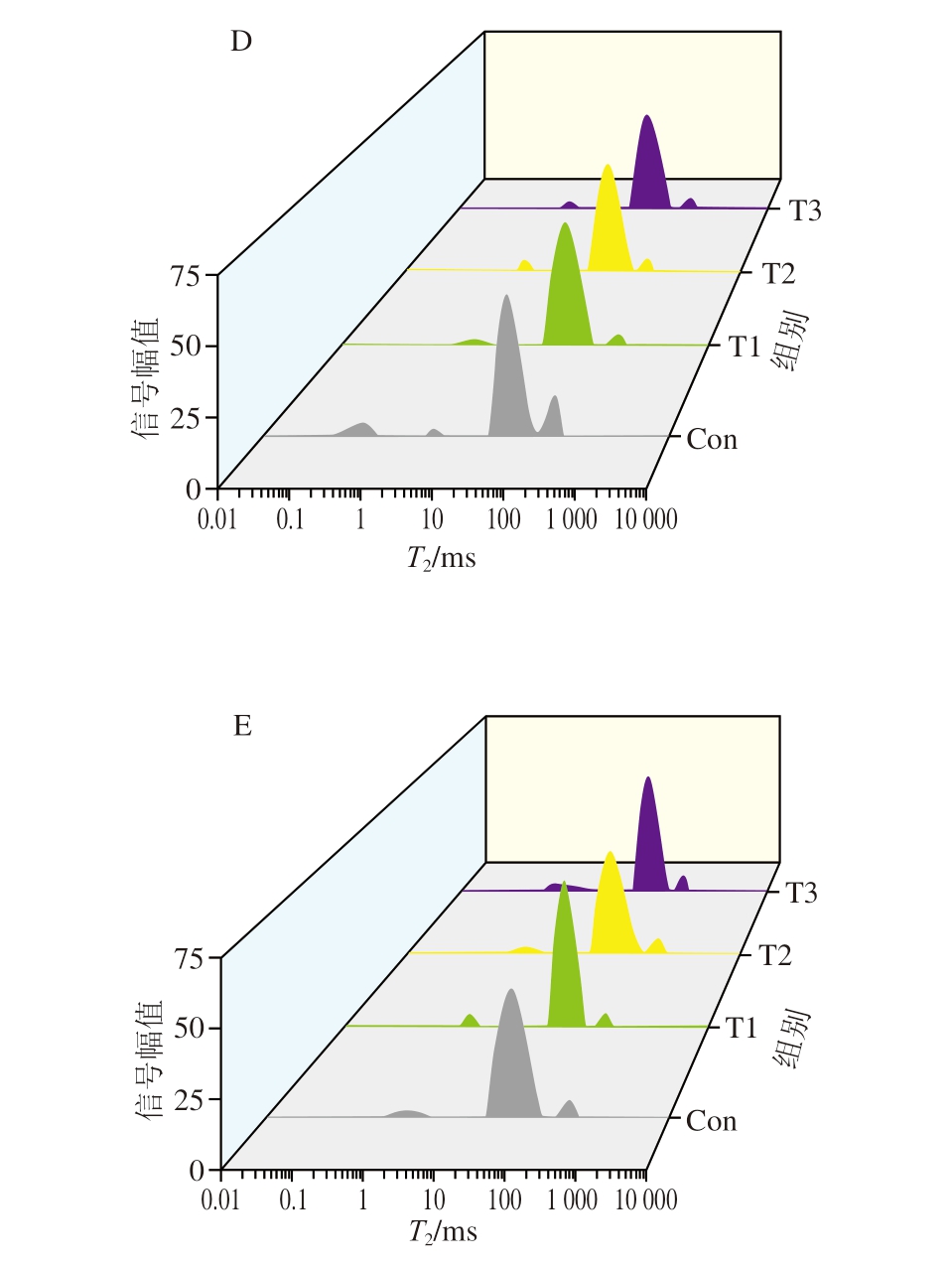
图6 敞篷运输组与5、10、15 ℃运输组猪肉贮藏0(A)、3(B)、6(C)、9(D)、12 h(E)的水分T2曲线
Fig. 6 Transverse relaxation time curves of moisture in the open-air, 5,10, and 15 ℃ transportation groups after 0 (A), 3 (B), 6 (C), 9 (D), and 12 h of storage (E)
P21、P22和P23分别为结合水、不易流动水、自由水T2曲线峰面积与总水分峰面积比值,表示各状态水分的相对含量。如表1所示,10 ℃运输条件下,不易流动水相对含量随贮藏时间延长逐渐下降,自由水相对含量相应增加,表明贮藏过程中存在水分状态转化现象。相比之下,其他运输组自由水相对含量呈现递减趋势,这可能是由于较高温度会加速自由水蒸腾损失[3]。同时,温度波动也可能改变水分状态与分布,导致自由水相对含量降低[10]。值得注意的是,15 ℃运输组结合水相对含量变化显著(P<0.05),其值随贮藏时间延长呈波动下降趋势且在贮藏结束时显著低于其他运输组(P<0.05),可能是由于运输与贮藏过程中,持续的高温环境导致的肌纤维收缩和蛋白质表面疏水性增强弱化了其水合能力,促使结合水向游离状态转化,最终导致持水力下降[35]。
表1 不同运输条件对猪肉贮藏期间水分分布的影响
Table 1 Effect of different transportation conditions on the moisture distribution in pork during storage
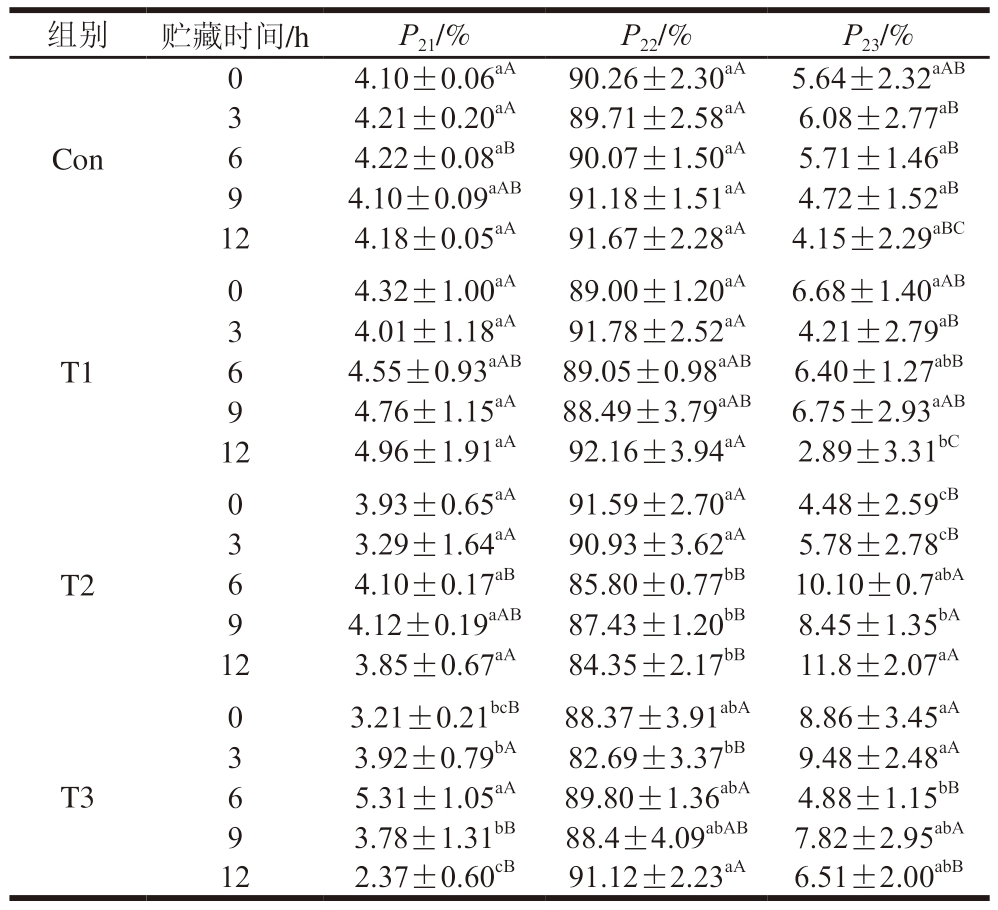
注:同列小写字母不同表示不同贮藏时间之间差异显著(P<0.05);同列大写字母不同表示不同运输条件之间差异显著(P<0.05)。
组别贮藏时间/hP21/%P22/%P23/%Con 04.10±0.06aA90.26±2.30aA5.64±2.32aAB 34.21±0.20aA89.71±2.58aA6.08±2.77aB 64.22±0.08aB90.07±1.50aA5.71±1.46aB 94.10±0.09aAB91.18±1.51aA4.72±1.52aB 124.18±0.05aA91.67±2.28aA4.15±2.29aBC T1 04.32±1.00aA89.00±1.20aA6.68±1.40aAB 34.01±1.18aA91.78±2.52aA4.21±2.79aB 64.55±0.93aAB89.05±0.98aAB6.40±1.27abB 94.76±1.15aA88.49±3.79aAB6.75±2.93aAB 124.96±1.91aA92.16±3.94aA2.89±3.31bC T2 03.93±0.65aA91.59±2.70aA4.48±2.59cB 33.29±1.64aA90.93±3.62aA5.78±2.78cB 64.10±0.17aB85.80±0.77bB10.10±0.7abA 94.12±0.19aAB87.43±1.20bB8.45±1.35bA 123.85±0.67aA84.35±2.17bB11.8±2.07aA 03.21±0.21bcB88.37±3.91abA8.86±3.45aA 33.92±0.79bA82.69±3.37bB9.48±2.48aA 65.31±1.05aA89.80±1.36abA4.88±1.15bB 93.78±1.31bB88.4±4.09abAB7.82±2.95abA 122.37±0.60cB91.12±2.23aA6.51±2.00abB T3
如图7所示,猪肉a*与OxyMb相对含量呈极显著正相关(P<0.01),证实OxyMb的积累是促进肉色红度提升的关键因素,该结果与贮藏前期15 ℃运输组a*和OxyMb相对含量均高于敞篷运输组与5 ℃运输组的结果相一致。猪肉L*与菌落总数也呈极显著正相关(P<0.01),揭示贮藏期间微生物快速生长,通过分解蛋白质改变表面光学特性,其代谢活动导致的水分重分布可能是L*升高的内在机制,敞篷运输组L*与菌落总数在贮藏期间普遍高于5 ℃运输组与10 ℃运输组的结果与相关性结果一致。猪肉ATP含量与糖原含量呈极显著正相关(P<0.01),可能是由于宰后肌肉中糖原作为无氧糖酵解底物对维持ATP水平的重要作用,充足糖原可延缓能量耗竭进程。
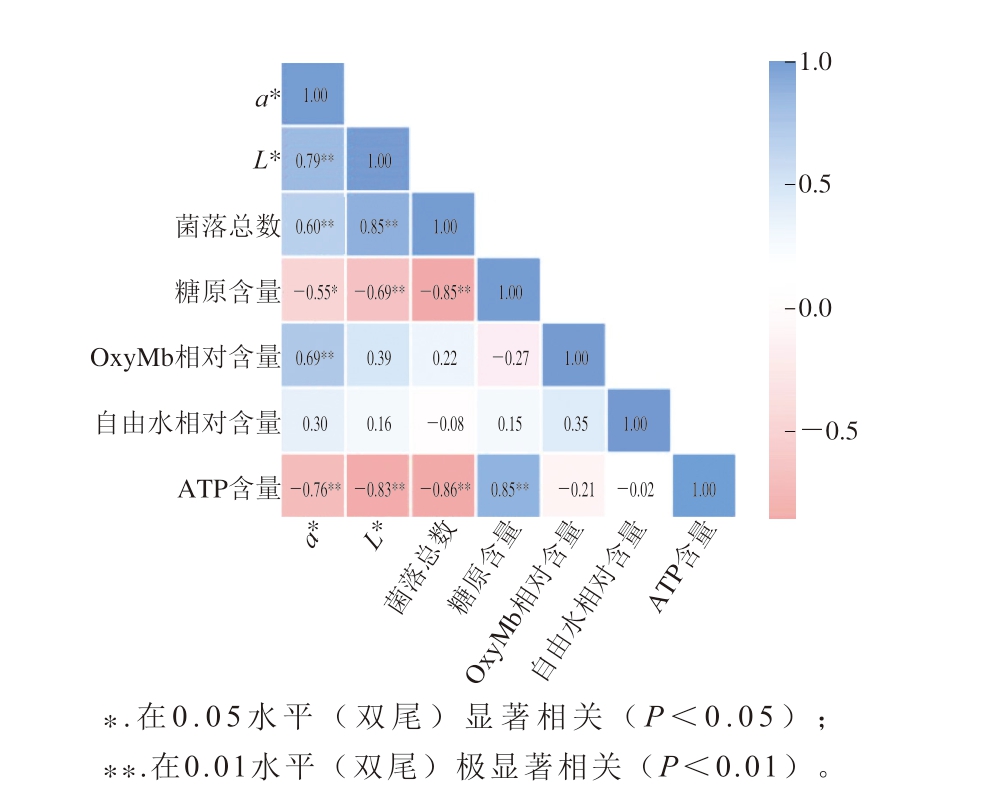
图7 猪肉品质指标相关性分析
Fig. 7 Correlation analysis among quality indicators of pork
随着贮藏时间延长,热鲜肉a*和L*均呈现显著上升趋势(P<0.05)。在温控运输条件下,a*随运输温度升高而显著升高(P<0.05)。4 种运输条件下,菌落总数均显著增加(P<0.05),其中敞篷运输组菌落总数最先超出可接受阈值。贮藏结束时,10 ℃和15 ℃运输组OxyMb相对含量无显著差异(P>0.05),但15 ℃运输组结合水相对含量显著低于10 ℃运输组(P<0.05)。贮藏期间,热鲜肉糖原含量及ATP含量均明显降低。贮藏6 h时,10 ℃运输组糖原含量较敞篷运输组、5 ℃运输组和15 ℃运输组分别高19.04%、12.78%和8.37%,ATP含量分别提升34.45%、28.35%和31.75%。综上,10 ℃运输条件能有效延缓糖原分解和ATP降解、抑制微生物生长,进而维持热鲜肉在贮藏期间的品质稳定性,同时有助于保持较好的肉色,是适用于夏季热鲜肉的较佳运输方式。
[1] 张德权, 侯成立. 热鲜肉与冷却肉品质差异之管见[J]. 肉类研究,2020, 34(5): 83-90. DOI:10.7506/rlyj1001-8123-20200220-041.
[2] 徐志方. 热鲜肉屠宰过程中PSE肉产生原因分析及解决办法探讨[J]. 肉类工业, 2018(8): 55-57. DOI:10.3969/j.issn.1008-5467.2018.08.016.
[3] JI C, WU B, GAO S, et al. Impact of roasting time on the color,protein, water distribution and key volatile compounds of pork[J].Journal of Food Composition and Analysis, 2024, 136: 106787.DOI:10.1016/j.jfca.2024.106787.
[4] 孙京新, 黄明. 我国猪肉加工产业现状、存在的问题及可持续发展建议[J]. 养猪, 2015(3): 62-64. DOI:10.13257/j.cnki.21-1104/s.2015.03.039.
[5] 苗旺, 陆欢然, 孔凡春. 国内猪肉鲜销产品及工艺分析-热鲜肉与冷却肉[J]. 农产品加工, 2022(16): 84-87. DOI:10.16693/j.cnki.1671-9646(X).2022.08.051.
[6] XU Y Q, LENG D M, LI X, et al. Effects of different electrostatic field intensities assisted controlled freezing point storage on water holding capacity of fresh meat during the early postmortem period[J]. Food Chemistry, 2024, 439: 138096. DOI:10.1016/j.foodchem.2023.138096.
[7] HUANG M M, WANG J M, ZHUANG H, et al. Effect of in-package high voltage dielectric barrier discharge on microbiological, color and oxidation properties of pork in modified atmosphere packaging during storage[J]. Meat Science, 2019, 149: 107-113. DOI:10.1016/j.meatsci.2018.11.016.
[8] KAALE L D, EIKEVIK T M, RUSTAD T, et al. Superchilling of food:a review[J]. Journal of Food Engineering, 2011, 107(2): 141-146.DOI:10.1016/j.jfoodeng.2011.06.004.
[9] LIU D S, LIANG L, XIA W S, et al. Biochemical and physical changes of grass carp (Ctenopharyngodon idella) fillets stored at -3 and 0 ℃[J]. Food Chemistry, 2013, 140(1/2): 105-114. DOI:10.1016/j.foodchem.2013.02.034.
[10] WANG S, ZHANG D Q, YANG Q F, et al. Effects of different cold chain logistics modes on the quality and bacterial community succession of fresh pork[J]. Meat Science, 2024, 213: 109502.DOI:10.1016/j.meatsci.2024.109502.
[11] 林珩迅, 何兴兴, 张成云, 等. 冰温贮藏对猪肉宰后品质及糖酵解途径相关酶活性的影响[J]. 食品科学, 2022, 43(3): 187-193.DOI:10.7506/spkx1002-6630-20201022-223.
[12] 刘婷婷, 岳琪琪, 张毅, 等. 不同环境温度对冷鲜猪肉品质及菌群多样性影响[J]. 食品科技, 2021, 46(9): 116-123. DOI:10.13684/j.cnki.spkj.2021.09.020.
[13] LEYGONIE C, BRITZ T J, HOFFMAN L C. Impact of freezing and thawing on the quality of meat: review[J]. Meat Science, 2012, 91(2):93-98. DOI:10.1016/j.meatsci.2012.01.013.
[14] ALONSO V, MUELA E, TENAS J, et al. Changes in physicochemical properties and fatty acid composition of pork following long-term frozen storage[J]. European Food Research and Technology, 2016,242(12): 2119-2127. DOI:10.1007/s00217-016-2708-y.
[15] VIRIYARATTANASAK C, HAMADA-SATO N, WATANABE M,et al. Equations for spectrophotometric determination of relative concentrations of myoglobin derivatives in aqueous tuna meat extracts[J]. Food Chemistry, 2011, 127(2): 656-661. DOI:10.1016/j.foodchem.2011.01.001.
[16] HAN M Y, WANG P, XU X L, et al. Low-field NMR study of heatinduced gelation of pork myofibrillar proteins and its relationship with microstructural characteristics[J]. Food Research International, 2014,62: 1175-1182. DOI:10.1016/j.foodres.2014.05.062.
[17] YE K P, DING D M, ZHU X, et al. Modified atmosphere packaging with a small change in gas ratio could maintain pork quality during-3 ℃ storage[J]. Food Control, 2020, 109: 106943. DOI:10.1016/j.foodcont.2019.106943.
[18] TRINDERUP C H, KIM Y H B. Fresh meat color evaluation using a structured light imaging system[J]. Food Research International, 2015,71: 100-107. DOI:10.1016/j.foodres.2015.02.013.
[19] MARTÍNEZ L, DJENANE D, CILLA I, et al. Effect of varying oxygen concentrations on the shelf-life of fresh pork sausages packaged in modified atmosphere[J]. Food Chemistry, 2006, 94(2): 219-225.DOI:10.1016/j.foodchem.2004.11.007.
[20] 金鑫, 禹迎迎, 徐幸莲, 等. 不同温度贮藏热鲜猪肉品质变化比较[J].食品科学, 2012, 33(16): 261-265.
[21] 薛盼盼. 宰后猪肉成熟过程中肌细胞凋亡和自噬对肉品质的影响及相关代谢产物的变化[D]. 扬州: 扬州大学, 2021. DOI:10.27441/d.cnki.gyzdu.2021.001484.
[22] LAN Y, SHANG Y B, SONG, Y, et al. Changes in the quality of superchilled rabbit meat stored at different temperatures[J]. Meat Science, 2016, 117(5): 173-181. DOI:10.1016/j.meatsci.2016.02.017.
[23] 张鹏程, 曾庆, 陈秋月, 等. 冷藏条件下调理猪肉与鲜猪肉的品质评价与比较[J]. 成都大学学报(自然科学版), 2023, 42(3): 248-254;261. DOI:10.3969/j.issn.1004-5422.2023.03.005.
[24] JOLLEY J, KIERMEIER A, SUMNER J. Microbiological quality of Australian beef, sheep and pork carcases, cuts and offals[J]. Foods,2023, 12(20): 3832. DOI:10.3390/foods12203832.
[25] 唐林, 郭柯宇, 赖鲸慧, 等. 屠宰过程中猪胴体表面及环境的细菌菌相分析[J]. 食品科学, 2022, 43(12): 203-209. DOI:10.7506/spkx1002-6630-20210803-025.
[26] ZAREIAN M, TYBUSSEK T, SILCOCK P, et al. Interrelationship among myoglobin forms, lipid oxidation and protein carbonyls in minced pork packaged under modified atmosphere[J]. Food Packaging and Shelf Life, 2019, 20: 100311. DOI:10.1016/j.fpsl.2019.100311.
[27] MIR N A, RAFIQ A, KUMAR F, et al. Determinants of broiler chicken meat quality and factors affecting them: a review[J]. Journal of Food Science and Technology, 2017, 54(10): 2997-3009. DOI:10.1007/s13197-017-2789-z.
[28] SHAO L T, CHEN S S, WANG H D, et al. Advances in understanding the predominance, phenotypes, and mechanisms of bacteria related to meat spoilage[J]. Trends in Food Science & Technology, 2021, 118:822-832. DOI:10.1016/j.tifs.2021.11.007.
[29] CHAUHAN S S, ENGLAND E M. Postmortem glycolysis and glycogenolysis: insights from species comparisons[J]. Meat Science,2018, 144: 118-126. DOI:10.1016/j.meatsci.2018.06.021.
[30] 邹波. 宰前驱赶应激对猪肉品质的影响及控制[D]. 南京: 南京农业大学, 2019. DOI:10.27244/d.cnki.gnjnu.2019.002039.
[31] ZHANG B L, LIU N, KANG K, et al. Dietary guanidineacetic acid supplementation ameliorated meat quality and regulated muscle metabolism of broilers subjected to pre-slaughter transport stress by metabolomics analysis[J]. Poultry Science, 2022, 101(4): 101739.DOI:10.1016/j.psj.2022.101739.
[32] KUO H L, CHEN M T, LIU D C, et al. Relationship between thermal properties of muscle proteins and pork quality[J]. Asian-Australasian Journal of Animal Sciences, 2005, 18(3): 427-432. DOI:10.5713/ajas.2005.427.
[33] CHEN B H, XU T S, YAN Q, et al. Effect of temperature fluctuations on large yellow croaker fillets (Larimichthys crocea) in cold chain logistics: a microbiological and metabolomic analysis[J].Journal of Food Engineering, 2025, 386: 112290. DOI:10.1016/j.jfoodeng.2024.112290.
[34] TAN M Q, LIN Z Y, ZU Y X, et al. Effect of multiple freeze-thaw cycles on the quality of instant sea cucumber: emphatically on water status of by LF-NMR and MRI[J]. Food Research International, 2018,109: 65-71. DOI:10.1016/j.foodres.2018.04.029.
[35] XU Y Q, ZHANG D Q, XIE F F, et al. Changes in water holding capacity of chilled fresh pork in controlled freezing-point storage assisted by different modes of electrostatic field action[J]. Meat Science, 2023, 204: 109269. DOI:10.1016/j.meatsci.2023.109269.