Color-Enhancing Effect of Plasma Activated Water-Gelatin Coatings on Snakehead (Channa argus) Fillets during Storage
张晓丽, 高瑞昌, 李梦哲, 等. 等离子体活化水-明胶涂液对乌鳢鱼片贮藏期间的发色作用[J]. 肉类研究, 2026, 40(4):47-53. DOI:10.7506/rlyj1001-8123-20250513-150. http://www.rlyj.net.cn
ZHANG Xiaoli, GAO Ruichang, LI Mengzhe, et al. Color-enhancing effect of plasma activated water-gelatin coatings on snakehead (Channa argus) fillets during storage[J]. Meat Research, 2026, 40(4): 47-53. (in Chinese with English abstract)DOI:10.7506/rlyj1001-8123-20250513-150. http://www.rlyj.net.cn
乌鳢(Channa argus)是一种营养价值高、分布广泛的鱼类,近年来市场需求增长及预制菜行业快速发展,其产量显著提升[1]。然而,鲜切乌鳢鱼片在加工、运输和贮藏过程中易受微生物污染及温度波动影响,导致品质保障难度增加、货架期缩短。贮藏环境的不稳定性会加速鱼片腐败变质,其中蛋白质变性和水解可引发感官特性、色泽及保水性等物理指标的劣化[2]。作为水产品品质评价的主要指标之一,色泽劣变会显著降低消费者购买意愿[3],进而导致资源浪费。
肌红蛋白(myoglobin,Mb)是一种小型球状蛋白,其结构特征为部分埋藏的卟啉环与中心铁原子结合形成血红素活性位点[4]。该铁离子具有6 个配位键,其中第6配位键与不同气体分子结合可形成不同的Mb构象,决定肌肉色泽呈现;同时,铁离子价态变化(Fe2+、Fe3+或Fe4+)也会影响肌肉色泽呈现[5]。新鲜鱼肉中血红素中心铁离子以Fe2+形式存在[6],当第6配位键无配位分子时形成脱氧肌红蛋白(deoxymyoglobin,Deoxy-Mb),呈现紫红色;当第6配位键与NO配位结合时形成亚硝基肌红蛋白(nitrosylmyoglobin,MbNO),呈现粉红色[5],且NO与Deoxy-Mb具有强亲和性[7]。亚硝酸盐(以亚硝酸钠为主)作为发色剂被广泛应用于肉类[7],但其与胺类或酰胺类反应生成的N-亚硝基化合物具有强致癌性,使亚硝酸盐残留成为被广泛关注的食品安全隐患[8]。为此,科研工作者们致力于研究既能降低亚硝酸盐残留风险又能维持等效发色效果的新型技术路径。
等离子体活化水(plasma activated water,PAW)通过高压等离子体射流电离蒸馏水制得,已应用于蛋白质结构修饰[9]及食品保鲜领域[10-11]。PAW制备过程中,气-液界面会发生复杂的化学反应[12],生成的活性氧和活性氮(reactive oxygen and nitrogen species,RONS)可赋予其杀菌特性,而NO2-和NO3-的存在则使其具有潜在发色功能。Ke Zhigang等[13]发现PAW经电化学处理能促进NO3-和NO2-还原反应,生成更多NO和NH4+,其中NO可与Mb结合生成MbNO,使金枪鱼片呈现粉红色且红度值(a*)上升,同时亚硝酸盐残留控制在可接受范围内。然而,Vichiansan等[14]发现采用PAW浸泡南美白对虾和枪乌贼虽能降低菌落总数,但会引发蛋白质和脂质氧化,这可能归因于PAW与肌肉的直接接触[15]。值得注意的是,低浓度NO在接触肌肉过程中通过缓慢作用于Mb可有效发挥护色作用[16]。因此,本研究选择天然明胶基薄膜作为载体,探究PAW-明胶涂液对乌鳢鱼片物理特性(尤其是色泽特征)的影响,旨在为肉类发色提供新思路。
新鲜乌鳢 市购。
明胶 河南中辰生物科技有限公司;连二亚硫酸钠上海易恩化学技术有限公司;Tris 国药集团化学试剂有限公司。
T25 ULTRA-TURRAX均质机 德国IKA公司;5810R高速离心机 德国Eppendorf公司;PHSJ-3F pH计 上海仪电科学仪器股份有限公司;CR-400色差仪 日本柯尼卡美能达株式会社;UV-19001紫外分光光度计 日本Shimadzu公司;OM-5数码相机 奥之心精密光学(上海)有限公司;PG-1000ZD等离子体发生器 南京苏曼等离子科技有限公司。
1.3.1 PAW制备
使用峰值电压为8 kV的等离子体发生器制备PAW。将等离子喷枪置于500 mL超纯水液面上方5 cm处,分别运行5、10、20 min,制备不同等离子体处理时间的PAW样品,分别记为PAW5、PAW10和PAW20。
1.3.2 PAW-明胶涂液制备
将2 g明胶颗粒与5 mL超纯水混合,室温下孵育30 min,边搅拌边加入超纯水或新鲜制备的PAW,直至明胶完全溶解,制备4 种明胶涂液,G:明胶溶解于超纯水;G-PAW5:明胶溶解于PAW5;G-PAW10:明胶溶解于PAW10;G-PAW20:明胶溶解于PAW20。所有涂液于4 ℃放置4 h后备用。
1.3.3 鱼片样品制备
乌鳢去鳞、去皮后,取背部肌肉切成均匀的薄片(3 cm×2 cm×1 cm),随机分为5 组,其中,FC组为无涂层对照组;FG组为4 ℃下将鱼片浸入G涂液1 min后取出,自然成膜;G-PAW5组、FG-PAW10组和FG-PAW20组为将鱼片分别浸入G-PAW5、G-PAW10及G-PAW20涂液1 min后取出,自然成膜。所有样品真空密封后于4 ℃贮藏12 d,分别于贮藏0、3、6、9、12 d取样分析。
1.3.4 pH值测定
参考Li Yingying等[17]的方法并稍作修改。准确称量2 g鱼片与18 mL蒸馏水于50 mL离心管中混合,4 ℃、10 000 r/min均质1 min,静置30 min,采用pH计测定pH值。每个样品设3 个平行。
1.3.5 水分含量测定
参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》[18]中的直接干燥法测定鱼片水分含量,每个样品设3 个平行。
1.3.6 持水性(water-holding capacity,WHC)测定
参考Yang Xinrui等[19]的方法,称取5 g(m1)鱼片,用双层滤纸包裹并置于离心管中,8 000 r/min离心15 min,取出鱼肉称质量,记为m2/g。每个样品设3 个平行。WHC按式(1)计算:
1.3.7 颜色特性测定
1.3.7.1 颜色变化记录
将不同贮藏时间鱼片样品置于标准拍照箱(DMD-037C-1)中,采用数码相机拍照,记录颜色变化。每个样品设3 个平行。
1.3.7.2 a*与白度测定
参考Shi Tong等[20]的方法,使用便携式色差仪测定鱼片a*、黄度值(b*)与亮度值(L*)。以CIE Lab白色校准板校准仪器。每组样品设3 个平行,每个样品在上、中、下3 个部位测定后取平均值。每个样品设3 个平行。白度按式(2)计算:
1.3.7.3 MbNO相对含量测定
参考王晶[21]的方法,取5 g鱼片样品,加入5 倍体积Tris-HCl缓冲液,匀浆,冰浴提取1 h。4 ℃、10 000 r/min离心15 min,过滤。取15 mL上清液加入装有30 mg连二亚硫酸钠的具塞试管中,摇匀,密封,避光静置10 min,采用紫外分光光度计分别在415、425 nm波长处测定吸光度。每个样品设3 个平行。MbNO相对含量按式(3)计算:
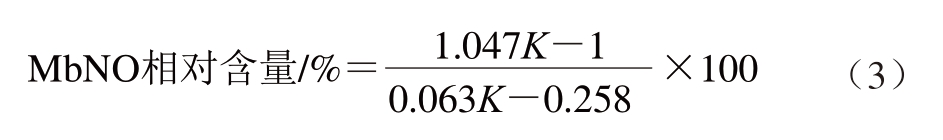
式中:K=A425 nm/A415 nm。
1.3.7.4 ![]() 残留量测定
残留量测定
参照GB 5009.33—2016《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》[22]中的分光光度法(盐酸萘乙二胺法),制作标准曲线(y=0.504x+0.032 5,R2=0.998)时将溶液浓度均稀释10 倍。每个样品设3 个平行。
1.3.8 感官评价
参照GB/T 37062—2018《水产品感官评价指南》[23]与贺莹等[24]的方法并适当修改。选取10 名感官评价人员按照感官评价标准(表1)对鱼片色泽、气味、组织形态及肌肉弹性进行评价,感官评分满分为40。为保证评价准确性与及时性,感官评价人员每隔72 h对乌鳢鱼片进行一次感官评价,共评价5 次。
表1 乌鳢鱼片感官评价标准
Table 1 Sensory evaluation criteria for snakehead fillets

分值色泽气味组织形态肌肉弹性7~10鲜亮具有新鲜鱼肉气味,无异味肌肉富有弹性,按压后凹陷立即消失4~6稍许暗淡稍有异味肌肉组织较致密,纹理较清晰肌肉组织致密,纹理清晰肌肉较有弹性,按压后凹陷消失较慢1~3明显暗淡有明显异味和臭味肌肉组织松散肌肉没有弹性,按压后凹陷不消失
所有实验均至少设置3 组平行,并进行重复实验,实验结果以平均值±标准差表示。采用SPSS Statistics 27软件对数据进行方差分析,通过Duncan多重比较检验判定组间差异显著性(P<0.05)。使用Excel 2016和Origin 2018软件制作图表。
pH值变化能够有效表征鱼肉贮藏过程中的理化性质动态演变[25]。由图1可知,新鲜鱼片的初始pH值为6.83。贮藏前期(0~3 d),各组pH值均显著降低(P<0.05);贮藏中期(3~9 d),FC和FG组pH值分别先从贮藏3 d的6.55和6.62显著增至贮藏6 d的6.82和6.71(P<0.05),再显著降至贮藏9 d的6.70和6.62(P<0.05),相比之下,PAW组pH值变化幅度较小。贮藏后期(9~12 d),FC、FG、FG-PAW5、FG-PAW10、FG-PAW20组pH值分别进一步降至6.54、6.50、6.31、6.22和6.32。整体而言,随着贮藏时间的延长,各组pH值均呈现波动下降趋势。此外,在相同贮藏时间下,PAW组pH值随等离子体处理时间的延长而降低。例如,贮藏3 d时,FG-PAW5、FG-PAW10、FG-PAW20组pH值从贮藏0 d的6.55分别显著降至6.50、6.42和6.39(P<0.05)。
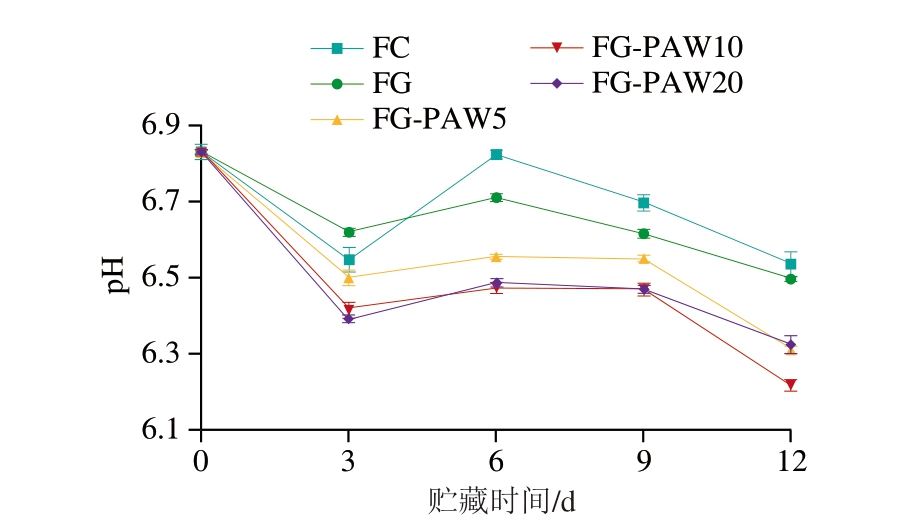
图1 4 ℃贮藏下PAW-明胶涂液处理乌鳢鱼片pH值变化
Fig. 1 Changes in pH of snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
这种pH值的动态变化规律与鱼片中的代谢活动密切相关。贮藏前期,pH值的降低主要源于鱼片中糖原无氧酵解产生的乳酸积累[26];贮藏中期,pH值回升则归因于蛋白质在微生物和内源酶作用下降解产生的氨、三甲胺等挥发性碱性物质[27]。与其他研究[27]不同的是,本研究贮藏后期鱼片pH值进一步下降,可能与该真空包装条件下,厌氧微生物代谢产生的有机酸中和了碱性物质,导致pH值再次降低。值得注意的是,PAW-明胶涂液处理能够显著降低鱼片pH值,且降低程度随等离子体处理时间的延长而增大,这可能是由于活性物质(如RONS)的持续作用所致。该结果与Lotfy等[15]采用PAW处理牛肉导致其pH值下降且下降程度随等离子体处理时间的延长而增大的结果一致。
由图2可知,新鲜乌鳢鱼片水分质量分数为77.50%,与陆俊玮等[27]报道的结果相近。在贮藏过程中,FC组水分含量随贮藏时间的延长而降低,贮藏结束时显著降至76.47%(P<0.05)。在相同贮藏时间下,FG组水分含量显著高于FC(P<0.05),明胶涂液的使用甚至使鱼片水分含量高于新鲜鱼片。贮藏12 d时,FG、FG-PAW5、FG-PAW10、FG-PAW20组水分质量分数分别达79.31%、79.43%、77.95%和78.60%,均显著高于FC组,且FG、FG-PAW5组水分含量显著高于FG-PAW10组和FG-PAW20组(P<0.05)。
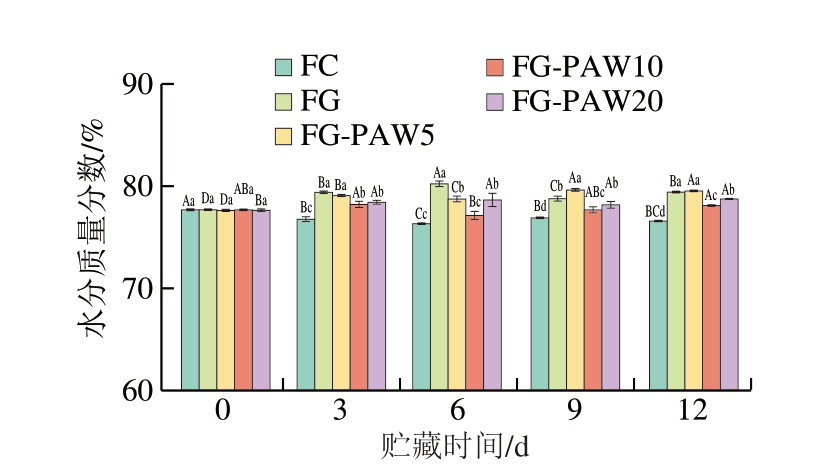
图2 4 ℃贮藏下PAW-明胶涂液处理乌鳢鱼片水分含量变化
Fig. 2 Changes in water content in snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
大写字母不同表示同一处理组在不同贮藏时间之间差异显著(P<0.05);小写字母不同表示同一贮藏时间下不同处理组之间差异显著(P<0.05)。图3、5、6同。
鱼片在贮藏过程中水分含量的变化主要与微生物作用和涂层特性相关。一方面,腐败菌的生长繁殖会引起肌肉组织细胞裂解[28],对肌肉结构造成损伤,导致水分流失,而真空包装的密封环境可在一定程度上抑制微生物生长,减少对鱼片质地的破坏,从而减缓水分流失;另一方面,明胶涂层不仅能够形成物理屏障,组织内部水分流失,涂液中的水分还可能不断渗入鱼片,使其水分含量增加。这可能也是导致FG组水分含量显著高于新鲜鱼片的关键原因。值得注意的是,FG组和FG-PAW5组水分含量一直保持在较高水平,而FG-PAW10组水分质量分数在整个贮藏期间保持相对稳定(约77%),这可能是因为等离子体处理10 min所制备PAW的活性组分(如RONS)与明胶分子发生特异性相互作用,通过调控其分子交联度等形成更为致密的凝胶网络结构,不仅能够减缓水分流失,还可实现活性成分的缓释作用,在避免PAW与鱼肉直接接触的同时延长其作用时间。相比之下,G和G-PAW5凝胶结构相对疏松,涂液中的水分更易渗入鱼片,使其水分含量升高,此推测还需进一步验证。Li Qibin等[29]在冰鲜鲑鱼保鲜研究中发现,采用乳液静电纺丝制备的聚己内酯/卵磷脂/细菌素CAMT6纳米纤维薄膜包裹鱼片可增加其水分含量,与本研究结果相一致。综上,明胶涂层,特别是经PAW处理的涂层,具有阻止水分流失的能力,能够有效减缓鱼片在贮藏期间的水分流失。
WHC是评估肌肉品质的重要指标,其变化直接反映肌肉组织的结构完整性,与肌肉的质地特性密切相关[30]。动物死亡后肌丝晶格收缩、肌球蛋白变性和细胞外空间扩张共同导致WHC下降,高WHC肌肉组织能有效保留水分及可溶性肌浆蛋白,低WHC则往往伴随大量营养成分流失[31]。如图3所示,随着贮藏时间的延长,鱼片WHC呈显著下降趋势(P<0.05)。其中,贮藏结束时FC组WHC下降幅度相对较小,仅从79.48%降至76.27%,而经涂液处理的鱼片的WHC显著低于FC组(P<0.05),分别降至68.66%(FG组)、71.08%(FG-PAW5组)、73.27%(FG-PAW10组)和74.42%(FG-PAW20组),其中等离子体处理10 min和20 min的PAW-明胶涂液表现出相对较高的WHC维持能力。值得注意的是,明胶涂层虽能够通过物理阻隔作用将水分束缚在鱼片中(图2),但在离心力作用下该封闭体系反而加剧WHC的降低,特别是水分含量最高的FG组和FG-PAW5组。因此,不可简单地以WHC降低表征鱼片品质劣变,还需结合水分含量与状态、蛋白质状态等多维度指标综合评估。
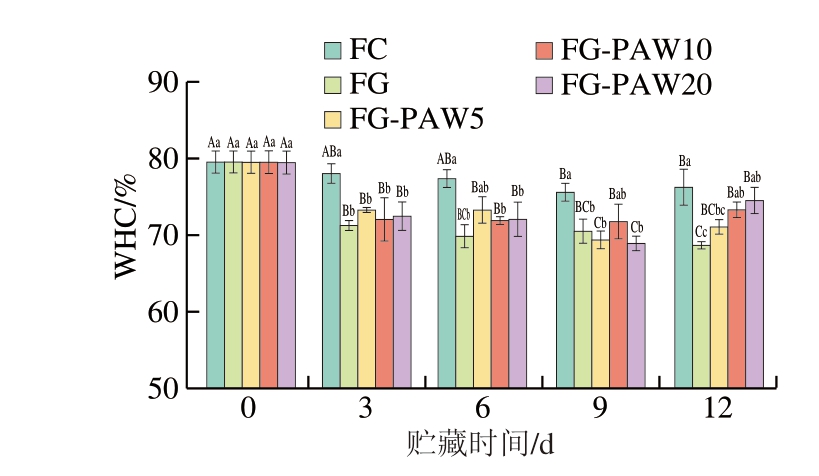
图3 4 ℃贮藏下PAW-明胶涂液处理乌鳢鱼片WHC变化
Fig. 3 Changes in WHC of snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
色泽是评价肉制品品质的重要指标之一,其变化直接影响消费者的接受程度[32]。如图4A所示,新鲜鱼片的红肉在无氧条件下呈现典型的紫红色。贮藏过程中,PAW-明胶涂液处理的鱼片从贮藏3 d起即呈现鲜艳的红色,而FC组和FG组鱼片仍呈现缺氧的紫红色,且从贮藏9 d开始,颜色逐渐变淡。如图4B所示,鱼片白肉从初始的透明偏黄色逐渐转变为白色,其中PAW处理组的鱼片色泽变化更协调。
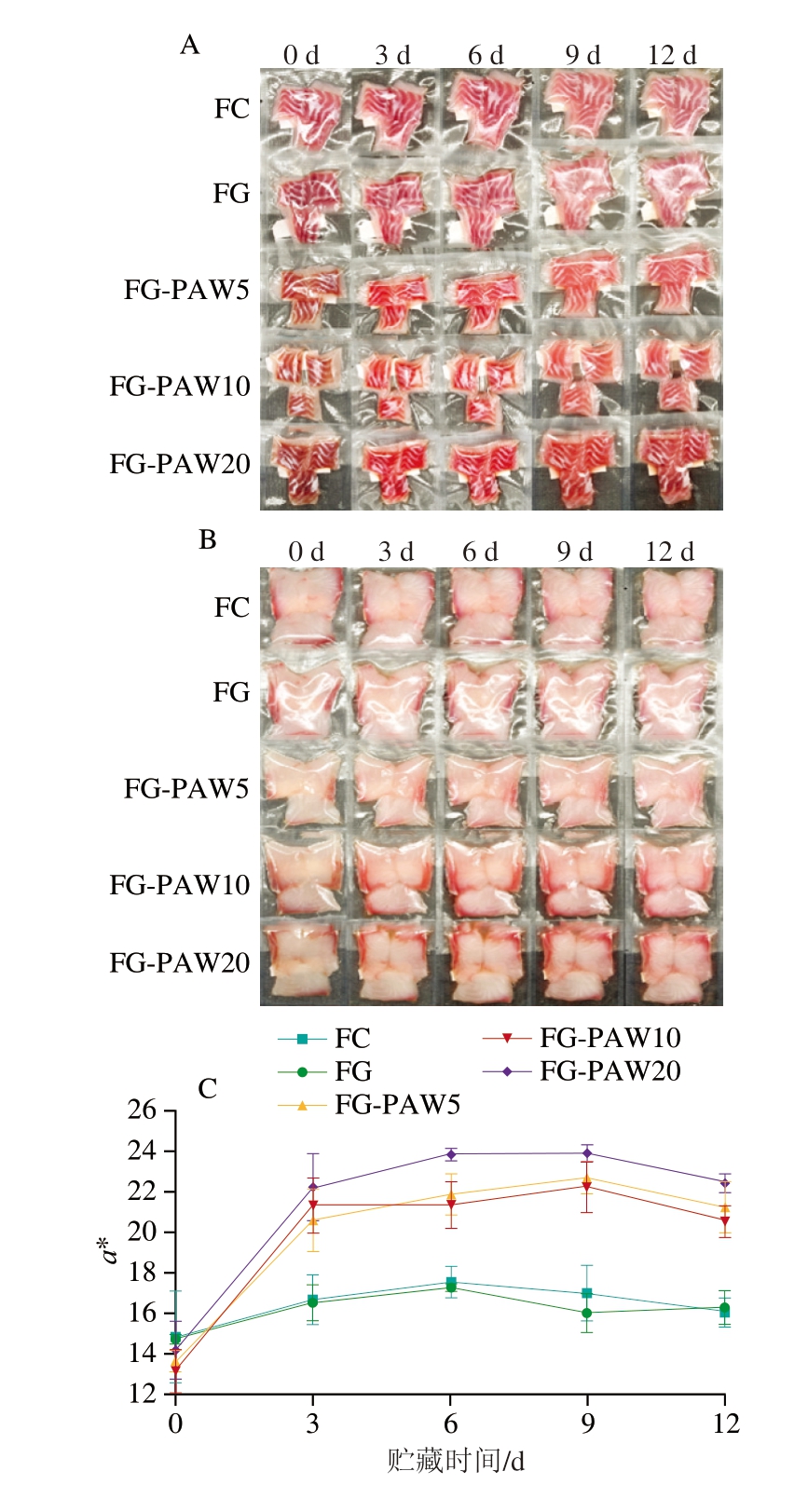
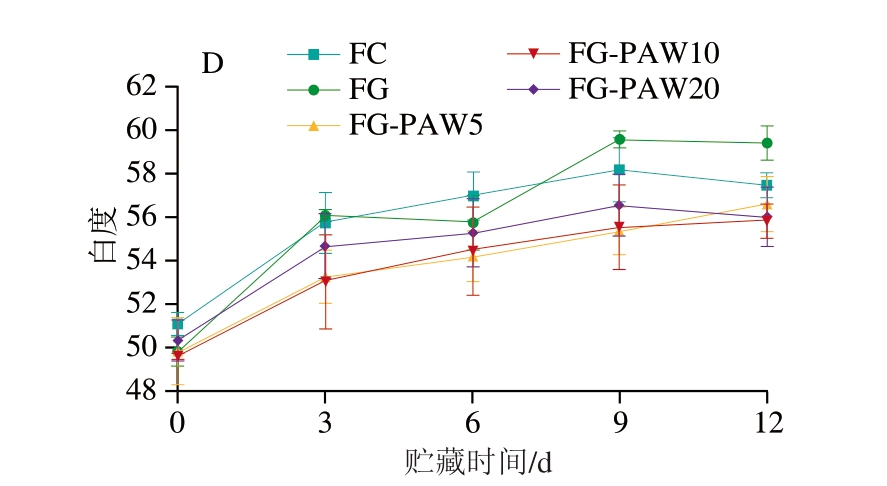
图4 4 ℃贮藏下PAW-明胶涂液处理乌鳢鱼片红肉(A)与白肉(B)颜色及a*(C)、白度(D)变化
Fig. 4 Changes in color of red meat (A) and white meat (B), redness value (C) and whiteness (D) of snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
如图4C所示,PAW-明胶涂液处理可有效提升乌鳢鱼片a*,而无PAW的FC组和FG组因在真空包装的密封环境中,鱼片呈现紫红色,a*在贮藏过程中也略有增加。贮藏9 d时,PAW-明胶涂液处理组a*达到峰值,FG-PAW5、FG-PAW10、FG-PAW20组a*分别从13.57、13.14、14.21显著增至22.67、22.26、23.93(P<0.05)。随着贮藏时间进一步延长,a*略有降低。这一结果与Lotfy等[15]采用PAW处理牛肉的研究结果较为一致,证实PAW处理时间与a*提升呈正相关。如图4D所示,各组白度随贮藏时间延长有不同程度的增加。贮藏结束时,各组白度分别增加14.06%(FC组)、19.66%(FG组)、11.17%(FGPAW5组)、11.84%(FG-PAW10组)和12.39%(FGPAW20组),以FG组增加程度最大。类似地,金枪鱼白度也随贮藏时间的延长而增加[32]。
因无外源NO的引入,未添加PAW的FC组与FG组未检出MbNO。由于NO与鱼片的接触过程较为缓慢,PAW-明胶涂液处理鱼片在贮藏初期也未检出MbNO,与a*结果相一致。如图5所示,随贮藏时间的延长,MbNO相对含量呈现先增加后降低的显著变化趋势(P<0.05)。贮藏3 d时,FG-PAW5、FG-PAW10、FG-PAW20组MbNO相对含量分别为27.65%、45.20%和36.78%,其中FG-PAW5组MbNO相对含量在贮藏6 d达到最大值(44.16%),而FG-PAW10组和FGPAW20组MbNO相对含量则在贮藏9 d分别增至最大值(53.42%和55.52%)。相同贮藏时间下,FG-PAW10组和FG-PAW20组MbNO相对含量始终显著高于FGPAW5组(P<0.05),可能是因为等离子体处理时间越长,PAW活性成分(如NO2-、NO3-等)含量越高[33],可与更多中心铁离子配位结合形成MbNO。贮藏结束时,各组鱼片MbNO相对含量分别降至15.90%、30.37%和28.42%,这种下降趋势可能与鱼片腐败变质导致的肌纤维结构破坏有关,水溶性蛋白随汁液流失[31],明胶涂层的物理阻隔作用可能维持物质保留,其中Mb的流失直接导致MbNO相对含量降低,最终导致鱼片白度上升、a*下降。
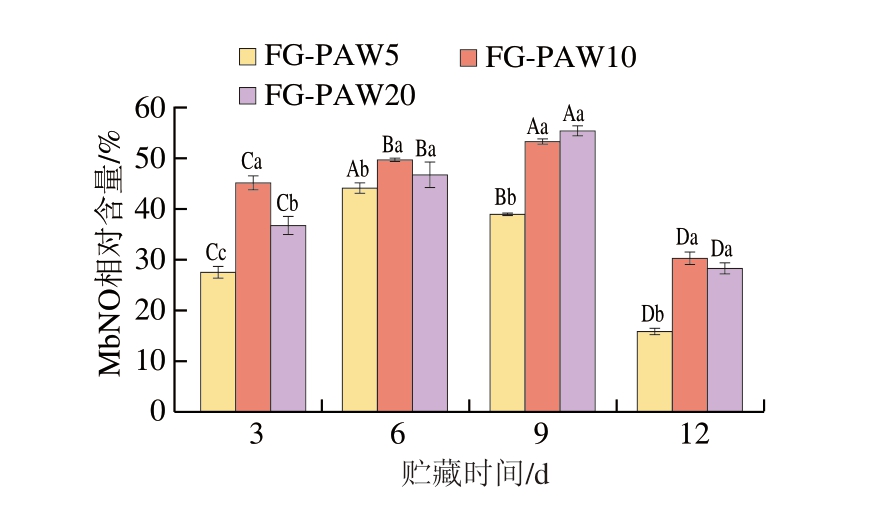
图5 4 ℃贮藏PAW-明胶涂液处理乌鳢鱼片MbNO相对含量变化
Fig. 5 Changes in MbNO relative content of snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
根据GB 2760—2024《食品安全国家标准 食品添加剂使用标准》[34]规定,水产品中亚硝酸盐残留量不得超过30 mg/kg。如图6所示,贮藏期间,FG-PAW5、FG-PAW10、FG-PAW20组NO2-最高残留量分别为0.55、1.02、1.32 mg/kg,均远低于标准限量。随贮藏时间的延长,NO2-残留量整体呈现先下降后上升的显著变化趋势(P<0.05)。这可能是因为贮藏前期NO2-主要与Mb结合形成MbNO导致其含量下降,与MbNO相对含量增加的变化趋势相符;贮藏后期因鱼片腐败变质导致Mb流失,MbNO生成减少,致使NO2-残留量回升。总而言之,PAW在促进鱼片发色(MbNO形成)的同时,其引入的NO2-始终维持在极低水平(<1.5 mg/kg),符合食品安全国家标准要求。
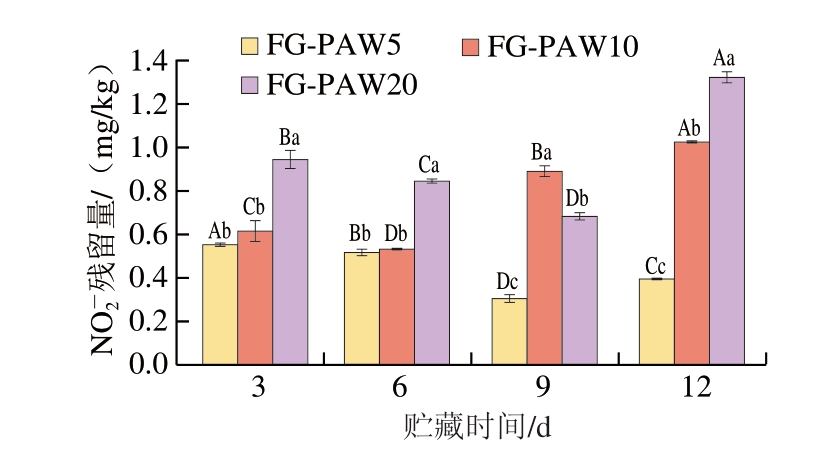
图6 4 ℃贮藏下PAW-明胶涂液处理乌鳢鱼片中NO-2残留量变化
Fig. 6 Changes in residual NO-2 in snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
如图7所示,新鲜乌鳢鱼片色泽、气味、组织形态及肌肉弹性均呈现为最佳状态。随贮藏时间的延长,鱼片感官评分呈现持续下降趋势,这主要归因于鱼肉中丰富的水分和蛋白质等,在微生物和内源酶作用下易发生腐败变质[35]。在贮藏过程中,PAW-明胶涂液处理鱼片的感官评分始终高于FC组和FG组。贮藏6 d时,FC组和FG组感官评分分别降至19.86和22.86,显著低于PAW-明胶涂液处理组(P<0.05)。贮藏结束时,FG-PAW5、FG-PAW10、FG-PAW20组感官评分分别降至21.71、23.14、22.14,此时乌鳢鱼片仍具有良好的感官品质,表明经PAW-明胶涂液处理具有较好的保鲜效果。贺莹等[24]采用肉桂精油-木耳多糖复合涂膜对鲜切鲈鱼片进行保鲜,涂膜鱼片感官评分在贮藏结束时仍保持较高水平,与本研究结果一致。此外,PAW-明胶涂液处理对鱼片的发色作用使其呈现更受消费者青睐的鲜红色,进一步提升了产品的感官接受度。
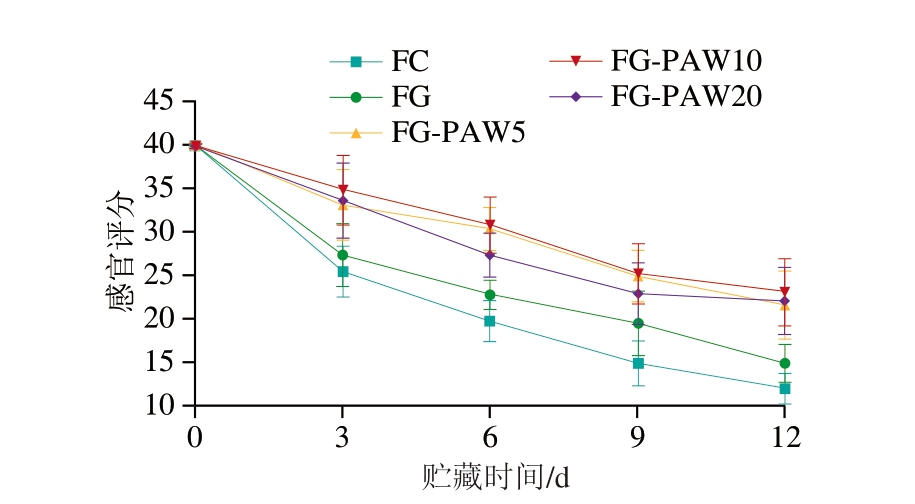
图7 4 ℃贮藏下PAW-明胶涂液处理乌鳢鱼片感官评分
Fig. 7 Sensory scores of snakehead fillets treated with PAW-gelatin coating solution during storage at 4 ℃
本研究通过考察PAW-明胶涂液处理对乌鳢鱼片贮藏期间理化特性的影响发现,贮藏前期,PAW-明胶涂液处理能有效降低鱼片pH值,明胶涂液处理可提高鱼片水分含量,贮藏结束时,FG-PAW10组水分质量分数为77.95%,甚至高于新鲜鱼片(77.50%)。然而,高水分含量也导致WHC降低,PAW的添加则可减缓FG-PAW10组和FG-PAW20组WHC降低程度。PAW中的活性成分可与Mb结合生成MbNO,其中FG-PAW20组MbNO相对含量最高达55.52%。因此,乌鳢鱼片a*增加使鱼片呈现令人愉悦的鲜红色。在发色的同时,鱼片中NO2-残留量最高仅为1.32 mg/kg,远低于食品安全国家标准限值(30 mg/kg),且PAW-明胶涂液处理鱼片感官评分更高。本研究不仅可为水产品保鲜与色泽调控提供新思路,也可为PAW-明胶涂液的应用提供理论基础。
[1] 陈胜军, 路美明, 相欢, 等. 乌鳢营养评价与加工保鲜技术研究进展[J]. 肉类研究, 2023, 37(2): 40-45. DOI:10.7506/rlyj1001-8123-20221017-141
[2] 许铭强, 苏文贵, 曹双瑜, 等. 不同冻藏温度对新疆高白鲑鱼肉的品质变化[J]. 新疆农业科学, 2022, 59(12): 3093-3103. DOI:10.6048/j.issn.1001-4330.2022.12.025.
[3] 朱文慧, 谭桂芝, 步营, 等. 低温等离子体耦合微酸性电解水对三文鱼的保鲜作用[J]. 中国食品学报, 2024, 24(2): 228-238.DOI:10.16429/j.1009-7848.2024.02.022.
[4] ESLAMI-FARSANI R, FARHADIAN S, SHAREGHI B, et al.Structural change of myoglobin structure after binding with spermidine[J]. Journal of Molecular Liquids, 2022, 352: 118691.DOI:10.1016/j.molliq.2022.118691.
[5] 陈雅淇. 等离子体活性水对肌红蛋白结构影响及火腿发色应用[D].广州: 华南理工大学, 2020. DOI:10.27151/d.cnki.ghnlu.2020.000660.
[6] RICHARDS M P, ØSTDAL H, ANDERSEN H J. Deoxyhemoglobinmediated lipid oxidation in washed fish muscle[J]. Journal of Agricultural and Food Chemistry, 2002, 50(5): 1278-1283.DOI:10.1021/jf011093m.
[7] 王自超. 外源性一氧化氮对罗非鱼的影响[D]. 南宁: 广西大学,2013.
[8] SEBRANEK J G, BACUS J N. Cured meat products without direct addition of nitrate or nitrite: what are the issues?[J]. Meat Science,2007, 77(1): 136-147. DOI:10.1016/j.meatsci.2007.03.025.
[9] LI M Z, SHI T, WANG X, et al. Plasma-activated water promoted the aggregation of Aristichthys nobilis myofibrillar protein and the effects on gelation properties[J]. Current Research in Food Science, 2022, 5:1616-1624. DOI:10.1016/j.crfs.2022.09.003.
[10] HAN Q Y, WEN X, GAO J Y, et al. Application of plasmaactivated water in the food industry: a review of recent research developments[J]. Food Chemistry, 2023, 405: 134797. DOI:10.1016/j.foodchem.2022.134797.
[11] 柯志刚, 田玉玲, 刘书来, 等. 等离子体活化水耦合生物保鲜剂对牛肉的保鲜作用[J]. 食品科学, 2025, 46(2): 20-29. DOI:10.7506/spkx1002-6630-20240614-084.
[12] ZHOU R W, ZHOU R S, WANG P Y, et al. Plasma-activated water:generation, origin of reactive species and biological applications[J].Journal of Physics D: Applied Physics, 2020, 53(30): 303001.DOI:10.1088/1361-6463/ab81cf.
[13] KE Z G, YI Y Q, LIU Y H, et al. Synergistic effects of plasmaactivated water (PAW) and electrochemical treatment on the color of tuna slices[J]. Food and Bioproducts Processing, 2024, 147: 42-52.DOI:10.1016/j.fbp.2024.05.012.
[14] VICHIANSAN N, PHANUMONG P, MEKWILAI T, et al. Effect of plasma-activated water (PAW) on the shelf lives of whiteleg shrimp(Litopenaeus vannamei) and splendid squid (Loligo formosana)[J].Food and Bioprocess Technology, 2024, 17(9): 2644-2660.DOI:10.1007/s11947-023-03282-z.
[15] LOTFY K, KHALIL S. Effect of plasma-activated water on microbial quality and physicochemical properties of fresh beef[J]. Open Physics,2022, 20(1): 573-586. DOI:10.1515/phys-2022-0049.
[16] HEROLD S, RÖCK G. Reactions of deoxy-, oxy-, and methemoglobin with nitrogen monoxide[J]. Journal of Biological Chemistry, 2003,278(9): 6623-6634. DOI:10.1074/jbc.m210275200.
[17] LI Y Y, HUANG X B, ZHAO X Q, et al. The refrigerated preservation effect of Amomum tsao-ko essential oil and its microcapsules loaded on polyvinyl alcohol/starch composite film based on broad-spectrum antibacterial properties on golden pompanos[J]. LWT-Food Science and Technology, 2025, 222: 117595. DOI:10.1016/j.lwt.2025.117595.
[18] 国家卫生和计划生育委员会. 食品安全国家标准 食品中水分的测定: GB 5009.3—2016[S]. 北京: 中国标准出版社, 2017.
[19] YANG X R, MEI J, XIE J. Effects of different slaughtering methods on the biochemical characteristics and quality changes of tilapia(Oreochromis niloticus) during cold storage[J]. Food Chemistry: X,2024, 24: 101951. DOI:10.1016/j.fochx.2024.101951.
[20] SHI T, XIE Y, CAO X Y, et al. Mechanism of L-arginine improving the macroscopic and microscopic qualities of Acipenser schrenckii surimi gel under low-salt conditions and microwave irradiation: significance of moisture migration and distribution[J]. Current Research in Food Science, 2025, 10: 101018. DOI:10.1016/j.crfs.2025.101018.
[21] 王晶. 冻罗非鱼鱼片新型发色方法的研究[D]. 海口: 海南大学,2015.
[22] 国家卫生和计划生育委员会, 国家食品药品监督管理总局. 食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定: GB 5009.33—2016[S]. 北京: 中国标准出版社, 2017.
[23] 国家市场监督管理总局, 国家标准化管理委员会. 水产品感官评价指南: GB/T 37062—2018[S]. 北京: 中国标准出版社, 2019.
[24] 贺莹, 冯玉, 邢佳瑶, 等. 肉桂精油-木耳多糖复合涂膜对冷藏鲜切鲈鱼片的保鲜效果[J]. 肉类研究, 2025, 39(2): 33-38. DOI:10.7506/rlyj1001-8123-20240902-232.
[25] 郑稳. 微冻、复合保鲜剂及抑菌涂膜剂对鲈鱼保鲜效果的影响[D].上海: 上海海洋大学, 2024. DOI:10.27314/d.cnki.gsscu.2024.001062.
[26] FU L L, RU Y, HONG Q L, et al. Active packaging coatings based on agarose caffeate: preparation, characterisation, and application in grass carp (Ctenopharyngodon idellus) preservation[J]. Food Packaging and Shelf Life, 2023, 37: 101089. DOI:10.1016/j.fpsl.2023.101089.
[27] 陆俊玮, 朱严华, 黄菊, 等. 芦荟提取物对冷藏黑鱼片的保鲜作用[J].浙江海洋大学学报(自然科学版), 2019(1): 36-43.
[28] 贺莹, 刘恩悦, 庞晓婷, 等. 姜黄素/壳聚糖可食性复合膜对鲈鱼片保鲜效果的研究[J]. 印刷与数字媒体技术研究, 2023(5): 83-91.DOI:10.19370/j.cnki.cn10-1886/ts.2023.05.009.
[29] LI Q B, LIANG W Q, LÜ L N, et al. Preparation of PCL/lecithin/bacteriocin CAMT6 antimicrobial and antioxidant nanofiber films using emulsion electrospinning: characteristics and application in chilled salmon preservation[J]. Food Research International, 2024,175: 113747. DOI:10.1016/j.foodres.2023.113747.
[30] 王扬蕊, 袁硕, 白凤翎, 等. 蜡样芽孢杆菌YF-2对冷藏三文鱼的保鲜作用[J]. 中国食品学报, 2025, 25(1): 305-313. DOI:10.16429/j.1009-7848.2025.01.029.
[31] KAALE L D, EIKEVIK T M, RUSTAD T, et al. Changes in water holding capacity and drip loss of Atlantic salmon (Salmo salar) muscle during superchilled storage[J]. LWT-Food Science and Technology,2014, 55(2): 528-535. DOI:10.1016/j.lwt.2013.10.021.
[32] BU Y, HAN M L, TAN G Z, et al. Changes in quality characteristics of southern bluefin tuna (Thunnus maccoyii) during refrigerated storage and their correlation with color stability[J]. LWT-Food Science and Technology, 2022, 154: 112715. DOI:10.1016/j.lwt.2021.112715.
[33] WANG H X, DING C J, LU J L, et al. Study on the thawing characteristics of beef in plasma-activated water[J]. Innovative Food Science & Emerging Technologies, 2024, 92: 103576. DOI:10.1016/j.ifset.2024.103576.
[34] 国家卫生健康委员会, 国家市场监督管理总局. 食品安全国家标准食品添加剂使用标准: GB 2760—2024[S]. 北京: 中国标准出版社,2024.
[35] LI T T, SHEN Y, CHEN H T, et al. Antibacterial properties of coaxial spinning membrane of methyl ferulate/zein and its preservation effect on sea bass[J]. Foods, 2021, 10(10): 2385. DOI:10.3390/foods10102385.