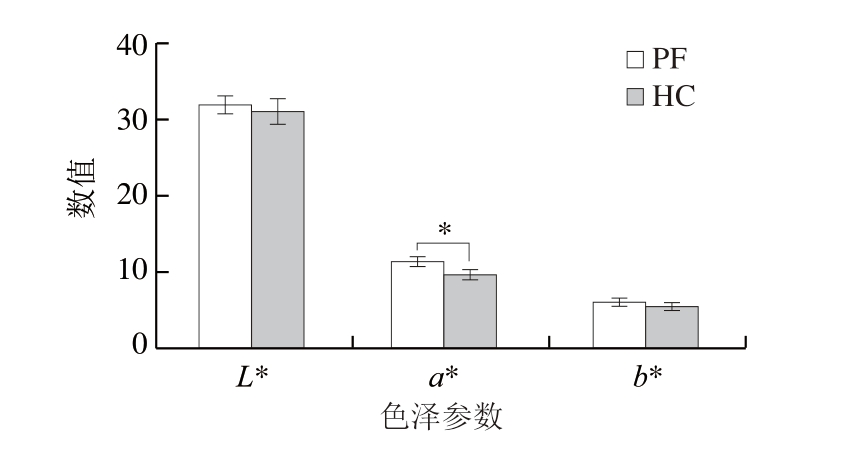
图1 宰前氧化应激对绵羊肉色的影响
Fig. 1 Effect of pre-slaughter oxidative stress on the color of lamb meat
*.差异显著(P<0.05)。图2同。
Effects of Premortem Oxidative Stress on the Quality and Oxidative Stability of Sheep Meat during Postmortem Aging
张义飞, 岳灵, 杨续金, 等. 宰前氧化应激对宰后成熟绵羊肉品质及氧化稳定性的影响[J]. 肉类研究, 2026, 40(4): 9-15.DOI:10.7506/rlyj1001-8123-20250429-132. http://www.rlyj.net.cn
ZHANG Yifei, YUE Ling, YANG Xujin, et al. Effects of premortem oxidative stress on the quality and oxidative stability of sheep meat during postmortem aging[J]. Meat Research, 2026, 40(4): 9-15. DOI:10.7506/rlyj1001-8123-20250429-132.http://www.rlyj.net.cn
在过去的20 年里,随着世界人均国内生产总值购买力平价的提高,绵羊肉产量在全球范围内稳步增长。在某种程度上,羊肉消费量的增加反映了居民生活水平的提高。然而,消费者却更喜爱牧区的羊肉,因为天然放牧的羊在肉质方面比高精料育肥更具优势,如具有更好的肉色、质构特性,更健康的脂肪酸谱[1],以及更高的鲜味特征脂肪酸和风味氨基酸含量[2]。这些优势得益于高矿化度的水资源、天然的草本植物、洁净的土壤等自然放牧条件,使天然放牧羊具有独特的肉质特征[3]。事实上,过度放牧在世界范围内已成为一个严重的问题,特别是在干旱和半干旱地区。中国已开始推行草地禁牧、休牧的草畜平衡制度。作为中国羊肉的主要产地,内蒙古地区绵羊的主要养殖模式已转变为高精料育肥,这样虽然可以使绵羊快速育肥,但也导致绵羊营养应激,引发瘤胃代谢物异常[4],导致机体氧化应激[5]。有研究[6]发现,饲喂高能量日粮的羔羊体内脂肪、血清胆固醇、三酰甘油和氧化应激水平均有所增加。
成熟过程对调控宰后肉品质具有重要作用。目前已有研究[7]发现,在宰后成熟过程中,羊肉的氧化稳定性会发生变化。Dou Lu等[7]指出,随着成熟时间的延长,羊肉中丙二醛水平增加。Carvalho等[8]发现,抗氧化酶如超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)和谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)等抗氧化酶的活性在宰后成熟过程中会降低,导致羊肉的抗氧化能力下降,从而影响羊肉品质。当肉类的抗氧化能力降低时,肉的成分,包括脂质、蛋白质、糖类、血红素等均会被氧化。尤其是脂质和蛋白质氧化,已被确定为对肉类品质有害[9]。
虽然相关报道表明饲喂高精料能诱导绵羊机体发生氧化应激,也指出宰后成熟过程中肉的氧化稳定性发生变化会影响肉品质,但宰前氧化应激是否通过宰后成熟过程影响肉品质,以及如何影响肉的氧化稳定性目前还尚不清楚。本研究旨在通过由饲养方式介导氧化应激的条件下,分析比较宰后绵羊肉品质及氧化稳定性的变化,为深入了解调控宰后羊肉品质的机制提供理论参考。
实验羔羊来自内蒙古土默特左旗成俊肉羊养殖场,品种为蒙古羊与小尾寒羊的杂交羔羊。
尿素、盐酸、磷酸、硝酸、盐酸胍、浓硫酸、三氯乙酸(trichloroacetic acid,TCA)、无水乙醇、氢氧化钠、三氯甲烷、磷酸氢二钾、磷酸二氢钾、乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)、EDTA-2Na、2-硫代巴比妥酸、2,4-二硝基苯肼(2,4-dinitrophenylhydrazine,DNPH) 国药集团化学试剂有限公司;乙酸乙酯上海麦克林生化科技股份有限公司;5,5’-二硫代双(2-硝基苯甲酸)(5,5’-dithiobis-(2-nitrobenzoic acid),DTNB)北京索莱宝科技有限公司;总抗氧化能力(total antioxidant capacity,T-AOC)测定试剂盒(A015-2-1)、SOD测定试剂盒(A001-3-2)、GSH-Px测定试剂盒(A005-1-2)、CAT测定试剂盒(A007-1-1) 南京建成生物工程研究所。
HS 4磁力搅拌器、VORTEX 2旋涡振荡器、A11 basic研磨杯 德国IKA公司;TGL-20B离心机 上海安亭科学仪器厂;Allegrax-30R高速冷冻离心机 美国贝克曼库尔特有限公司;U-2910紫外-可见分光光度计 日本Hitachi公司;XHF-DY高速分散器 宁波新芝生物科技股份有限公司;PHS-3C数字式pH计 上海仪电科学仪器股份有限公司;CR-20色差仪 日本Konica Minolta公司;KDY-9830凯氏定氮仪 北京市通润源机电技术有限责任公司;SOX606脂肪测定仪 山东海能科学仪器有限公司;SX2-4-10马弗炉 上海一恒科技有限公司。
1.3.1 饲养管理
本动物实验得到内蒙古农业大学机构动物护理和使用委员会批准,符合国家动物福利法规(批准号:NND2022106)。
随机选择10 只羔羊分为天然放牧组(PF)和高精料育肥组(HC),每组各5 只。PF组羔羊全程为天然草场纯放牧,不补充精料。HC组羔羊饲喂育肥日粮,基础日粮由粗饲料混合牧草和精补料组成,精补料配方:玉米67%、麸皮9%、豆粕12%、棉粕10%、石粉1%、食盐0.5%、微量元素0.5%(均为质量分数),精粗料质量比7∶3,预饲期15 d,育肥期60 d。
实验前将羊舍进行彻底消毒,实验期间对羊舍进行定期打扫和消毒,自然通风。实验羊只于每天8:00和18:00进行2 次饲喂,安装独立食槽和饮水装置,保证羊只自由采食和饮水。
1.3.2 样品采集与测定
饲养结束后,实验用羔羊现场屠宰,宰前禁食24 h,屠宰时,每个处理组屠宰5 只羔羊,平均活体质量分别为(51.57±3.90)kg(PF)和(49.91±3.80)kg(HC),平均胴体质量分别为(25.27±1.91)kg(PF)和(24.46±1.86)kg(HC)。宰后取相同部位背最长肌,每条背最长肌平均分为5 块。取其中1 块进行现场检测,对于不能现场测定的指标(羰基含量、总巯基含量、硫代巴比妥酸反应物(thiobarbituric acid reactive substances,TBARS)值和抗氧化能力),将样品立即在液氮中快速冷冻待测,并指定为宰后成熟0 h样品。然后将剩余4 块样品分别在4 ℃下贮藏6、24、72、120 h,每个贮藏期结束时获得的样品立即测定或于-80 ℃保存待测。
1.3.3 色度测定
使用经自检及白板、零点校准后的色差仪对肉色进行测定。随机选择肉样,沿垂直肌纤维的方向切取3 cm×3 cm×2 cm的肉块进行测定,记录样品亮度值(L*)、红度值(a*)、黄度值(b*),每组样品平行测定3 次,取平均值。
1.3.4 常规营养成分测定
水分含量的测定参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》中的方法;灰分含量的测定参照GB 5009.4—2016《食品安全国家标准 食品中灰分的测定》中的方法;粗蛋白含量的测定参照GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》中的方法;粗脂肪含量的测定参照GB 5009.6—2016《食品安全国家标准 食品中脂肪的测定》中的方法。
1.3.5 活性氧(reactive oxygen species,ROS)含量测定
参考张玉林等[10]的方法并稍作修改。取样品0.5 g,剪碎后放入含4.5 mL Tri-HCl缓冲液(10 mmol/L Tris-HCl、10 mmol/L蔗糖、0.1 mmol/L EDTA-2Na、0.008 g/mL NaCl,pH 7.4)的容器中。在冰浴条件下,10 000×g匀浆20 s,此过程重复3 次。随后4 ℃、3 000×g离心15 min,收集上清液。采用双缩脲法测定上清液中的蛋白质量浓度。之后,取100 μL上清液与100 μL反应缓冲液(10 mmol/L Tris-HCl、10 mmol/L蔗糖、0.1 mmol/L EDTA-2Na、0.008 g/mL NaCl、10 μmol/L 2’,7’-二氯二氢荧光素二乙酸酯,pH 7.4)混合,在避光、37 ℃条件下孵育15 min。最后,测定孵育后的荧光强度,激发波长488 nm,发射波长525 nm。
1.3.6 pH值测定
称取剔除筋腱后的样品2.5 g,加入10 mL预冷的蒸馏水,10 000 r/min匀浆20 s。待溶液稳定后,使用数字式pH计测定样品pH值。
1.3.7 羰基含量测定
参考丁红艳等[11]的方法并稍作修改,将1 g切碎的样品与10 mL 0.15 mol/L KCl溶液匀浆(10 000 r/min,10 s/次,3 次),吸取0.1 mL匀浆物至2 mL离心管中,向其中加入1 mL 10%(m/m)TCA溶液,2 000×g离心10 min,去除上清液。一管添加1 mL 0.2%(m/m)DNPH溶液(溶于2 mol/L HCl),一管添加1 mL 2 mol/L HCl作为对照。室温静置1 h(每20 min涡旋1 次)后,加入1 mL 10%(m/m)TCA溶液,将样品涡旋并再次2 000×g离心10 min,去除上清液,将沉淀用1.5 mL乙醇-乙酸乙酯(1∶1,V/V)洗涤,混匀,15 000×g离心5 min,重复2 次。然后将沉淀溶于1.5 mL 6 mol/L盐酸胍溶液(溶于20 mmol/L磷酸钾缓冲液,pH 6.5)中,涡旋混匀,4 000×g离心3 min,分别在370、280 nm波长处测定样品吸光度。羰基含量以nmol/mg表示。
1.3.8 总巯基含量测定
参考丁红艳等[11]的方法并稍作修改。取1 g肉样切碎至小米粒大小,加入9 mL 0.6 mol/L氯化钾溶液,匀浆3 次(10 000 r/min,10 s/次,3 次),之后使用脱脂棉纱布过滤匀浆液,取0.1 mL滤液,加入2.5 mL磷酸缓冲液(0.1 mol/L KH2PO4/K2HPO4、1 mmol/L EDTA、8 mol/L尿素,pH 8.0),加入0.05 mL 10 mmol/L DTNB溶液,混匀后避光放置15 min(黑纸或锡箔纸包裹),4 500×g离心5 min,取上清液,测定412 nm波长处吸光度,总巯基含量以nmol/mg表示。
1.3.9 TBARS值测定
参考丁红艳等[11]的方法并稍作修改。取适量样品用研磨杯研磨20 s后,准确称取5.0 g研磨后的肉样,加入25 mL 7.5%(m/m)TCA溶液(含0.01%(m/m)EDTA),用磁力搅拌器搅拌30 min(放入转子后用封口膜封口),双层定性滤纸过滤2 次;取5 mL上清液,加入5 mL 0.02 mol/L 2-硫代巴比妥酸溶液,在沸水浴中保温40 min(用无菌封口膜封口)后取出,室温冷却1 h,倒入离心管,加入5 mL三氯甲烷,摇匀,静置15 min,分层后吸取上清液,测定532、600 nm波长处的吸光度。
1.3.10 抗氧化能力测定
使用0.9 g/100 mL生理盐水对肉样进行漂洗,准确称取1.0 g肉样,加入9 倍体积生理盐水,在冰水浴条件下,使用高速匀浆机进行组织匀浆(8 000 r/min),制成10%的组织匀浆液,3 000 r/min离心10 min,取上清液,根据试剂盒说明书分别测定样品T-AOC、GSH-Px、CAT、SOD活性。
采用Microsoft Excel软件进行数据处理、SPSS 25.0软件进行显著性分析、Origin软件作图。
羊肉的颜色对消费者的购买欲有重要影响,消费者更喜爱颜色为鲜红色的羊肉,因为它通常与更高的新鲜度和更好的肉品质相联系[12]。a*反映肉的红度,数值越大则肉色越鲜红,说明肉更新鲜。如图1所示,PF组具有比HC组更高的a*,这可能是PF组绵羊肉中肌纤维的细胞色素和肌红蛋白含量较高所导致的[13]。Sadrarhami等[14]的饲养实验结果表明,虽然高精料育肥的羔羊生长更快,产肉量也更高,但放牧的羔羊更加活跃,进食和走动的次数更多,使放牧羊肉具有更为优质的营养成分和肉色。这一结论与本研究结果相吻合。

图1 宰前氧化应激对绵羊肉色的影响
Fig. 1 Effect of pre-slaughter oxidative stress on the color of lamb meat
*.差异显著(P<0.05)。图2同。
羊肉的营养成分指标反映其价值。如图2所示,与PF组相比,HC组的灰分含量显著降低(P<0.05),而粗脂肪含量显著升高(P<0.05),水分和粗蛋白含量则无显著差异。羊肉中脂肪和脂肪酸的含量受饲养系统的影响,与高精料育肥的羊相比,通常以放牧饲养为主的羔羊的脂肪含量更低[15]。放牧期间羔羊摄入了土壤中的矿物质等金属元素,可能是导致PF组灰分含量较高的原因。李春冬等[16]的研究也得出类似结论。
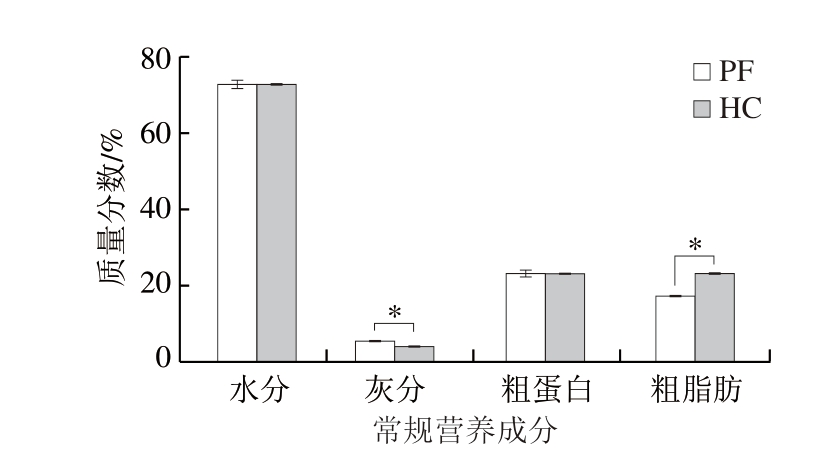
图2 绵羊肉常规营养成分
Fig. 2 Proximate nutrients of lamb meat
绵羊肌纤维的ROS含量可以反映绵羊机体氧化应激的程度[17],较高的ROS含量表明绵羊机体氧化应激更严重。如图3所示,宰后成熟0 h的HC组羊肉ROS含量显著高于PF组(P<0.05),表明宰前高精料育肥诱导绵羊机体发生了氧化应激。值得注意的是,宰后成熟0~6 h期间,2 组羊肉样品的ROS含量均呈下降趋势,这可能是屠宰初期肌纤维进行无氧酵解消耗糖原所导致的[18]。宰后成熟6~120 h期间,2 组羊肉样品的ROS含量均呈上升趋势,但HC组始终高于PF组,且随着宰后成熟时间延长,2 组样品ROS含量差距逐渐缩小,在120 h达最小值,表明受到宰前氧化应激的影响,宰后成熟期间绵羊肌纤维也发生了一定程度的氧化应激。Fernandez-Turren等[19]在研究中也表达了类似的观点。
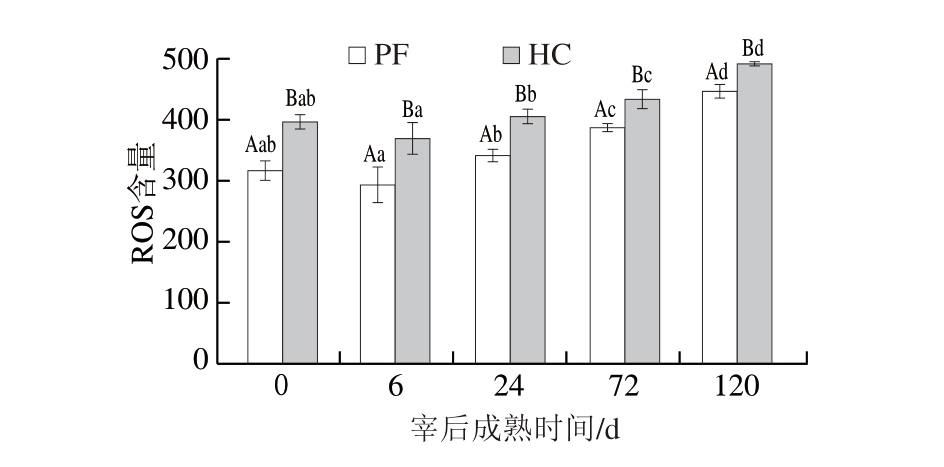
图3 宰后成熟期间绵羊肉ROS含量
Fig. 3 ROS content in lamb meat during postmortem aging
小写字母不同表示组内差异显著(P<0.05);大写字母不同表示组间差异显著(P<0.05)。图4~7同。
通常来说,宰后成熟期间,羊肉的pH值随时间的延长呈先下降到极限pH值后上升的趋势,直至成熟过程结束。如图4所示,2 组羊肉均在宰后成熟24 h达到极限pH值,但HC组的极限pH值显著低于PF组(P<0.05)。极限pH值是评价宰后肉品质的重要指标,较低的极限pH值会导致肉质量缺陷,如颜色变深、保水性降低和质构特性变差[20]。相反,较高的极限pH值可带来更高的保水性能和更好的嫩度,而肉的极限pH值受糖原含量、糖酵解通量、线粒体丰度、肌纤维氧化应激程度等多种因素调控[21]。
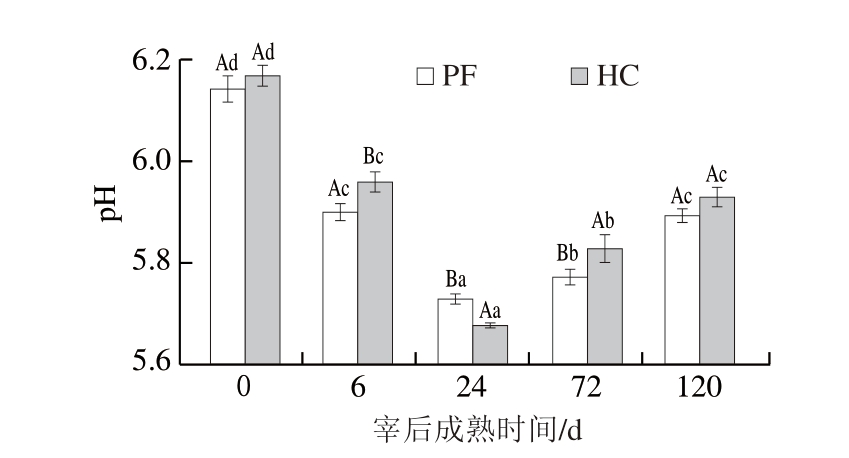
图4 宰后成熟期间绵羊肉pH值
Fig. 4 pH of lamb meat during postmortem aging
如图5所示,宰后成熟期间,HC组的羰基含量始终显著高于PF组,而总巯基含量始终显著低于PF组(P<0.05)。肌原纤维蛋白质骨架侧链上带有NH-或NH2-的氨基对ROS很敏感,在氧化过程中,这些基团易被氧化成羰基基团,因此羰基含量越高,表明蛋白质被氧化的程度越高[22]。而当发生氧化应激时,肌原纤维蛋白中的巯基易被ROS攻击,转化为二硫键、磺酸、亚磺酸及次磺酸,所以总巯基含量越低,表明蛋白质氧化程度越高[23]。结果表明,HC组的氧化应激程度比PF更严重。该结果在阿拉木苏[24]的饲养实验中也得到了印证。
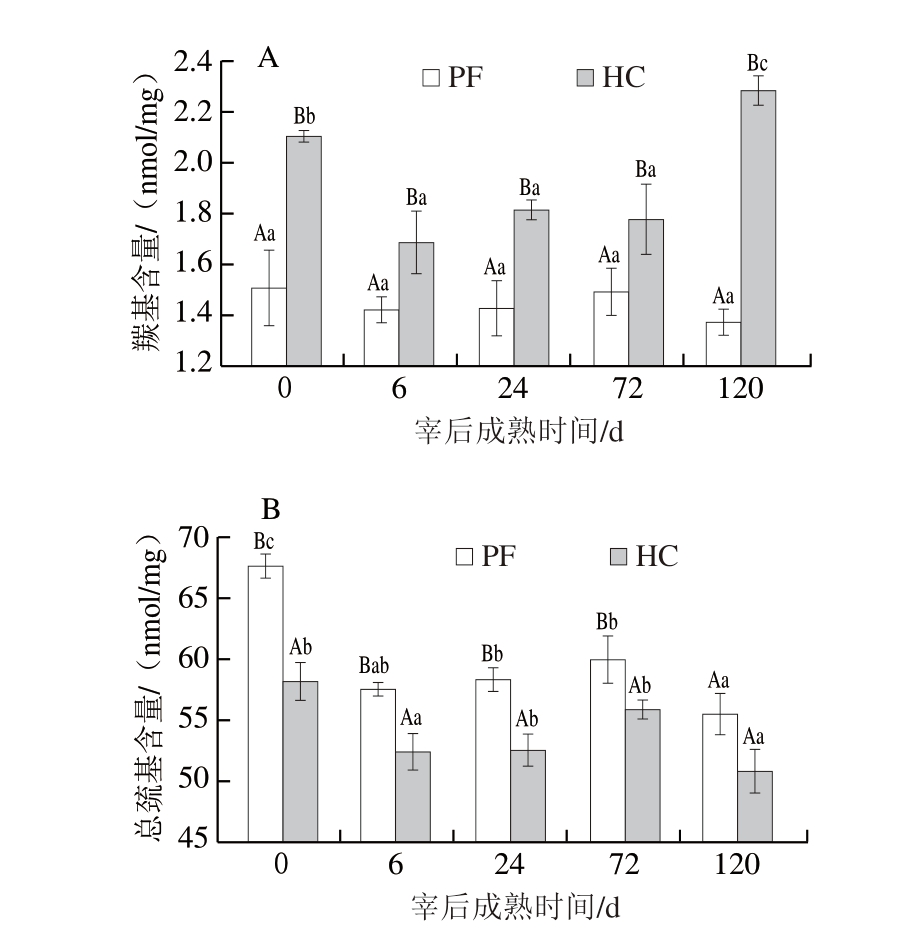
图5 宰后成熟期间绵羊肉羰基含量(A)与总巯基含量(B)
Fig. 5 Carbonyl content (A) and sulfhydryl content (B) in lamb meat during postmortem aging
TBARS值是衡量脂肪过氧化和氧化应激的指标[25],TBARS值越高,表明脂肪氧化程度越大。如图6所示,宰后成熟早期,2 组羊肉脂肪氧化程度差异并不明显,但宰后成熟24 h时,2 组羊肉脂肪的抗氧化能力出现显著差异(P<0.05),PF组的TBARS值还维持在较稳定的水平,而HC组在宰后成熟24 h后开始快速上升。肉中的脂肪氧化会产生多种负面影响,它可能导致肉腐臭异味的产生、肉色发生变化,以及肉嫩度和营养价值的降低[26]。上述结果说明,与PF组相比,HC组在宰后成熟过程中脂肪氧化更严重,更易对肉品质产生不利影响。
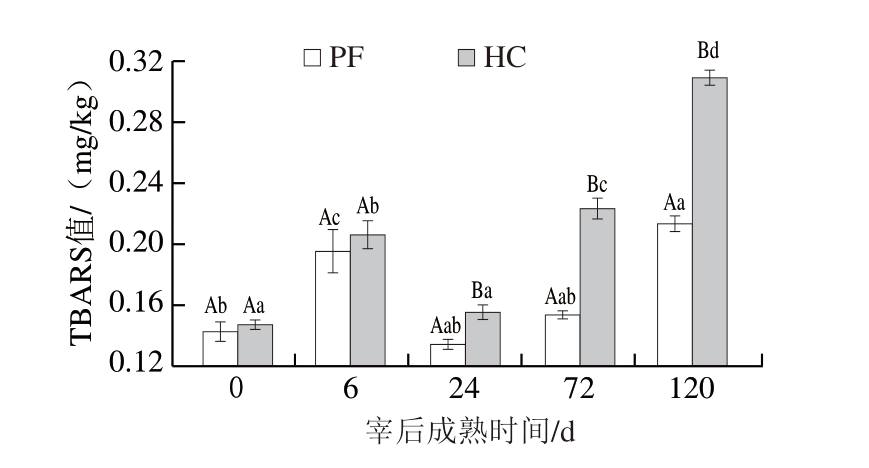
图6 宰后成熟期间绵羊肉TBARS值
Fig. 6 Thiobarbituric acid reactive substances (TBARS) value of lamb meat during postmortem aging
CAT、SOD、GSH-Px活性和T-AOC通常是用于评估肉类自身防止氧化反应以保持其品质能力的常用指标[27]。CAT、SOD和GSH-Px的活性反映肉中抗氧化酶的存在和有效性,它们有助于中和ROS并抵抗氧化应激。如图7所示,HC与PF组的SOD活性在宰后成熟72~120 h期间上升,HC组在宰后成熟6~24 h期间同样呈上升趋势,其余时间均下降,但在宰后成熟6、72、120 h时,HC组绵羊肉的SOD活性均显著低于PF组(P<0.05),这表明饲喂高精料导致宰后羊肉SOD活性降低。在整个宰后成熟过程中,PF组绵羊肉GSH-Px活性始终显著高于HC组(P<0.05),且均呈0~24 h平稳,24~120 h下降趋势。表明饲喂高精料导致宰后羊肉GSH-Px活性降低,特别是成熟后期。2 组羊肉的CAT活性在宰后成熟过程中的变化趋势一致,均为0~6 h时下降,6~24 h时上升,24~120 h时再次下降。但HC组的CAT活性始终低于PF组,这种差异在0、6、24 h显著(P<0.05);实验结果表明,饲喂高精料导致宰后羊肉CAT酶活性降低。T-AOC是衡量抗氧化剂在体内累积作用的指标,体现了酶类和非酶类抗氧化剂的总体水平,也体现出各抗氧化剂间的协同抗氧化的能力[28]。本研究中,HC组的T-AOC在宰后成熟期间始终低于PF组。宰后成熟期间,2 组样品T-AOC的变化趋势基本一致,在0~6 h时变化较为平稳,6~120 h时呈下降趋势,即随着宰后成熟时间延长,2 组羊肉样品的T-AOC逐渐下降。但从宰后成熟24 h开始,与PF组相比,HC组的T-AOC开始迅速下降,HC组绵羊肉的T-AOC在宰后成熟24~120 h期间降低52.94%,PF组只降低23.61%。结果表明,饲喂高精料介导的氧化应激导致羊肉的抗氧化能力变差且在宰后成熟后期迅速降低。
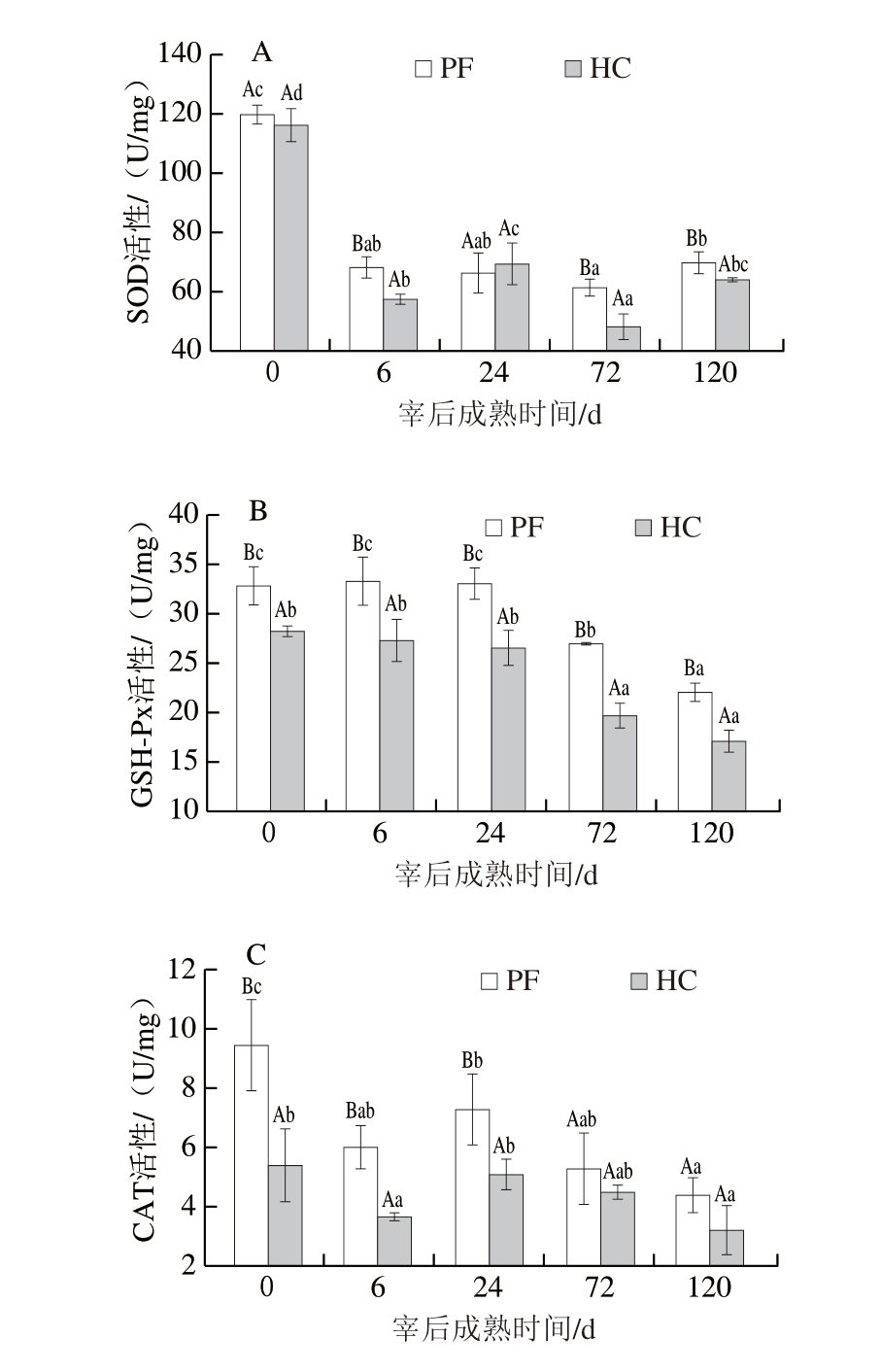
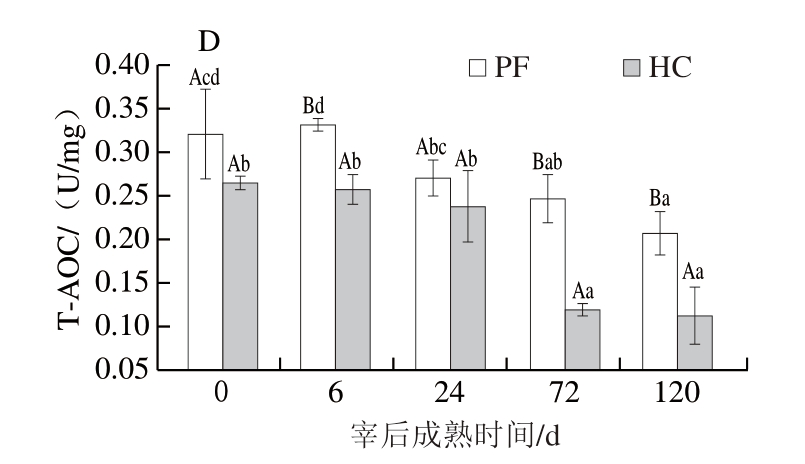
图7 宰后成熟期间绵羊肉SOD(A)、GSH-Px(B)、CAT活性(C)和T-AOC(D)
Fig. 7 SOD (A), GSH-Px (B), CAT activities (C) and T-AOC (D) of lamb meat during postmortem aging
宰后成熟6 h的ROS含量达最低值,宰后成熟24 h时的pH值是样品的极限pH值,而这2 个时间点也是CAT、SOD、GSH-Px活性变化的拐点。为此,进一步分析这2 个时间点酶活性的相关性(图8),发现宰后成熟6 h时,ROS含量与CAT、SOD、GSH-Px活性均呈负相关,而与宰后成熟24 h时的pH值并无很强的相关性。
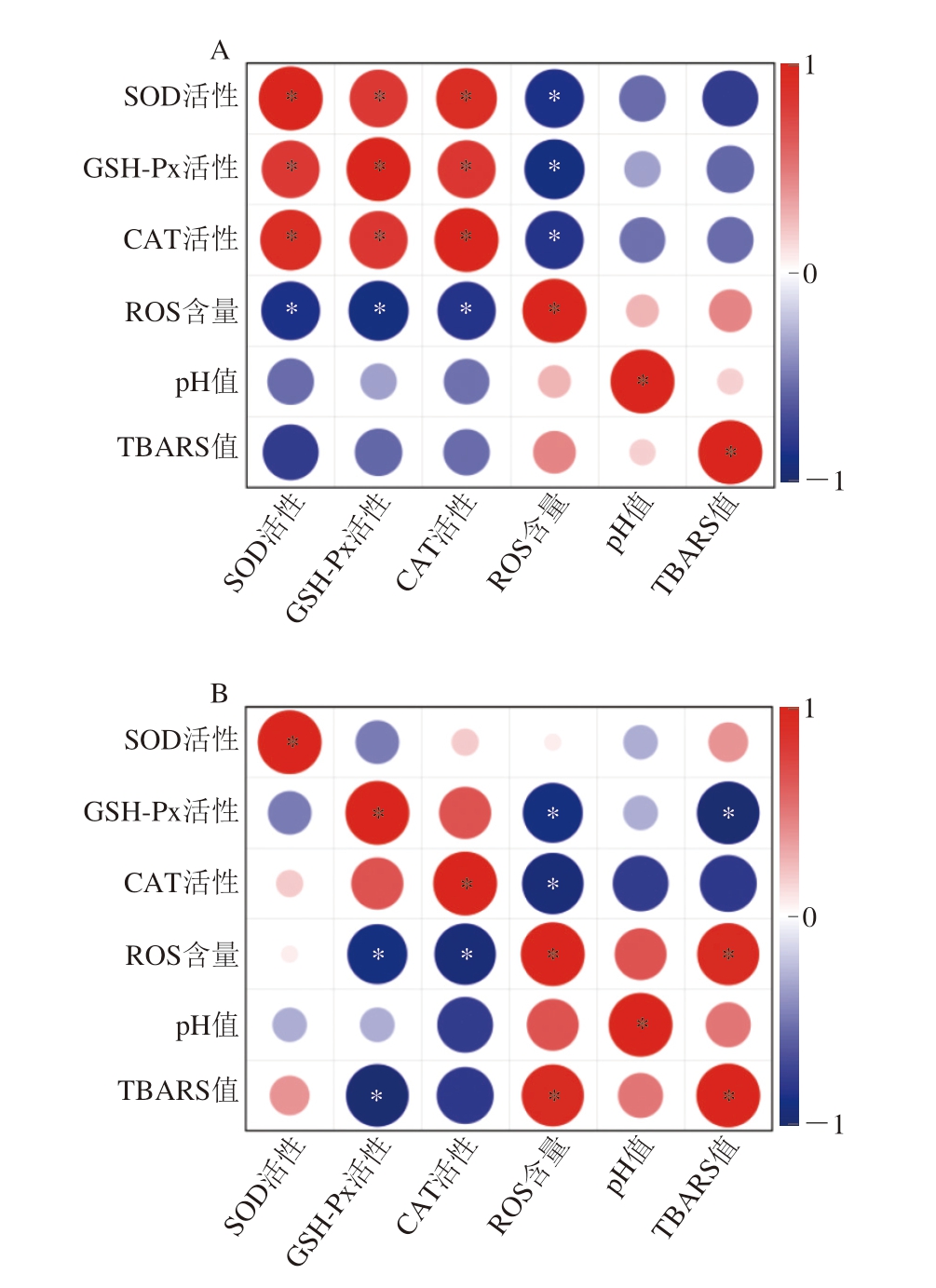
图8 宰后成熟6 h(A)和24 h(B)抗氧化酶活性与pH值、ROS含量、TBARS值的相关性分析
Fig. 8 Correlation analysis of antioxidant enzyme activities with pH,ROS content and TBARS value in lamb meat for 6 (A) and 24 h (B)postmortem aging
*.显著相关(P<0.05)。
SOD是细胞中对抗ROS介导损伤的第1道防线,当肌纤维因氧化应激而受损时,线粒体复合体功能失常,ROS大量产生时,SOD活性随之升高,它能将ROS中的超氧阴离子歧化为H2O2和O2[29]。当肌纤维内存在大量H2O2时,H2O2产生的ROS又通过降低CAT、SOD、GSH-Px活性产生部分丙二醛[30]。这可能解释了宰后成熟24 h的HC组SOD活性突然上升,但在72 h又下降的现象,是因为宰后成熟6~24 h期间,HC组肌纤维氧化应激受损更严重,促使SOD活性上升,大量歧化O2-,当产生过多H2O2时,反而抑制了SOD的活性。但为何PF组未发生明显变化及其具体机制还需后续实验进行验证。
GSH-Px是动物机体内广泛存在的一种在保护细胞免受ROS引起的氧化损伤方面起重要作用的过氧化物分解酶[31]。当机体发生氧化应激,第1道防线SOD启动时将ROS歧化为大量H2O2,但H2O2也具有强氧化性,会持续破坏肌纤维线粒体。此时线粒体内的GSH-Px发挥作用,将催化谷胱甘肽(glutathione,GSH)与H2O2发生反应,将其还原为H2O[32],同时GSH被氧化为氧化型GSH。因此GSH-Px的活性在一定程度上体现了机体抗氧化能力的强弱。结合本研究结果,表明饲喂高精料介导的氧化应激降低了绵羊肉宰后成熟过程中的抗氧化能力。
CAT是存在于细胞质和过氧化物酶体内的一种降解H2O2非常有效的高活性酶。但值得注意的是,大多数细胞线粒体缺乏CAT会导致线粒体中H2O2的降解效率低下,特别是在氧化应激条件下,产生的H2O2比正常条件下更多[33],这使GSH-Px-GSH系统在线粒体中降解H2O2时经常受到GSH水平的限制。当线粒体无法承受大量H2O2时,线粒体膜被破坏,将H2O2释放到细胞质中,此时肌纤维内的CAT活性提高[34]。这解释了本研究中,2 组样品宰后成熟6~24 h时CAT活性上升的现象。虽然CAT在氧化应激的主要场所线粒体中含量较低,但本研究结果也表明,宰后成熟过程中HC组肌纤维的CAT活性低于PF组,进一步表明饲喂高精料介导的氧化应激降低了绵羊肉宰后成熟过程中的抗氧化能力。
随着宰后成熟时间的延长,机体内的抗氧化酶系渐渐失活,肌肉的氧化稳定性也逐渐失衡,产生丙二醛、羰基等氧化产物。丙二醛是导致机体氧化应激和脂质过氧化的物质,通常被作为反映脂质氧化损伤程度的生物标志物[35]。本研究结果表明,HC组脂肪氧化更严重,且宰后成熟6~24 h时TBARS值下降,这也符合先前宰后成熟6~24 h时抗氧化酶活性提高的论证。
高精料育肥导致绵羊机体氧化应激产生ROS,宰后成熟过程中,ROS产生H2O2,通过降低CAT、SOD、GSH-Px活性产生丙二醛,导致绵羊肉氧化稳定性变差,绵羊肉中脂肪与蛋白质的氧化对肉品质造成负面影响。这些结果进一步支持了宰前氧化应激通过宰后成熟影响肉品质的假设,但宰后成熟过程中ROS对抗氧化酶的影响、极限pH值与氧化应激的关系仍需进一步探究。
[1] 呼日, 李春冬, 徐伟良, 等. 放牧型和舍饲型羊肉感官特征的差异性分析[J]. 农业与技术, 2025, 45(4): 111-116. DOI:10.19754/j.nyyjs.20250228023.
[2] 王莉, 魏健, 吴斌, 等. 饲养方式对牦牛肌肉脂肪酸组成和挥发性风味物质的影响研究进展[J]. 动物营养学报, 2025, 37(1): 87-100.
[3] ZHANG Q Y, QUE M, LI W, et al. Gangba sheep in the Tibetan Plateau: validating their unique meat quality and grazing factor analysis[J]. Journal of Environmental Sciences, 2021, 101: 117-122.DOI:10.1016/j.jes.2020.06.024.
[4] BEHAN A A, AKHTAR M T, LOH T C, et al. Meat quality, fatty acid content and NMR metabolic profile of dorper sheep supplemented with bypass fats[J]. Foods, 2021, 10(5): 1133. DOI:10.3390/foods10051133.
[5] 牟春堂. 葡萄籽原花青素缓解高精料致绵羊结肠炎症损伤及其作用机制[D]. 晋中: 山西农业大学, 2021. DOI:10.27285/d.cnki.gsxnu.2021.000818.
[6] LIANG Y X, BAO Y J, GAO X X, et al. Effects of Spirulina supplementation on lipid metabolism disorder, oxidative stress caused by high-energy dietary in Hu sheep[J]. Meat Science, 2020, 164:108094. DOI:10.1016/j.meatsci.2020.108094.
[7] DOU L, LIU C, YANG Z H, et al. Effects of oxidative stability variation on lamb meat quality and flavor during postmortem aging[J].Journal of Food Science, 2022, 87(6): 2578-2594. DOI:10.1111/1750-3841.16138.
[8] CARVALHO R H, IDA E I, MADRUGA M S, et al. Collapse of the endogenous antioxidant enzymes in post-mortem broiler thigh muscles triggers oxidative stress and impairs water-holding capacity[J].Journal of Food Science and Technology, 2019, 56(3): 1371-1379.DOI:10.1007/s13197-019-03611-1.
[9] HUANG Y X, SARKHEL S, ROY A, et al. Interrelationship of lipid aldehydes (MDA, 4-HNE, and 4-ONE) mediated protein oxidation in muscle foods[J]. Critical Reviews in Food Science and Nutrition,2024, 64(32): 11809-11825. DOI:10.1080/10408398.2023.2245029.
[10] 张玉林, 曹锦轩, 潘道东, 等. 成熟过程中活性氧簇(ROS)对肌原纤维蛋白结构的影响[J]. 现代食品科技, 2014, 30(9): 26-32; 108.DOI:10.13982/j.mfst.1673-9078.2014.09.005.
[11] 丁红艳, 院珍珍, 闫光瑾, 等. 不同生物保鲜剂对藏羊肉反复冻融过程中氧化的抑制作用[J]. 食品工业科技, 2025, 46(7): 301-307.DOI:10.13386/j.issn1002-0306.2024050028.
[12] 徐一焜, 张文燕, 张一敏, 等. 生鲜红肉发色特性及其调控机制的研究进展[J]. 食品科学, 2025, 46(8): 336-345. DOI:10.7506/spkx1002-6630-20241018-112.
[13] RUEDT C, GIBIS M, WEISS J. Meat color and iridescence:origin, analysis, and approaches to modulation[J]. Comprehensive Reviews in Food Science and Food Safety, 2023, 22(4): 3366-3394.DOI:10.1111/1541-4337.13191.
[14] SADRARHAMI I, ALIKHANI M, GHASEMI E, et al. Effects of nomadic grazing system and indoor concentrate feeding systems on performance, behavior, blood parameters, and meat quality of finishing lambs[J]. PLoS ONE, 2022, 17(12): e0278669. DOI:10.1371/journal.pone.0278669.
[15] 刘梦静, 郭军, 闫鑫磊, 等. 内蒙古放牧和舍饲绵羊肉的脂肪酸特征[J]. 肉类研究, 2020, 34(6): 38-44. DOI:10.7506/rlyj1001-8123-20200429-110.
[16] 李春冬, 刘国强, 呼日, 等. 锡林郭勒不同地区羊肉矿物质元素比较分析[J]. 食品安全质量检测学报, 2024, 15(19): 131-137.DOI:10.19812/j.cnki.jfsq11-5956/ts.20240725001.
[17] ÖNDER N T, BATI Y U, GÖKDEMIR T, et al. Oxidative response of sheep to transcervical applications[J]. Zuchthygiene, 2023, 58(6): 877-881. DOI:10.1111/rda.14361.
[18] ENGLAND E M, SCHEFFLER T L, KASTEN S C, et al.Exploring the unknowns involved in the transformation of muscle to meat[J]. Meat Science, 2013, 95(4): 837-843. DOI:10.1016/j.meatsci.2013.04.031.
[19] FERNANDEZ-TURREN G, REPETTO J L, ARROYO J M, et al.Lamb fattening under intensive pasture-based systems: a review[J].Animals, 2020, 10(3): 382. DOI:10.3390/ani10030382.
[20] BEAUCLERCQ S, MIGNON-GRASTEAU S, PETIT A, et al.A divergent selection on breast meat ultimate pH, a key factor for chicken meat quality, is associated with different circulating lipid profiles[J]. Frontiers in Physiology, 2022, 13: 935868. DOI:10.3389/fphys.2022.935868.
[21] BALDI G, YEN C N, DAUGHTRY M R, et al. Exploring the factors contributing to the high ultimate pH of broiler pectoralis major muscles affected by wooden breast condition[J]. Frontiers in Physiology, 2020,11: 343. DOI:10.3389/fphys.2020.00343.
[22] CAKATAY U, TELCI A, KAYALI R, et al. Relation of aging with oxidative protein damage parameters in the rat skeletal muscle[J].Clinical Biochemistry, 2003, 36(1): 51-55. DOI:10.1016/s0009-9120(02)00407-1.
[23] HILLION M, BERNHARDT J, BUSCHE T, et al. Monitoring global protein thiol-oxidation and protein S-mycothiolation in Mycobacterium smegmatis under hypochlorite stress[J]. Scientific Reports, 2017, 7(1):1195. DOI:10.1038/s41598-017-01179-4.
[24] 阿拉木苏. 舍饲和放牧对阿尔巴斯绒山羊生长发育、抗氧化能力及免疫功能的影响[D]. 呼和浩特: 内蒙古农业大学, 2023.DOI:10.27229/d.cnki.gnmnu.2023.001372.
[25] 宋瑞晗, 马艳秋, 迟玉杰, 等. 蛋黄粉在加速贮藏过程中的脂质氧化及保质期预测[J]. 食品科学, 2023, 44(21): 193-203. DOI:10.7506/spkx1002-6630-20221005-033.
[26] 葛迎港, 崔柯鑫, 陈慧, 等. 3种抗氧化剂处理对干制鲅鱼脂肪氧化和挥发性风味成分的影响[J]. 肉类研究, 2023, 37(4): 21-28.DOI:10.7506/rlyj1001-8123-20230110-002.
[27] ECHEGARAY N, PATEIRO M, MUNEKATA P E S, et al.Measurement of antioxidant capacity of meat and meat products:methods and applications[J]. Molecules, 2021, 26(13): 3880.DOI:10.3390/molecules26133880.
[28] WANG B, XU C C, LIU C, et al. The effect of dietary lycopene supplementation on drip loss during storage of lamb meat by iTRAQ analysis[J]. Antioxidants, 2021, 10(2): 198. DOI:10.3390/antiox10020198.
[29] ZHAO H Q, ZHANG R F, YAN X Y, et al. Superoxide dismutase nanozymes: an emerging star for anti-oxidation[J]. Journal of Materials Chemistry B, 2021, 9(35): 6939-6957. DOI:10.1039/d1tb00720c.
[30] WANG L L, YU Q L, HAN L, et al. Study on the effect of reactive oxygen species-mediated oxidative stress on the activation of mitochondrial apoptosis and the tenderness of yak meat[J]. Food Chemistry, 2018, 244: 394-402. DOI:10.1016/j.foodchem.2017.10.034.
[31] LIU C, LI B Z, YAN Q, et al. Protective effects and mechanisms of recombinant human glutathione peroxidase 4 on isoproterenol-induced myocardial ischemia injury[J]. Oxidative Medicine and Cellular Longevity, 2021, 2021(1): 6632813. DOI:10.1155/2021/6632813.
[32] 王宣懿, 许师源, 于海波, 等. 维生素E对热应激雏鸡血清NO含量及GSH-Px活性的影响[J]. 当代畜牧, 2020(5): 10-12.
[33] BAI J, CEDERBAUM A I. Mitochondrial catalase and oxidative injury[J]. Biological Signals & Receptors, 2001, 10(3/4): 189-199.DOI:10.1159/000046887.
[34] XU H Y, RANJIT R, RICHARDSON A, et al. Muscle mitochondrial catalase expression prevents neuromuscular junction disruption,atrophy, and weakness in a mouse model of accelerated sarcopenia[J].Journal of Cachexia, Sarcopenia and Muscle, 2021, 12(6): 1582-1596.DOI:10.1002/jcsm.12768.
[35] 南国荣, 郑彦楷, 陈宇, 等. 沙葱多糖对敌草快攻毒小鼠抗氧化功能的影响及其机制[J]. 饲料研究, 2025, 48(8): 67-72. DOI:10.13557/j.cnki.issn1002-2813.2025.08.012.