在中国传统饮食中,鸭血既是川渝经典菜肴“毛血旺”的核心食材,也是南京“鸭血粉丝汤”的核心食材。研究[1]表明,鸭血不仅蛋白质含量高而且富含多种人体必需氨基酸。近年来,国内食品市场上鸭血制品掺假现象屡禁不止,严重威胁食品安全与消费者信任[2]。由于鸭血产量低且市场需求旺盛,部分商家为牟取利益,常以猪血、鸡血等低价动物血液替代或掺杂鸭血制品,甚至通过添加工业色素(如亮红)及凝固剂(如阿拉伯胶)模拟鸭血的色泽与质地[1,3-4]。这些掺假行为不仅严重侵害了消费者权益,还可能引发过敏反应或肝肾损伤[5]。因此,建立快速、准确的鸭血制品中异源性动物成分检测方法,对保障公众健康、规范市场秩序具有重要意义[6]。
基于DNA扩增原理的聚合酶链式反应(polymerase chain reaction,PCR)技术现已成为食品检测领域物种源性鉴定的重要分析方法[4]。目前,鸭成分检测主要采用普通PCR和实时荧光定量PCR(real-time fluorescence quantitative PCR,real-time PCR)2 种方法[7],其中real-time PCR凭借高效、灵敏的特点,已广泛应用于肉类成分检测,尤其在物种特异性分析中具有显著优势[7-10]。对于鸭源性成分检测,目前国内相关的检测标准包括SB/T 10923—2012《肉及肉制品中动物源性成分的测定 实时荧光PCR法》[11]、SN/T 2727—2010《饲料中禽源性成分检测方法 实时荧光PCR方法》[12]、BJS 202309《鸭血中鸭鸡鹅源性成分的测定》[13]、GB/T 38164—2019《常见畜禽动物源性成分检测方法 实时荧光PCR法》[14]和BJS 201904《食品中多种动物源性成分检测实时荧光PCR法》[15]。然而,上述方法需针对不同物种靶标基因进行多次独立扩增,难以实现大批量样品中多源性成分的同步快速检测,导致检测效率低下且成本高昂。相较于传统的单通道real-time PCR检测体系,新型多重real-time PCR检测体系通过优化引物设计策略和反应参数,可在单一扩增体系中实现多种动物源性成分的同步鉴别[2,16-20]。但是,目前多重real-time PCR方法也存在一些缺陷,例如,针对每种源性成分需独立设计特异性引物对及荧光探针,即一个物种源性检测需要3 条引物,当检测目标增至3 种以上时,反应体系中引物浓度累积易引发引物二聚体形成,导致非特异性扩增[21],而且多条引物的使用一定程度上也增加了实验成本。
针对上述问题,本研究聚焦鸭血制品中常见的猪血与鸡血掺假现象,开发了一种基于多重real-time PCR技术的检测方法,该方法针对所检测猪、鸡和鸭源性基因设计通用上下游引物,再根据物种基因特性设计针对物种特异性的分子信标探针,以减少引物数量。通过采集市售鸭血样品,利用所构建的多重real-time PCR体系进行检测分析,同时与GB/T 38164—2019方法进行比对,评价该方法对实际样品的检测能力,验证该方法的实际应用可行性。
1 材料与方法
1.1 材料与试剂
水牛肉、黄牛肉、山羊肉、绵羊肉、鹅肉、鸭肉、猪肉、猪血、鸡肉、鸡血、19 份市售散装新鲜鸭血样品(编号1~19,于-20 ℃冷冻保存备用)购于本地市场;牦牛肉、狐狸、犬、猫、马、鼠组织为本实验室冻存标本。
DNA提取试剂盒 德国Qiagen公司;TaqMan real-time PCR酶预混液 日本TaKaRa公司;引物和探针均由生工生物工程(上海)股份有限公司合成。
1.2 仪器与设备
CFX-96 real-time PCR仪 美国Bio-Rad公司;UV-1700紫外分光光度计 日本岛津公司;1-16K高速冷冻离心机 德国Sigma公司;TU-100C恒温金属浴 上海一恒科技有限公司;BSA224S电子天平 德国赛多利斯科学仪器有限公司。
1.3 方法
1.3.1 引物和探针设计
从GenBank数据库中下载猪、鸡和鸭线粒体基因组序列(基因序列号分别为KX982652.1、KY039437.1和NC_022418.1),使用DNAMAN软件对3 个物种的16S rDNA基因序列进行比对分析,采用SnapGene软件在该基因保守区域设计通用引物UN-F/R,并在可变区域内设计针对物种特异性的分子信标探针。内参引物(对)序列参照GB/T 38164—2019中真核生物18S rRNA引物序列[14],具体的引物和探针序列见表1。
表1 引物和探针序列
Table 1 Sequences of primers and probes used in this study
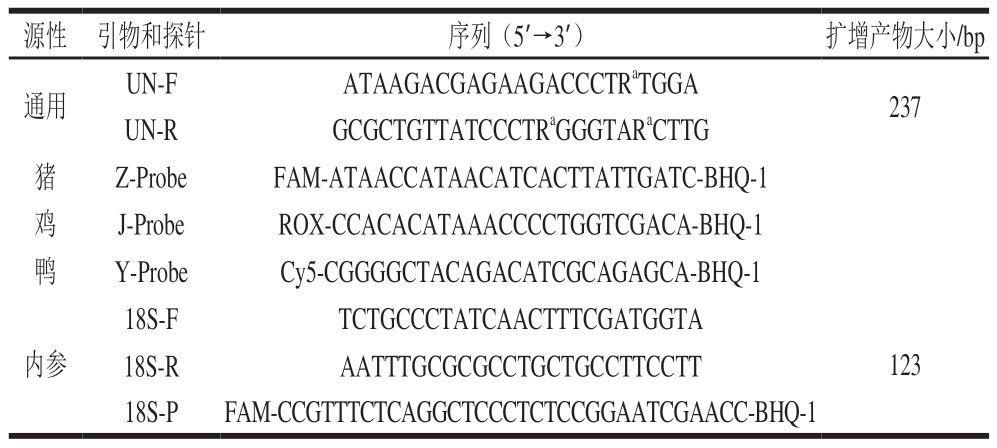
注:a.简并碱基,R=A/G;FAM.6-羧基荧光素(6-carboxyfluorescein);ROX.羧基-X-罗丹明(carboxy-X-rhodamine);Cy5.花青素5(cyanine 5);BHQ.黑洞猝灭剂(black hole quencher)。
源性 引物和探针序列(5’→3’)扩增产物大小/bp通用UN-FATAAGACGAGAAGACCCTRaTGGA237 UN-RGCGCTGTTATCCCTRaGGGTARaCTTG猪Z-ProbeFAM-ATAACCATAACATCACTTATTGATC-BHQ-1鸡J-ProbeROX-CCACACATAAACCCCTGGTCGACA-BHQ-1鸭Y-ProbeCy5-CGGGGCTACAGACATCGCAGAGCA-BHQ-1 18S-FTCTGCCCTATCAACTTTCGATGGTA内参123 18S-RAATTTGCGCGCCTGCTGCCTTCCTT 18S-PFAM-CCGTTTCTCAGGCTCCCTCTCCGGAATCGAACC-BHQ-1
1.3.2 DNA提取及浓度、纯度的测定
采用DNA提取试剂盒对肉组织及血制品样品依据试剂盒操作说明提取DNA,使用紫外分光光度计分别测定其在260 nm和280 nm波长处的光密度(OD260 nm和OD280 nm)。DNA质量浓度按式(1)计算:
计算OD260 nm/OD280 nm,当该比值介于1.8~2.0之间时,表明所提取的DNA模板纯度较高,质量满足后续实验要求。随后,对各样品中的DNA模板进行倍比稀释,评估该检测体系的灵敏度。
1.3.3 鸭肉和鸭血制品模拟掺假样品的制备
为验证检测方法对不同基质样品的适用性及差异,本研究设计2 种类型的模拟掺假样品体系:1)选取鸭肉作为基础基质,制备生肉掺假模型;2)采用市售纯鸭血制备血制品掺假模型。此设计基于以下双重考虑:生肉掺假模型在理想条件下验证方法的核心灵敏度,规避血制品复杂基质(凝固剂、色素等添加物)对检测结果的干扰;血制品掺假模型则评估该方法在真实血制品样品中的技术适用性。生肉模拟掺假样品制备参照范维等[16]的方法:分别以鸭肉为本底,独立制备鸭肉-猪肉、鸭肉-鸡肉2 种二元模拟掺假样品,对于每种掺假成分均设置100.00%、10.00%、1.00%、0.10%、0.01%共5 个质量分数梯度。同理,以市售纯鸭血为本底,参照上述方法分别制备掺入猪血、鸡血的鸭血模拟掺假样品,并设置100.00%、10.00%、1.00%、0.10%、0.01% 5 个质量分数梯度。每组混合样品设10 个平行。
1.3.4 多重real-time PCR体系的建立及优化
多重real-time PCR体系:DNA模板(质量浓度为20~100 ng/μL)2 μL、2×Premix Ex Taq 12.5 μL、UN-F/UN-R(10 μmol/μL)0.5 μL、Z-Probe(FAM)(10 μmol/μL)1.0 μL、J-Probe(ROX)(10 μmol/μL)1.0 μL、Y-Probe(Cy5)(10 μmol/μL)1.0 μL,去离子水补足至25 μL。
以建立好的反应体系摸索PCR最佳退火温度,将退火温度分别设置为55、58、60、62、64 ℃进行优化测试,反应程序如下:95 ℃、30 s预变性;随后进行40 个循环的扩增,每个循环包括95 ℃、5 s的变性步骤及30 s的退火/延伸/荧光信号收集步骤,每个温度设置2 个平行,根据PCR扩增曲线特征参数(包括循环阈(cycle threshold,Ct)值、相对荧光强度、扩增效率、曲线线型)及反应耗时等指标进行综合分析,确定最佳退火温度。
1.3.5 多重real-time PCR方法特异性验证
选取14 种典型动物(牦牛、水牛、黄牛、山羊、绵羊、猪、鸡、鸭、鹅、狐狸、犬、猫、马、鼠)的肌肉样本进行基因组DNA提取。基于前期构建的多重realtime PCR检测体系,对上述14 个DNA样品分别进行检测分析,综合评价该方法的物种鉴别特异性。
1.3.6 多重real-time PCR方法灵敏度测定
分别测定所提取的猪、鸡、鸭3 种样品的DNA模板质量浓度,基于倍比稀释原理,分别将猪、鸡、鸭3 种样品的DNA经5 倍连续稀释,质量浓度为0.04~1 000 ng/μL。用建立的多重real-time PCR检测体系对不同质量浓度样品分别进行检测,每个反应体系加入2 μL DNA模板,各质量浓度设置6 个平行样,记录PCR扩增Ct值。以DNA质量浓度对数值为横坐标、Ct值为纵坐标绘制标准曲线,扩增效率按式(2)计算,评估该检测体系的灵敏度。
式中:k为标准曲线斜率。
1.3.7 多重real-time PCR方法检出限测定
取上述制备好的不同掺入比例的混合肉及血制品,按照基因组试剂盒说明书进行DNA提取,不同掺入比例的10 个平行样采用本实验建立的多重real-time PCR方法进行检测。在10 次平行实验中,规定10 次结果均检出时的最低质量分数为该目标源性成分的检出限[22]。
1.3.8 市售样品测定
利用本研究建立的多重real-time PCR方法与国标(GB/T 38164—2019)方法分别对19 份不同来源的市售鸭血样品进行检测,验证方法的实用性,同时了解市场上鸭血制品的掺假情况。
1.4 数据处理
样品Ct值通过Bio-Rad CFX Manager分析软件(v3.0)获取。数据的整理与分析基于Microsoft Excel软件,实验结果以平均值±标准差表示。图表绘制采用Microsoft PowerPoint软件完成。
2 结果与分析
2.1 PCR退火温度的优化结果
由图1可知,猪、鸡、鸭3 种目标源性成分 在退火温度55~64 ℃范围内均有典型扩增曲线。退火温度在55~60 ℃区间时,各通道(FAM、ROX、Cy5)扩增曲线形态典型,Ct值相对稳定。当退火温度升至62~64 ℃时,可观察到扩增曲线出现 显著右移及平台期荧光信号强度降低 的特征,表明退火温度过高导致引物与模板结合效率下降,从而引起扩增效率降低。尽管55 ℃或58 ℃也能产生良好的扩增信号,但在多重real-time PCR体系中,多种引物和探针并存,更高的退火温度(60 ℃)在保持高效扩增的同时能提供更高的反应特异性和信号稳健性,有利于减少多重real-time PCR中非特异性扩增风险。因此,选择60 ℃作为后续研究的退火温度。
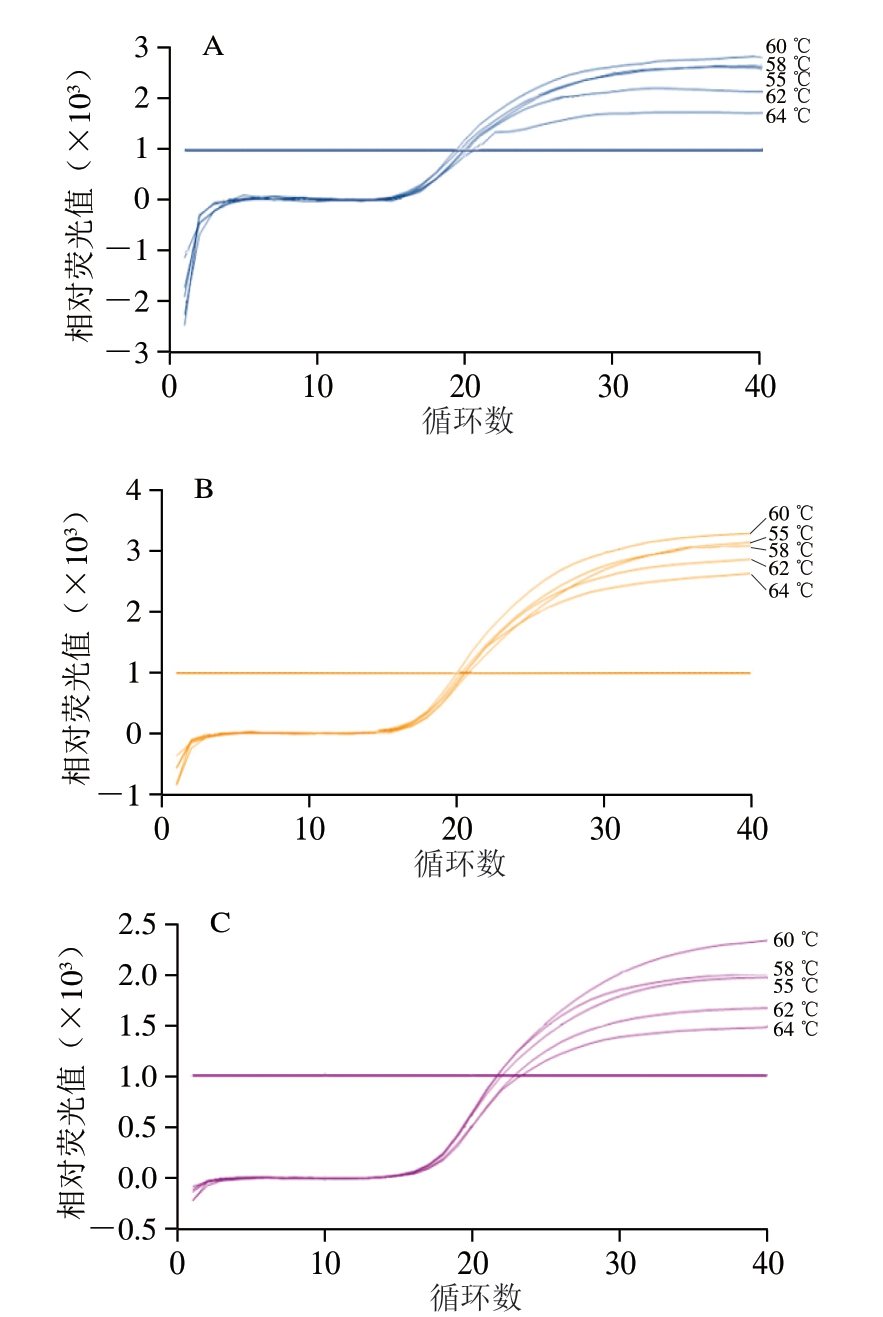
图1 不同退火温度对real-time PCR结果的影响
Fig.1 Effect of different annealing temperatures on the results of real-time PCR
A.FAM通道(猪源);B.ROX通道(鸡源);C.Cy5通道(鸭源)。图3同。
2.2 多重real-time PCR方法特异性实验结果
如图2所示,只有猪、鸡、鸭的DNA样品出现相应扩增曲线,其他物种样品均无扩增曲线,表明该体系具有良好的特异性,能有效从常见肉类中鉴别出目标源性成分。
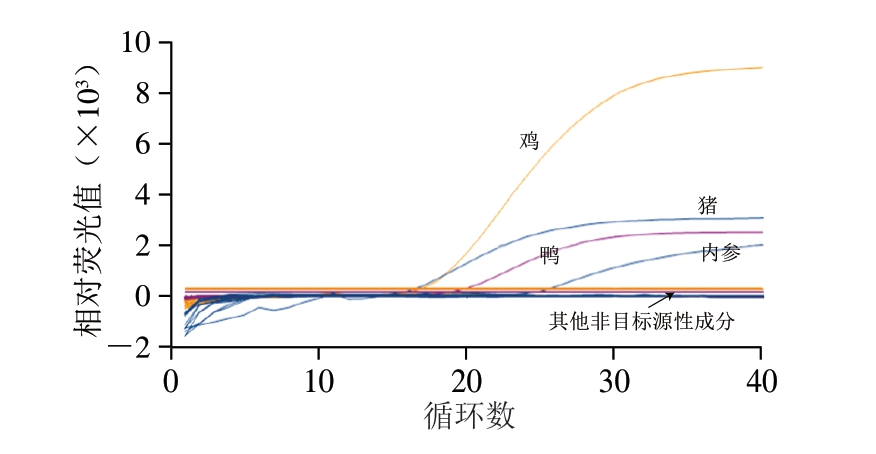
图2 多重real-time PCR体系特异性验证结果
Fig.2 Results of specificity validation of multiple real-time PCR systems
2.3 多重real-time PCR灵敏度测定结果
如图3所示,基于多重real-time PCR体系的灵敏度分析表明,当猪、鸡源性DNA质量浓度≥0.04 ng/μL时,体系能够检出对应源性成分;鸭源性成分的检出临界值则为0.06 ng/μL。通过梯度质量浓度验证,本研究最终确定该检测方法的灵敏度为0.06 ng/μL。
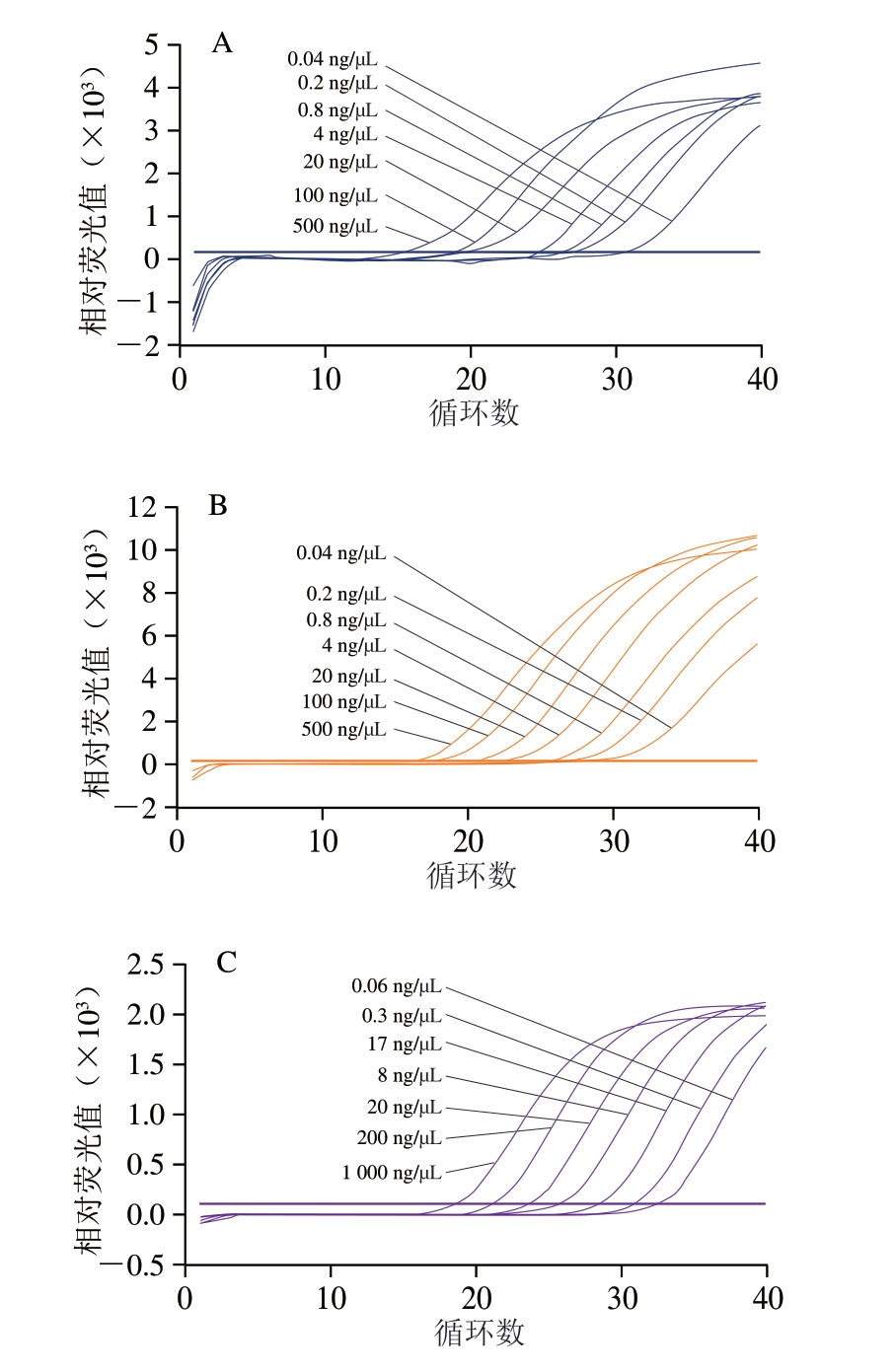
图3 多重real-time PCR体系灵敏度测定结果
Fig.3 Results of sensitivity validation of multiple real-time PCR systems
如图4 所示,3 种源性(猪、鸡、鸭)D N A 在0.04~1 000 ng/μL内均呈现稳定的线性关系,猪源性DNA的标准曲线方程为y=-3.561 7x+25.694(R2=0.999 7),扩增效率为90.9%;鸡源性DNA的标准曲线方程为y=-3.279 6x+25.039(R2=0.996 7),扩增效率为101.9%;鸭源性DNA的标准曲线方程为y=-3.513 8x+26.278(R2=0.998 7),扩增效率为92.2%。3 种源性DNA扩增效率均在90%~110%之间,平均扩增效率为95.0%(R2>0.980),扩增效率良好,实验数据可靠。上述结果表明,该多重real-time PCR方法对低质量浓度掺假成分的检测具有高灵敏度和可靠性。
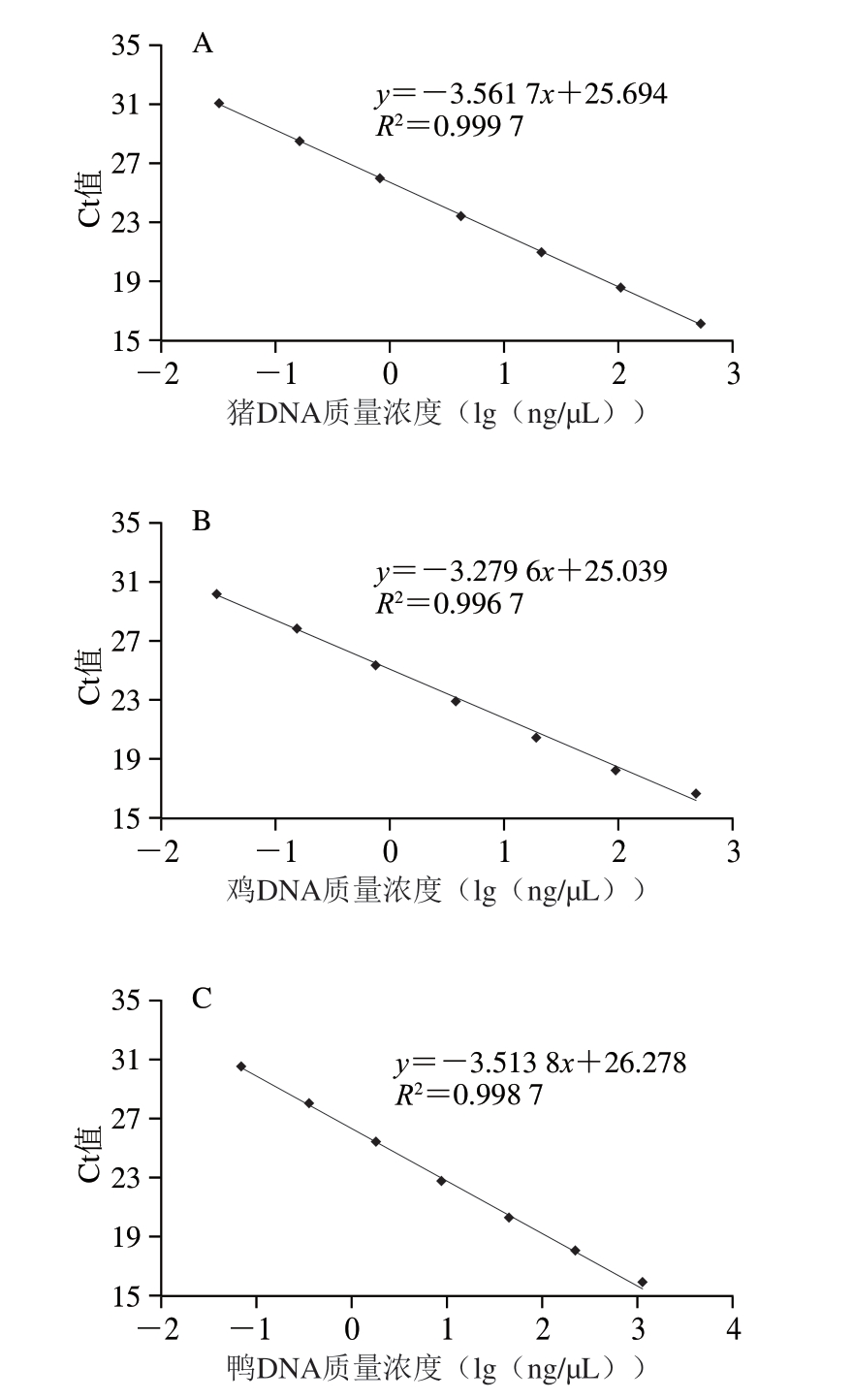
图4 猪(A)、鸡(B)和鸭源性成分(C)定量检测标准曲线
Fig.4 Standard curves for quantitative detection of pig- (A), chicken- (B), and duck-derived components (C)
2.4 鸭肉及鸭血制品掺假检出限的确定
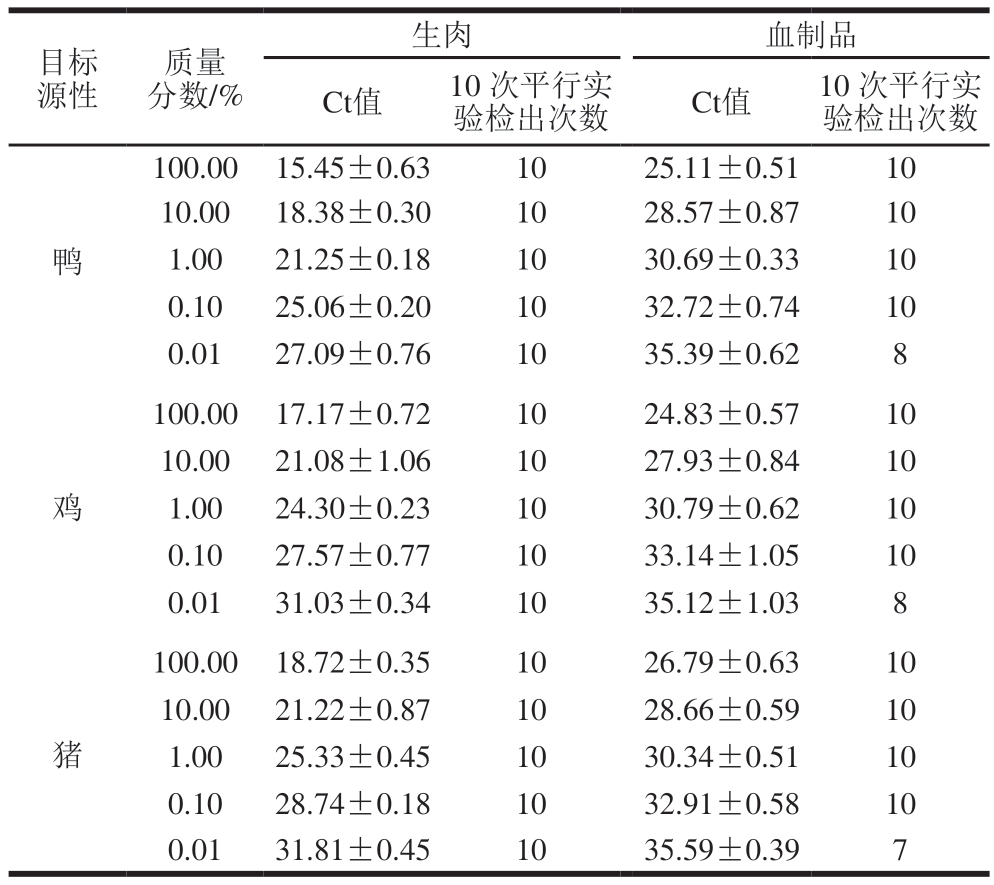
为科学评估本研究对不同样品基质检测效能的差异化影响,分别构建生鲜肉基质与深加工血制品基质2 类实验模型。通过构建的鸭源性成分梯度掺假模型,验证该检测方法对鸭肉及鸭血制品的适用性及差异。如表2所示,不同掺假比例的鸭肉及鸭血样品中,源性成分Ct值与质量分数呈显著负相关(R2>0.980)。当鸭源性成分质量分数从100.00%降至0.01%时,生肉样品Ct值由15.45±0.63升至27.09±0.76,血制品则由25.11±0.51升至35.39±0.62,鸡源性和猪源性成分也呈现出类似的趋势。此外,对比生肉和血制品,在相同掺入比例下,血制品的Ct值普遍高于生肉,推测可能是由于血制品的成分相对复杂,对检测造成一定干扰。综合各目标源性成分在不同质量分数下的检测结果,在生肉中,当掺入质量分数为0.01%时,各源性成分Ct值虽有升高但仍能检测到;而在血制品中,当掺入质量分数为0.10%时检测情况相对较好,当降至0.01%时Ct值较高,检测难度明显增大。基于此定量关系,现规定该检测体系对生肉样品的检出限为0.01%(95%置信水平),而对血制品中目标成分的检出限则为0.10%(95%置信水平)。
表2 多重real-time PCR对掺假鸭肉及鸭血制品的测定结果
Table 2 Results of multiple real-time PCR detection of adulterated duck meat and duck blood products
目标源性质量分数/%生肉血制品Ct值10 次平行实验检出次数Ct值10 次平行实验检出次数鸭100.00 15.45±0.631025.11±0.5110 10.00 18.38±0.301028.57±0.8710 1.0021.25±0.181030.69±0.3310 0.1025.06±0.201032.72±0.7410 0.0127.09±0.761035.39±0.628鸡100.00 17.17±0.721024.83±0.5710 10.00 21.08±1.061027.93±0.8410 1.0024.30±0.231030.79±0.6210 0.1027.57±0.771033.14±1.0510 0.0131.03±0.341035.12±1.038猪100.00 18.72±0.351026.79±0.6310 10.00 21.22±0.871028.66±0.5910 1.0025.33±0.451030.34±0.5110 0.1028.74±0.181032.91±0.5810 0.0131.81±0.451035.59±0.397
2.5 市售鸭血的测定结果
如表3所示,对19 份市售鸭血样品进行平行测定,本研究构建的多重real-time PCR方法与GB/T 38164—2019方法均能有效检出猪、鸡、鸭源性成分。其中,检出猪源性成分的样品1 份(检出率5.26%)、检出鸡源性成分的样品11 份(检出率57.89%)、检出鸭源性成分的样品12 份(检出率63.16%),其中5 份(占比26.32%)样品同时存在鸡/鸭源性成分。从检测结果的Ct值来看,本方法各目标源性成分的Ct值较GB/T 38164—2019方法平均降低2.3±0.7,这说明本实验方法能够更快速、更灵敏地检测到样品中的目标源性成分。总体上,2 种方法的检测结果高度一致,表明本实验所建立的方法结果可靠,可用于市售鸭血样品中常见掺假源性成分的检测。
表3 不同检测方法对19 份市售鸭血的Ct值检测结果
Table 3 Cycle threshold results of detection of 19 commercially available duck blood samples by different methods
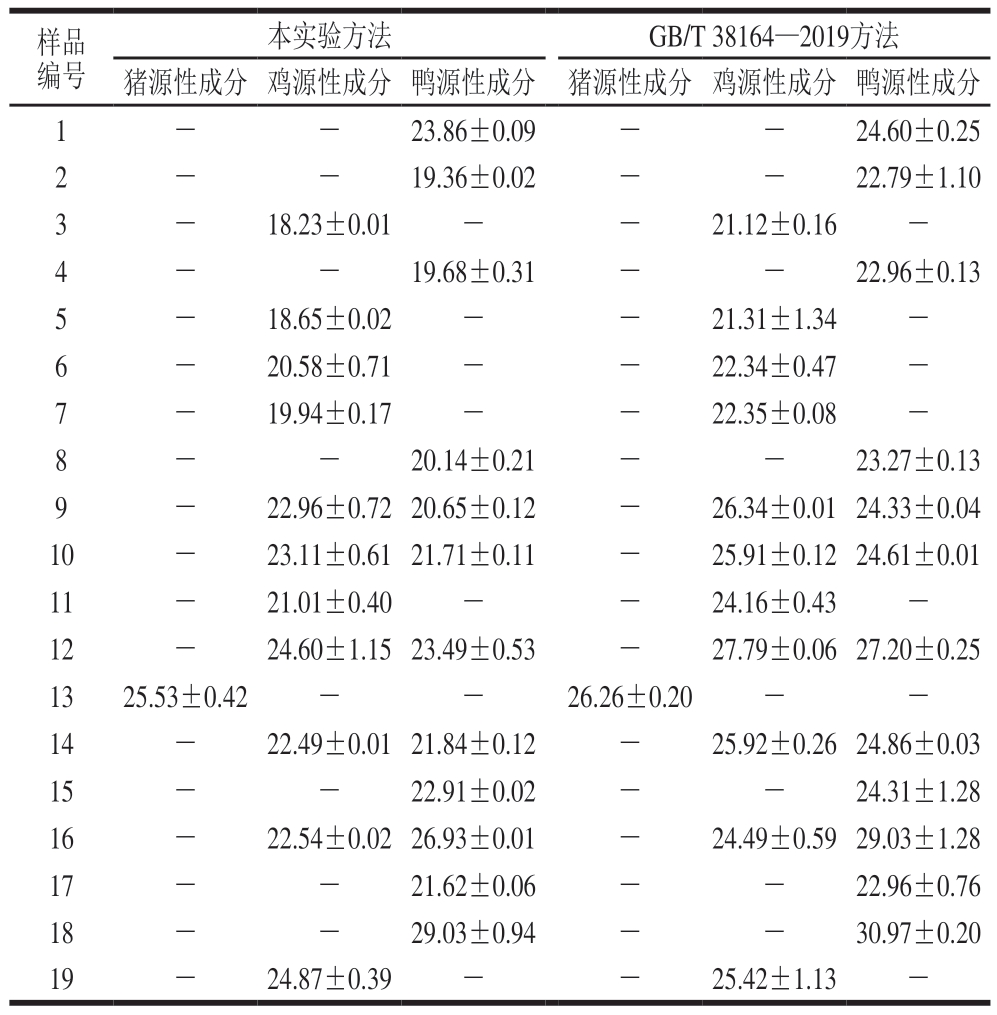
注:-.未检测到荧光信号。
本实验方法GB/T 38164—2019方法猪源性成分 鸡源性成分 鸭源性成分 猪源性成分 鸡源性成分 鸭源性成分1--23.86±0.09--24.60±0.25 2--19.36±0.02--22.79±1.10 3-18.23±0.01--21.12±0.16-4--19.68±0.31--22.96±0.13 5-18.65±0.02--21.31±1.34-6-20.58±0.71--22.34±0.47-7-19.94±0.17--22.35±0.08-8--20.14±0.21--23.27±0.13 9-22.96±0.72 20.65±0.12-26.34±0.01 24.33±0.04 10-23.11±0.61 21.71±0.11-25.91±0.12 24.61±0.01 11-21.01±0.40--24.16±0.43-12-24.60±1.15 23.49±0.53-27.79±0.06 27.20±0.25 1325.53±0.42--26.26±0.20--14-22.49±0.01 21.84±0.12-25.92±0.26 24.86±0.03 15--22.91±0.02--24.31±1.28 16-22.54±0.02 26.93±0.01-24.49±0.59 29.03±1.28 17--21.62±0.06--22.96±0.76 18--29.03±0.94--30.97±0.20 19-24.87±0.39--25.42±1.13-样品编号
3 讨 论
近年来,鸭血制品掺假时有报道,已成为食品安全的突出问题[1,5,23-24]。多重real-time PCR技术因其高通量、高灵敏度和特异性等优势,在肉类掺假检测中展现出重要应用价值[25-27]。传统单靶标PCR方法受限于检测通量和操作效率,难以满足复杂基质中多物种源性成分的同步鉴别需求[6-7,28-31]。本研究基于TaqMan探针技术,成功构建了1 种多重real-time PCR检测方法,实现了鸭血制品中猪、鸡、鸭源性成分的同步鉴别。该方法的核心策略是利用1 对靶向猪、鸡、鸭线粒体16S rDNA保守区的通用引物(UN-F/R)进行同步扩增,并在其可变区设计并应用分别标记FAM、ROX、Cy5荧光基团的物种特异性探针(Z-Probe、J-Probe、Y-Probe)进行精准识别。该策略相比传统多重real-time PCR方法(通常每个物种需要1 对引物和1 条探针)显著简化了反应体系,引物总数由9 条缩减至5 条,有效规避了多对引物共存可能引发的引物二聚体形成及荧光信号干扰风险。引物特异性实验表明,该方法能准确区分猪、鸡、鸭源性成分,对测试的11 种非目标动物(包括牛、羊、鹅、狐狸、犬、猫、马、鼠等常见物种及易混淆物种)均无非特异性扩增(图2),显示出优异的种间鉴别能力,满足复杂食品基质对检测特异性的严格要求。在特异性方面,本方法显著优于Liu Wanwan等[32]报道的通用引物介导多重PCR(后者在检测8 种肉类混合模板时观察到猪和鸡引物产生<100 bp的杂带),也优于Köppel等[33]开发的需7 对独立引物与探针的七重检测体系(后者引物间交叉反应风险显著增加)。
本实验数据充分证明了该方法的高灵敏度与可靠性,该方法对猪、鸡、鸭DNA的检测限分别为0.04、0.04、0.06 ng/μL,生肉与血制品的灵敏度分别为0.01%和0.10%(95%置信水平),其扩增效率达95.0%(R2>0.980),显著优于GB/T 38164—2019方法(Ct值降低2.3±0.7),优于Dolch等[34]报道的针对禽肉检测的TaqMan多重real-time PCR检测法(其灵敏度为0.5%)。在检测限方面,本研究方法0.04 ng/μL仍可稳定检出(Ct值≤33.50),显著优于于文莹等[5]建立的多重real-time PCR检测鸭血制品时的1 ng/μL检测限。同时,在复杂鸭血制品基质中达到的0.10%灵敏度也优于近期报道的同类多重real-time PCR检测方法[20,30]。
市售鸭血样品检测结果显示,19 份鸭血中猪、鸡、鸭源性成分检出率分别为5.26%(1/19)、57.89%(11/19)及63.16%(12/19),其中26.32%(5/19)的样品存在鸡/鸭源性成分共检出现象。与GB/T 38164—2019方法的对比实验证实,2 种方法在定性检出猪、鸡、鸭源性成分的总体结果上完全一致。然而,基于本方法更低的Ct值和更高的检测灵敏度,其在识别低含量目标源性成分(尤其是潜在的低水平掺假)方面具有潜在优势,能够更精准地反映样品中不同源性成分的含量差异。
尽管本研究建立的方法在特异性、灵敏度、多重检测能力和实际应用表现上展现出诸多优势,但仍存在一定的局限性。首先,本方法对鸭血制品的检测灵敏度(0.10%)显著低于生肉基质(0.01%),提示复杂加工基质(尤其是凝固的血制品)仍然是影响检测性能的关键因素,未来可探索更高效的血制品DNA提取方法,以克服不同基质之间检测限差异[30]。其次,当前方法仅针对猪、鸡、鸭3 种最常涉及的掺假物种进行检测,对于其他潜在掺假源(如牛血或其他禽类)需进一步拓展检测靶标。最后,本研究样本量(n=19)相对有限,更大规模的样本验证将有助于更全面地评估方法的稳定性和广泛适用性。未来研究可考虑将该通用引物/多重探针策略应用于其他动物源性食品的多物种同步鉴别,并探索其在高通量预筛查动物源性掺假方面的应用潜力。
4 结 论
本研究成功建立了一种基于通用引物结合多重TaqMan探针的多重real-time PCR方法,用于鸭血制品中猪、鸡、鸭源性成分的同步、快速、高灵敏度检测。该方法特异性强、灵敏度高,多重检测效率显著优于需多次独立反应的现有标准方法,其在鸭血制品中灵敏度达0.06 ng/μL,检出限为0.10%。在市售鸭血样品检测中,该方法能够高效、快速筛查鸭血制品中的猪血与鸡血掺杂问题,为打击食品掺假行为提供了可靠的技术支持,同时为肉类源性成分鉴别领域的方法创新提供了重要实践参考。
[1] FANG J, XING J L, XU X R, et al.Research progress on the authenticity of duck blood[J].Microchemical Journal, 2024, 206:111609.DOI:10.1016/j.microc.2024.111609.
[2] GAO L J, DU B Y, MA Q H, et al.Multiplex-PCR method application to identify duck blood and its adulterated varieties[J].Food Chemistry,2024, 444: 138673.DOI:10.1016/j.foodchem.2024.138673.
[3] 李美桃, 张春鹏, 王波.实时荧光PCR检测鸭血制品中掺假成分[J].食品工业, 2022, 43(1): 293-295.
[4] 李杰, 钱云开, 王伟, 等.临沂市鸭血制品动物源性成分检测及掺假分析[J].肉类工业, 2022, 3(5): 27-32.DOI:10.3969/j.issn.1008-5467.2022.03.005.
[5] 于文莹, 迟凯月, 徐宁, 等.鉴定鸭血及掺假品种的多重方法的建立及应用[J].食品科技, 2022, 47(12): 307-312.DOI:10.13684/j.cnki.spkj.2022.12.018.
[6] ZHOU C, WANG J F, XIANG J L, et al.Rapid detection of duck ingredient in adulterated foods by isothermal recombinase polymerase amplification assays[J].Food Chemistry: Molecular Sciences, 2023, 6:100162.DOI:10.1016/j.fochms.2023.100162.
[7] 范美霞, 黄立强, 徐传霞, 等.普通PCR与实时荧光PCR两种方法研究鸭血中的鸭源性成分[J].食品安全导刊, 2021(7): 58-59.DOI:10.16043/j.cnki.cfs.2021.07.024.
[8] 陈果.实时荧光检测鸭血中的动物源性成分[J].食品安全质量检测学报, 2019, 10(11): 3339-3342.DOI:10.3969/j.issn.2095-0381.2019.11.019.
[9] 马慧娟, 徐慧, 张维祥, 等.食品中动物源性成分PCR检测法探究[J].中国食品工业, 2021(19): 98-102.
[10] 张媛媛, 孟镇, 仇凯, 等.种属特异性法鉴别罐头食品中猪、牛、羊、鸡、鸭源性成分[J].食品与发酵工业, 2021, 47(3): 164-169.DOI:10.13995/j.cnki.11-1802/ts.024477.
[11] 商务部流通产业促进中心.肉及肉制品中动物源性成分的测定 实时荧光PCR法: SB/T 10923—2012[J].北京: 中国标准出版社, 2013.
[12] 国家质量监督检验检疫总局.饲料中禽源性成分检测方法 实时荧光PCR方法: SN/T 2727—2010[J].北京: 中国标准出版社, 2010.
[13] 国家市场监督管理总局.鸭血中鸭鸡鹅源性成分的测定: BJS 202309[S].北京: 中国标准出版社, 2023.
[14] 中国检验检疫科学研究院, 大连海关, 青岛海关, 等.常见畜禽动物源性成分检测方法 实时荧光PCR法: GB/T 38164—2019[J].北京:中国标准出版社, 2019.
[15] 成都市食品药品检验研究院, 中国科学院成都生物研究所, 北京维德维康生物技术有限公司.食品中多种动物源性成分检测实时荧光PCR法: BJS 201904[J].北京: 中国标准出版社, 2019.
[16] 范维, 高晓月, 李贺楠, 等.4 种动物源性成分多重real-time PCR检测方法的建立及其在驴肉制品检测中的应用[J].食品科学, 2023,44(8): 317-323.DOI:10.7506/spkx1002-6630-20220406-056.
[17] 侯东军, 韩合敬, 郝智慧, 等.三重荧光PCR法鉴定食品中牛、猪、鸭3 种动物源性成分[J].畜牧与兽医, 2016, 48(4): 45-48.
[18] 雷庆, 赵中开.多重荧光定量PCR法同时定量检测4 种混合熟肉种源[J].食品安全导刊, 2021(21): 83-87.DOI:10.16043/j.cnki.cfs.2021.21.047.
[19] 林霖, 陈国培, 何永盛, 等.基于多重荧光PCR检测的肉及其制品中鸭DNA成分的鉴别方法[J].食品与机械, 2017(5): 95-98.DOI:10.13652/j.issn.1003-5788.2017.05.019.
[20] 吕二盼, 周正, 周巍, 等.动物源性食品鸭血、猪血DNA提取及多重PCR鉴别研究[J].食品工业科技, 2012, 33(16): 228-231.DOI:10.13386/j.issn1002-0306.2012.16.082.
[21] 陈珍金, 张璜, 石磊, 等.利用LAMP技术快速检测羊肉制品中的鼠源性成分[J].食品科学, 2021, 42(12): 322-327.DOI:10.7506/spkx1002-6630-20201016-146.
[22] CHEN X Y, LU L X, XIONG X H, et al.Development of a real-time PCR assay for the identification and quantification of bovine ingredient in processed meat products[J].Scientific Reports, 2020, 10(1): 2052.DOI:10.1038/s41598-020-59010-6.
[23] 耿永然.鸭血豆腐常见血源掺假判别、甲醛暴露评估及品质分析[D].天津: 天津科技大学, 2016.DOI:10.27359/d.cnki.gtqgu.2016.000094.
[24] 张卫.真假鸭血豆腐[J].中国食品, 2012(12): 20-21.
[25] 王金斌, 白蓝, 李文, 等.同步检测动物源性成分的五重PCR的条件优化和检出限分析[J].核农学报, 2018, 32(3): 506-514.
[26] 杨冬燕, 杨小柯, 李浩, 等.用多重荧光PCR技术鉴别牛肉中掺入的猪马鸭成分的研究[J].中国预防医学杂志, 2015, 16(7): 528-533.DOI:10.16506/j.1009-6639.2015.07.006.
[27] 岳苑.实时荧光PCR法检测肉制品中鸡、鸭源性成分[J].生物加工过程, 2016, 14(6): 41-45.DOI:10.3969/j.issn.1672-3678.2016.06.008.
[28] 程欣.应用实时荧光PCR方法鉴别食品中的鸭源性成分[D].南京:南京农业大学, 2015.
[29] 程欣, 何玮玲, 黄明.实时荧光PCR法检测食品中鸭肉成分[J].食品科学, 2013, 34(24): 92-96.DOI:10.7506/spkx1002-6630-201324019.
[30] 邓迎春, 刘颖, 王一凡, 等.实时荧光法检测鸭血制品中其他动物源性成分[J].食品科技, 2024, 49(8): 342-348.DOI:10.13684/j.cnki.spkj.2024.08.039.
[31] CHEN C, CHEN J, ZHANG Y, et al.Quantitative detection of beef and beef meat products adulteration by the addition of duck meat using micro drop digital polymerase chain reaction[J].Journal of Food Quality, 2020(6): 1-8.DOI:10.1155/2020/2843056.
[32] LIU W W, TAO J, XUE M, et al.A multiplex PCR method mediated by universal primers for the identification of eight meat ingredients in food products[J].European Food Research and Technology, 2019, 245:2385-2392.DOI:10.1007/s00217-019-03350-9.
[33] KÖPPEL R, ZIMMERLI F, BREITENMOSER A.Heptaplex real-time PCR for the identification and quantification of DNA from beef, pork,chicken, turkey, horse meat, sheep (mutton) and goat[J].European Food Research and Technology, 2009, 230: 125-133.DOI:10.1007/s00217-009-1154-5.
[34] DOLCH K, ANDRÉE S, SCHWÄGELE F.Comparison of real-time PCR quantification methods in the identification of poultry species in meat products[J].Foods, 2020, 9(8): 1049.DOI:10.3390/foods9081049.