切片即食发酵香肠因其独特的口感和风味深受消费者青睐。传统即食发酵香肠以猪瘦肉和猪背膘为主要原料,辅以食盐、糖、香辛料混合搅拌后灌入肠衣,在通风良好的环境中自然发酵而成[1]。传统经验式生产方式缺乏标准化和可控性,难以保障不同批次产品质量一致,进而影响高品质产品的稳定输出。优化发酵剂应用策略有望提升风味特征并增强产品质量稳定性[2-3],从而助力即食发酵香肠的标准化生产。
在发酵肉制品生产过程中,凝固酶阴性葡萄球菌(coagulase negative staphylococci,CNS)和乳酸菌(lactic acid bacteria,LAB)通常作为核心发酵剂,发挥降解蛋白质、调控风味前体物质生成及调节酸度等作用[4-6]。然而,发酵过程仅依赖细菌发酵剂会出现产品特征风味不足的问题[7]。研究表明,酵母菌独特的代谢能力能够促进酯类、高级醇类和羰基化合物等关键挥发性风味物质的生成[8-10],从而增强产品中的花果香味[11]、奶香味[12]和甜香味[13]等香气特征。由此可见,采用酵母菌与传统细菌发酵剂联合接种策略有望弥补细菌发酵剂这一缺陷,提升即食发酵香肠的食用品质。
值得注意的是,酵母菌的接种方式可能对即食发酵香肠的食用品质产生显著影响,但目前相关研究结论尚不一致。部分研究指出,表面接种酵母菌有助于抑制有害霉菌的生长,但对产品感官品质的提升效果有限[14];而另一些研究则发现,酵母菌的内部接种可促进挥发性风味物质,特别是酯类的生成,从而增强发酵香肠的风味[15]。造成这些差异的原因可能包括所用酵母菌菌株的生理特性差异,以及接种方式与肉糜基质之间的相互作用机制尚未明确,菌株间潜在的代谢异质性可能是导致发酵香肠感官品质结果差异的关键因素。
为深入揭示不同酵母菌菌株及其接种方式在即食发酵香肠中的具体作用,本研究从传统发酵肉制品中分离获得4 株代表性酵母菌菌株(汉逊德巴利酵母(Debaryomyces hansenii)MF4、D.hansenii MF5、近平滑假丝酵母(Candida parapsilosis)MA3和C.parapsilosis MY6),它们均表现出较强的耐酸、耐盐、耐低温和耐亚硝酸盐能力,并具备较高的蛋白酶与脂肪酶活性(数据未发表)。基于菌株特性及应用潜力,本研究设计了不同的菌株组合及接种方式(表面喷涂与内部接种),分析其对即食发酵香肠感官属性、理化特征及风味的影响,旨在明确酵母菌的有效接种策略,提升产品的风味层次与食用品质,并为功能型发酵剂的开发提供参考依据。
1 材料与方法
1.1 材料与试剂
原料:杜洛克公猪(10 月龄、体质量110~140 kg)后腿瘦肉和背膘,市购。
辅料:葡萄糖、食盐、D-异抗坏血酸钠(食品级)、NaNO2(食品级)、酪蛋白酸钠(食品级),购自河南万邦实业有限公司。
菌株:马胃葡萄球菌(Staphylococcus equorum)E-1、木糖葡萄球菌(Staphylococcus xylosus)NY-2、副干酪乳酪杆菌(Lacticaseibacillus paracasei)YL-1、D.hansenii MF4、D.hansenii MF5、C.parapsilosis MA3和C.parapsilosis MY6均分离自传统发酵肉制品,于本实验室保藏。
培养基及试剂:MRS培养基、脑心浸液肉汤(brainheart infusion broth,BHI)培养基、麦芽汁(malt extract,ME)培养基、甘露醇高盐琼脂(mannitol salt agar,MSA)培养基、麦芽汁琼脂(malt extract agar,MEA)培养基、平板计数琼脂(plate count agar,PCA)培养基 青岛海博生物技术有限公司;2-甲基-3-庚酮上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
pH 200便携式pH测试仪 上海振迈仪器设备有限公司;CR-400色彩色差计 柯尼卡美能达光学仪器有限公司;HD-6水分活度(water activity,aw)测量仪无锡华科仪器仪表有限公司;TA.XT Plus质构仪 英国Stable Micro Systems公司;PEN3电子鼻 德国Airsense Analytics公司;TS-5000Z电子舌 日本Insent公司;7890A-5975C气相色谱-质谱联用(gas chromatographymass spectrometry,GC-MS)仪 美国Agilent公司;KBF-240恒温恒湿培养箱 德国宾得公司。
1.3 方法
1.3.1 菌株的活化与发酵剂的制备
菌株均分离自传统发酵肉制品,并于-80 ℃下保存。L.paracasei YL-1接种于MRS液体培养基,37 ℃培养24 h;S.equorum E-1和S.xylosus NY-2接种于BHI培养基,37 ℃培养24 h;D.hansenii MF4、D.hansenii MF5、C.parapsilosis MY6和C.parapsilosis MA3接种于ME培养基,28 ℃培养24 h,以完成活化。活化后的菌悬液以1%的接种量接入对应培养基中继续培养至对数生长期。随后取菌悬液于4 ℃、5 000×g条件下离心15 min,弃上清液,使用无菌水按比例重悬并进行梯度稀释,测定其OD600 nm,将OD600 nm代入菌密度标准曲线中计算对应的活菌数,将菌悬液作为发酵剂备用。
菌密度标准曲线绘制:将离心后的菌悬液梯度稀释至不同浓度,测定其OD600 nm并进行平板计数,根据OD600 nm与对应菌落数建立菌密度标准曲线。
1.3.2 发酵香肠的制作
将猪后腿瘦肉和猪背膘按质量比7∶3混合,以肉馅质量为基准分别加入食盐(2.5%,m/m,下同)、食用葡萄糖(0.3%)、NaNO2(0.015%)、D-异抗坏血酸钠(0.1%)、酪蛋白酸钠(0.1%)和发酵剂,搅拌均匀后分成10 组,其中S.equorum E-1和S.xylosus NY-2的接种量均为1×107 CFU/g,L.paracasei YL-1的接种量为1×106 CFU/g,D.hansenii MF4、D.hansenii MF5、C.parapsilosis MA3和C.parapsilosis MY6的接种量均为1×104 CFU/g,具体分组见表1。内部接种时将发酵剂与肉馅混匀后灌入天然猪肠衣,每隔10 cm左右打结。灌肠4 h后,在香肠表面均匀喷洒酵母菌液,每根香肠喷洒2 mL。接种完成的香肠在25 ℃、相对湿度85%~95%条件下发酵1 d,随后转入10~15 ℃、相对湿度70%~85%条件下成熟45 d。整个过程中所有原辅料及菌液均需在灌肠前充分混匀,喷涂时确保菌液均匀覆盖肠体表面。
表1 实验分组
Table 1 Experimental grouping
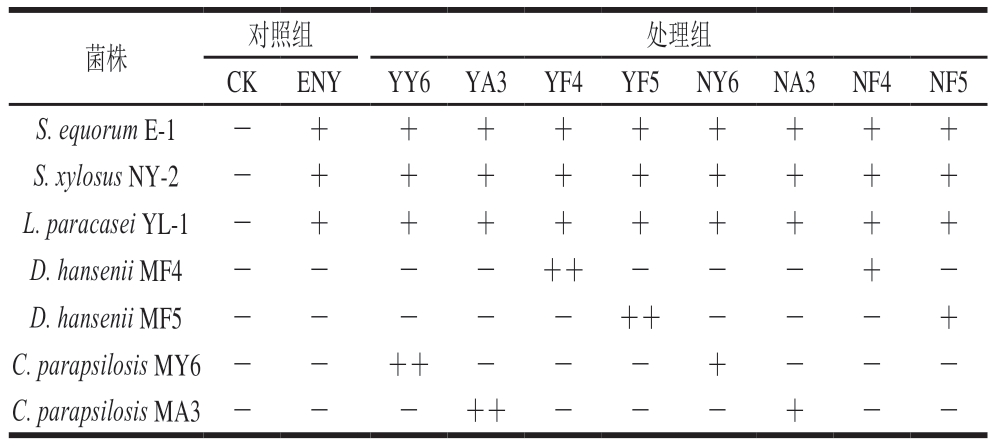
注:-.未接种;+.内部接种;++.表面喷涂。
菌株对照组处理组CKENYYY6 YA3 YF4 YF5 NY6 NA3 NF4 NF5 S.equorum E-1-+++++++++S.xylosus NY-2-+++++++++L.paracasei YL-1-+++++++++D.hansenii MF4----++---+-D.hansenii MF5-----++---+C.parapsilosis MY6 --++---+---C.parapsilosis MA3 ---++---+--
香肠发酵时间共46 d,于发酵第0、3、7、14、21、31天测定pH值、水分含量、aw、色泽,发酵结束时(第46天)进行感官评价及质构、电子鼻、电子舌、微生物数量和风味测定。
1.3.3 感官评价
招募感官评价人员,首先通过调查问卷筛选符合条件的人员,并采用三角试验法进一步测试其感官敏锐度,最终筛选出11 名人员(7 名女性、4 名男性)作为评价小组成员。成员需接受为期1 个月的基础感官培训,以熟悉发酵香肠的感官特征。正式评价时,每位成员坐在感官评价室的独立隔间内对20 g随机编码的发酵香肠样品进行9 分制评分,范围从1 分(低)到9 分(高),每项评分取平均值,感官评分标准见表2。
表2 发酵香肠感官评分标准
Table 2 Sensory evaluation criteria for fermented sausages

评价指标评分标准评分色泽瘦肉呈宝石红色、脂肪呈白色或乳白色,色泽明亮9~7瘦肉呈深红色或粉红色、脂肪呈杏黄色或浅黄色,亮度适中6~4瘦肉呈灰红色或黑红色、脂肪呈灰黄色,亮度暗沉3~1大理石纹理脂肪与瘦肉分布均匀,大理石纹理清晰自然,切面整体观感佳9~7脂肪与瘦肉分布较均匀,纹理不够清晰,切面观感一般6~4脂肪分布不均匀,团状聚集,纹理不明显,切面观感差3~1质构香肠组织紧致、富有弹性,切面完整不松散,咀嚼时不硬不韧9~7香肠组织较为紧致,弹性一般,切面轻微松散,咀嚼感适中6~4香肠组织松散或过硬,切面易碎,咀嚼时口感差,缺乏弹性或韧性3~1切面平整度切面平整光滑,整齐完整,无明显凹凸或碎裂现象9~7切面较为平整,存在轻微不平或少量碎裂,整体观感一般6~4切面凹凸明显或碎裂严重,切割不整齐,观感差3~1口感咀嚼时富有弹性,硬度适中9~7弹性适中,较硬或较软6~4弹性较差,坚硬或松软3~1咸味、肉香味、脂香味、奶香味、花果香味、甜味、酸味、香料味、清新味、哈喇味和腐臭味较强9~7气味咸味、肉香味、脂香味、奶香味、花果香味、甜味、酸味、香料味、清新味、哈喇味和腐臭味适中6~4咸味、肉香味、脂香味、奶香味、花果香味、甜味、酸味、香料味、清新味、哈喇味和腐臭味较弱3~1滋味酸、甜、苦、咸、鲜味较强9~7酸、甜、苦、咸、鲜味适中6~4酸、甜、苦、咸、鲜味较弱3~1风味层次感风味丰富,肉香、发酵香协调,口感层次分明且平衡9~7风味较为明显,层次感不够突出或协调性一般,整体口感尚可6~4风味单一或不协调,层次感差,口感平淡或出现不良异味3~1持久度、鲜味、咸味、肉香味、脂香味、甜香味、奶香味、苦味、乳酸味、花果香味和香料味较强9~7后味持久度、鲜味、咸味、肉香味、脂香味、甜香味、奶香味、苦味、乳酸味、花果香味和香料味适中6~4持久度、鲜味、咸味、肉香味、脂香味、甜香味、奶香味、苦味、乳酸味、花果香味和香料味较弱3~1总体可接受度较喜欢9~7适中6~4不喜欢3~1
1.3.4 pH值、水分含量、aw、色泽和质构测定
将p H 计插入发酵香肠样品中测定p H 值。参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》中的直接干燥法测定样品水分含量。参照GB 5009.238—2016《食品安全国家标准 食品水分活度的测定》中的水分活度仪扩散法测定样品aw。参考肖亚庆等[16]的方法测定样品亮度值(lightness value,L*)、红度值(redness value,a*)和黄度值(yellowness value,b*)。参考Škrlep等[17]的方法测定样品质构特征。
1.3.5 电子鼻测定
发酵香肠的气味特征使用电子鼻进行分析,参考Wen Rongxin等[18]的方法并稍作修改。电子鼻配备10 个传感器,即W1C、W5S、W3C、W6S、W5C、W1S、W1W、W2S、W2W和W3S,可根据挥发性化合物的不同化学性质区分气味,传感器相关信息见表3。将香肠肠衣除去,绞碎后均匀混合,称取10 g置于50 mL离心管中,使用3 层保鲜膜密封,将离心管置于40 ℃恒温水浴锅内加热5 min。测定参数设置如下:吹洗时间60 s,准备时间5 s,数据采集时间120 s,结束时间5 s。每个样品平行测定3 次。
表3 电子鼻传感器性能描述
Table 3 Performance description of electronic nose sensors

传感器名称传感器相应特性W1C对芳香族化合物敏感W5S对氮氧化合物敏感W3C对氨水、苯等芳香化合物敏感W6S对烃类敏感W5C对短链烷烃、芳香成分敏感W1S对甲基类敏感W1W对含硫化合物敏感W2S对醇类、醛酮类敏感W2W对芳香成分、有机硫化物敏感W3S对长链烷烃敏感
1.3.6 电子舌测定
发酵香肠的滋味特征通过电子舌进行分析,参考Li Xiang’ao等[19]的方法并稍作修改。称取10 g切碎的香肠于100 mL蒸馏水中,8 000~8 500 r/min均质2 min,均质后的混合物在3 000×g、4 ℃条件下离心10 min,收集上清液,分别用0.45、0.22 μm水相滤膜过滤,取上清液35 mL置于50 mL烧杯中,在室温下使用电子舌检测其咸味、苦味、收敛性、后味-A、后味-B、鲜味和丰富度,每个样品循环4 次。以基准液为空白对照,每个样品平行测定6 次。
1.3.7 微生物计数
无菌条件下将10 g香肠样品置于90 mL无菌生理盐水,采用均质机均质2 min(6 000 r/min)。将均质液用无菌生理盐水进行10 倍梯度稀释后,取104~105梯度稀释液0.2 mL倾注于培养基培养。具体而言:在MRS和MSA培养基上分别进行LAB和CNS计数,温度为35 ℃,培养48 h;在PCA培养基上进行菌落总数测定,温度为30 ℃,培养48 h;在MEA培养基上进行酵母菌计数,温度为28 ℃,培养72 h。每个样品平行测定3 次。
1.3.8 挥发性风味物质测定
参考Yang Peng等[20]的方法并稍作修改。取3 g切碎的香肠样品加入10 μL 0.01 mg/mL 2-甲基-3-庚酮溶液,置于20 mL顶空瓶中封盖,在60 ℃水浴锅中平衡15 min。使用50/30 μm CAR/DVB/PDMS固相微萃取头,55 ℃下萃取45 min后置于GC-MS仪进样口,250 ℃热解吸5 min。GC条件:使用DB-WAX毛细管柱(30 m×250 μm,0.25 μm),载气为He,流速1.0 mL/min,不分流方式进样,进样口温度250 ℃;升温程序:初始温度40 ℃,保持4 min;随后5 ℃/min升至245 ℃,保持5 min。MS条件:离子源温度230 ℃,电离方式为电子电离,电子能量70 eV,传输线温度250 ℃;扫描范围20~500 m/z。通过与NIST质谱库比对鉴定挥发性成分,各挥发性风味物质含量按下式计算:
1.4 数据处理
原始数据使用Microsoft Excel 2019软件整理成数据集,结果以平均值±标准差表示。使用SPSS 21软件对数据进行单因素方差分析,采用Duncan多重比较法进行组间差异显著性分析,P<0.05表示差异显著。使用Origin 2024软件绘图。
2 结果与分析
2.1 不同酵母菌菌株及其接种方式对即食发酵香肠感官品质的影响
如图1a所示,各组发酵香肠总体可接受度评分排名为YF4>YF5>ENY>NF4>NF5>NY6>NA3>YY6>CK>YA3,说明D.hansenii在改善发酵香肠感官品质方面优于C.parapsilosis,且D.hansenii采用表面喷涂法优于内部接种法。表面喷涂D.hansenii提高了发酵香肠的总体可接受度,具体而言,在气味方面,YF4和YF5组发酵香肠的奶香味和花果香味较浓郁(图1b)。在色泽和质构方面,YF4组香肠切面颜色呈宝石红色,大理石纹理清晰,切片紧实,且具有较好的弹性(图2)。此外,接种酵母菌的发酵香肠鲜味得分高于CK和ENY对照组(图1c)。综上所述,YF4组发酵香肠在外观、色泽、质构、气味和滋味方面表现优异,表明表面喷涂D.hansenii MF4对提升即食发酵香肠感官品质具有重要作用。
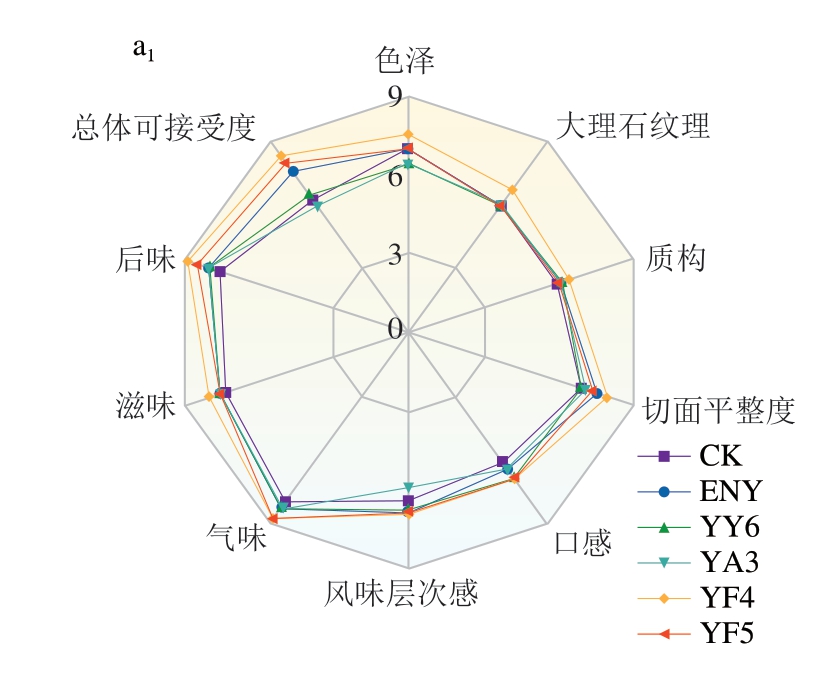
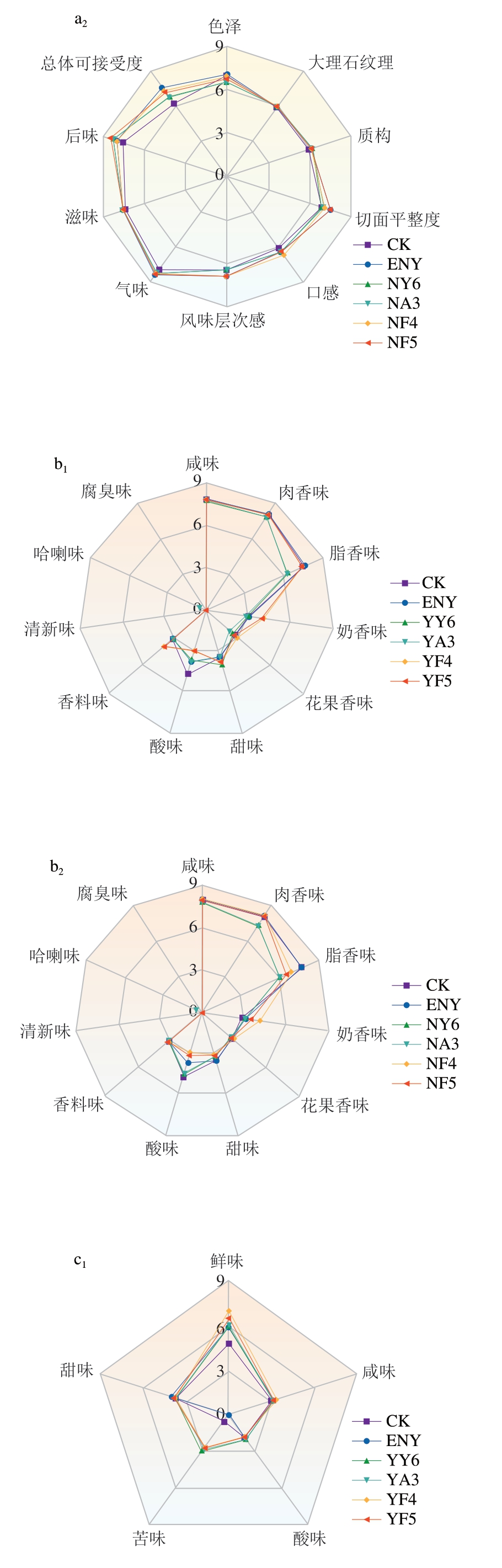
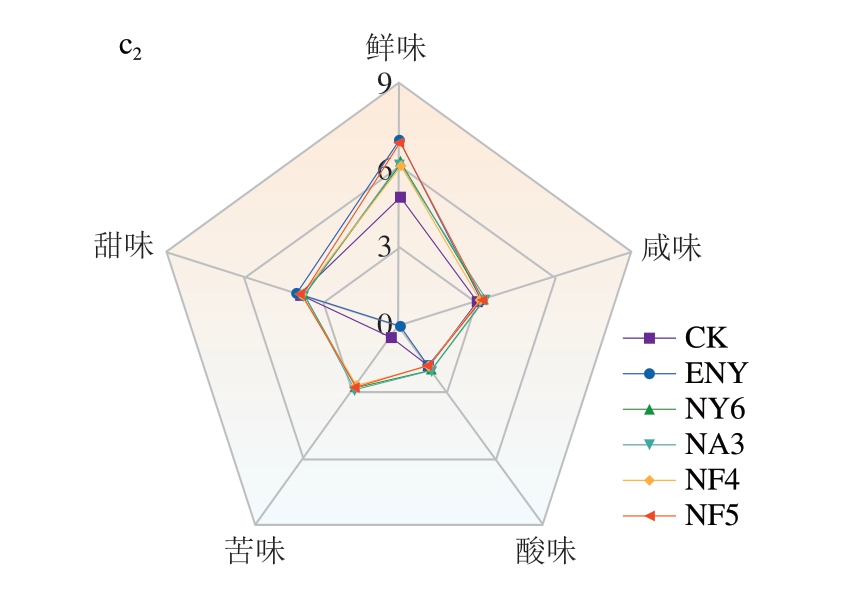
图1 不同处理组发酵香肠感官(a)、气味(b)和滋味(c)评分
Fig.1 Sensory scores (a), odor scores (b), and taste scores (c) of fermented sausages from different treatment groups
下标1.表面喷涂;下标2.内部接种。图3~5同。
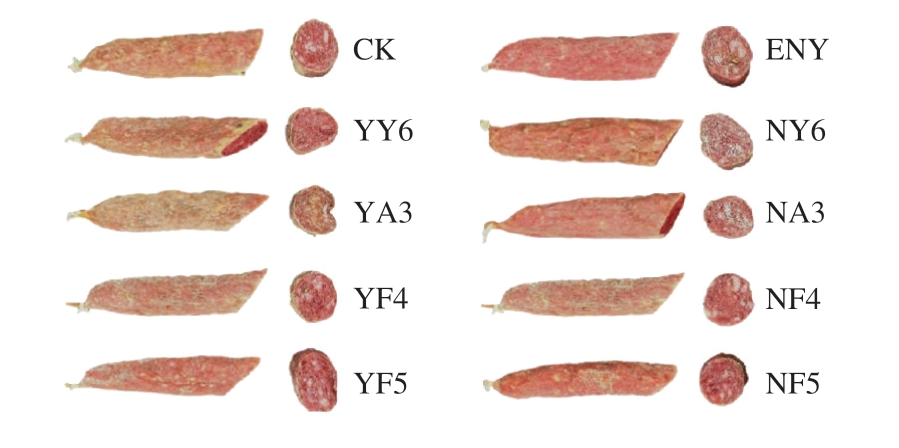
图2 不同处理组发酵香肠的外观及横切面特征
Fig.2 Appearance and cross-sectional characteristics of fermented sausages from different treatment groups
2.2 不同酵母菌菌株及其接种方式对即食发酵香肠pH值、水分含量、aw和质构的影响
如图3a所示,所有组发酵香肠的pH值在发酵初期(第0~3天)均呈下降趋势,中后期(第3~31天)逐渐回升并趋于稳定。发酵后期pH值的升高可能与蛋白水解作用以及接种或自然存在的酵母菌对乳酸的消耗有关[21]。然而,酵母菌的不同接种方式影响了pH值水平,其中,表面喷涂组香肠的pH值略高于内部接种组,这可能是因为表面生长的酵母菌获得了充足的氧气供应,能够有效消耗乳酸,减少酸性物质的积累,从而提高pH值。
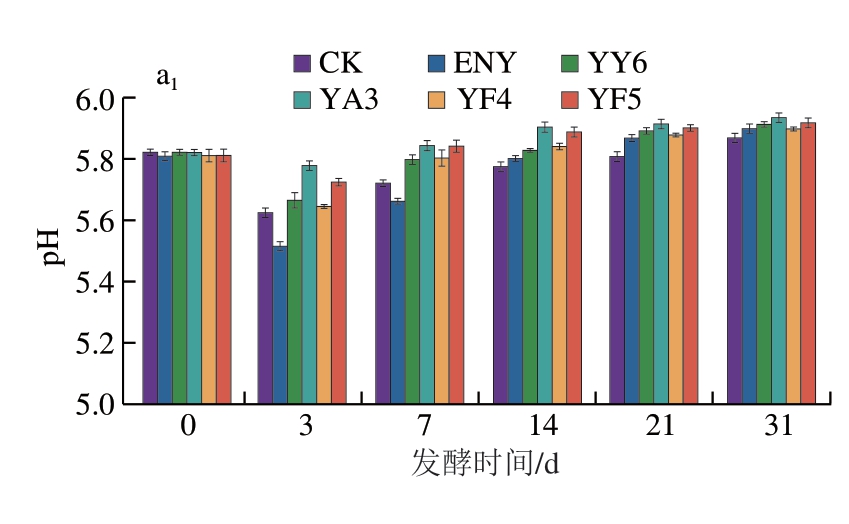
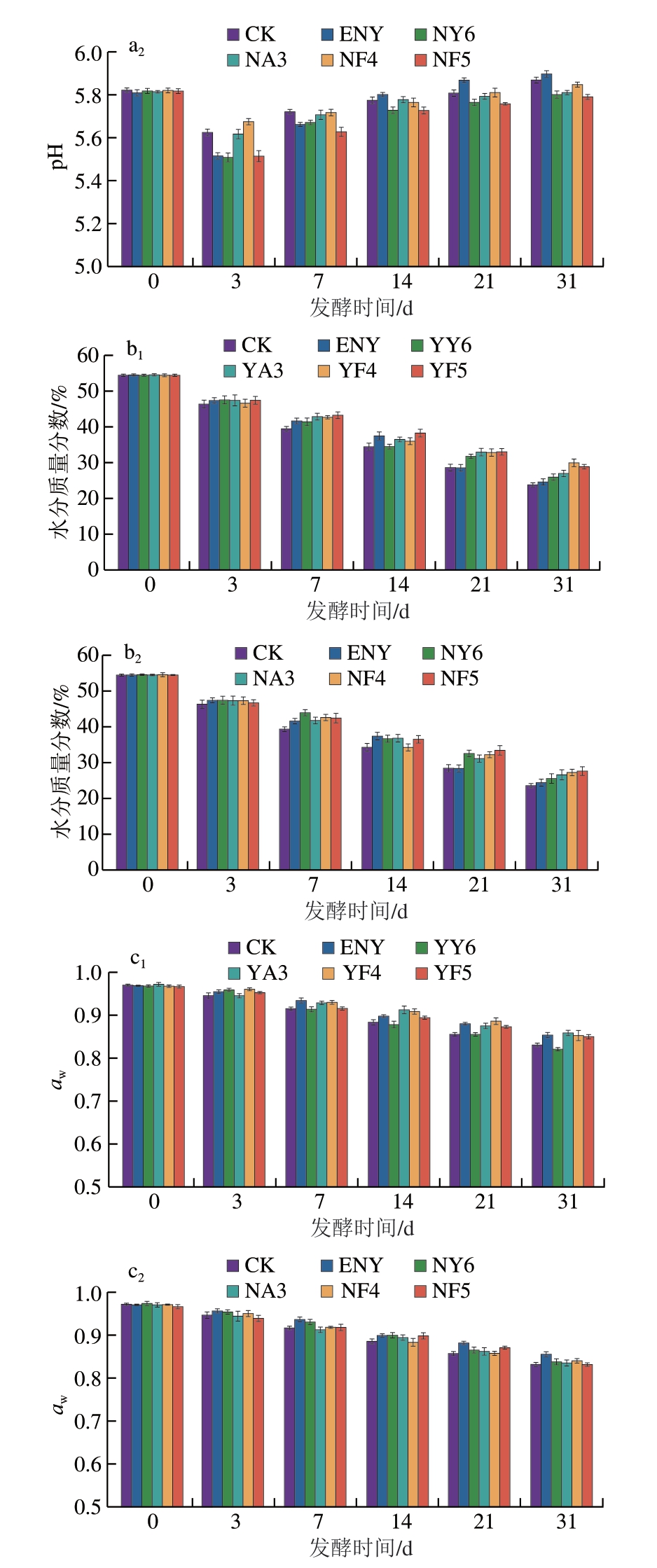
图3 不同处理组发酵香肠的pH值(a)、水分含量(b)和aw(c)
Fig.3 pH (a), moisture content (b) and water activity (c) of fermented sausages from different treatment groups
如图3b、c所示,在发酵的31 d内,各个处理组发酵香肠的水分含量和aw均呈下降趋势,但不同处理组间仍存在一定差异。表面喷涂酵母组香肠发酵结束时的水分含量略高于内部接种酵母组,这可能是由于酵母菌在香肠表面的生长影响了水分迁移,减缓水分损失[22]。尤其是YF4组和YF5组表现出较高的水分含量,这说明表面喷涂D.hansenii可提高发酵结束时产品中的水分含量。
由表4可知,与CK和ENY组相比,YF4组香肠的硬度、弹性、黏聚性和胶着度均有所提高,而咀嚼性有所降低,这可能与D.hansenii的接种有关,其参与肉蛋白的变性和凝胶形成,促进香肠内部构建更加致密的凝胶网络结构,从而增强黏聚性和胶着度[23]。此外,接种C.parapsilosis MY6的NY6和YY6组香肠表现出较高的硬度,这与感官评价结果相符(数据未列出)。
表4 不同处理组发酵香肠的质构参数
Table 4 Texture parameters of fermented sausages from different treatment groups
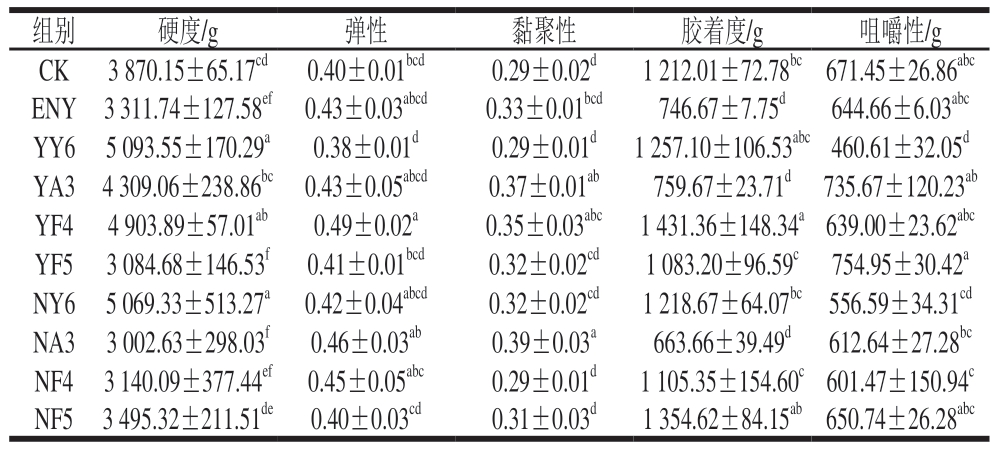
注:同列小写字母不同表示差异显著(P<0.05)。表5同。
组别硬度/g弹性黏聚性胶着度/g咀嚼性/g CK 3 870.15±65.17cd0.40±0.01bcd0.29±0.02d1 212.01±72.78bc 671.45±26.86abc ENY 3 311.74±127.58ef 0.43±0.03abcd0.33±0.01bcd746.67±7.75d644.66±6.03abc YY6 5 093.55±170.29a0.38±0.01d0.29±0.01d 1 257.10±106.53abc 460.61±32.05d YA3 4 309.06±238.86bc 0.43±0.05abcd0.37±0.01ab759.67±23.71d 735.67±120.23ab YF4 4 903.89±57.01ab0.49±0.02a0.35±0.03abc 1 431.36±148.34a 639.00±23.62abc YF5 3 084.68±146.53f 0.41±0.01bcd0.32±0.02cd1 083.20±96.59c 754.95±30.42a NY6 5 069.33±513.27a 0.42±0.04abcd0.32±0.02cd1 218.67±64.07bc 556.59±34.31cd NA3 3 002.63±298.03f0.46±0.03ab0.39±0.03a663.66±39.49d 612.64±27.28bc NF4 3 140.09±377.44ef 0.45±0.05abc0.29±0.01d1 105.35±154.60c 601.47±150.94c NF5 3 495.32±211.51de 0.40±0.03cd0.31±0.03d1 354.62±84.15ab 650.74±26.28abc
2.3 不同酵母菌菌株及其接种方式对即食发酵香肠色泽的影响
如图4a、b所示,各组香肠的L*和a*均呈先上升后下降的趋势。发酵初期(第0~3天),L*的增加与pH值的快速下降相吻合。随着发酵过程中的水分流失,发酵香肠蛋白网络结构收缩,导致表面粗糙度增加、光泽度下降,从而使L*降低。发酵初期a*的升高主要与亚硝基肌红蛋白的形成有关。此后,随着肌红蛋白的氧化降解,a*逐渐下降。在发酵结束时,YF4组香肠a*仍维持在较高水平,这可能与D.hansenii MF4代谢释放的抗氧化物质有关[24]。在整个发酵过程中,各组香肠的b*均呈不同程度的下降(图4c)。发酵结束时,D.hansenii组的b*略高于其他组。
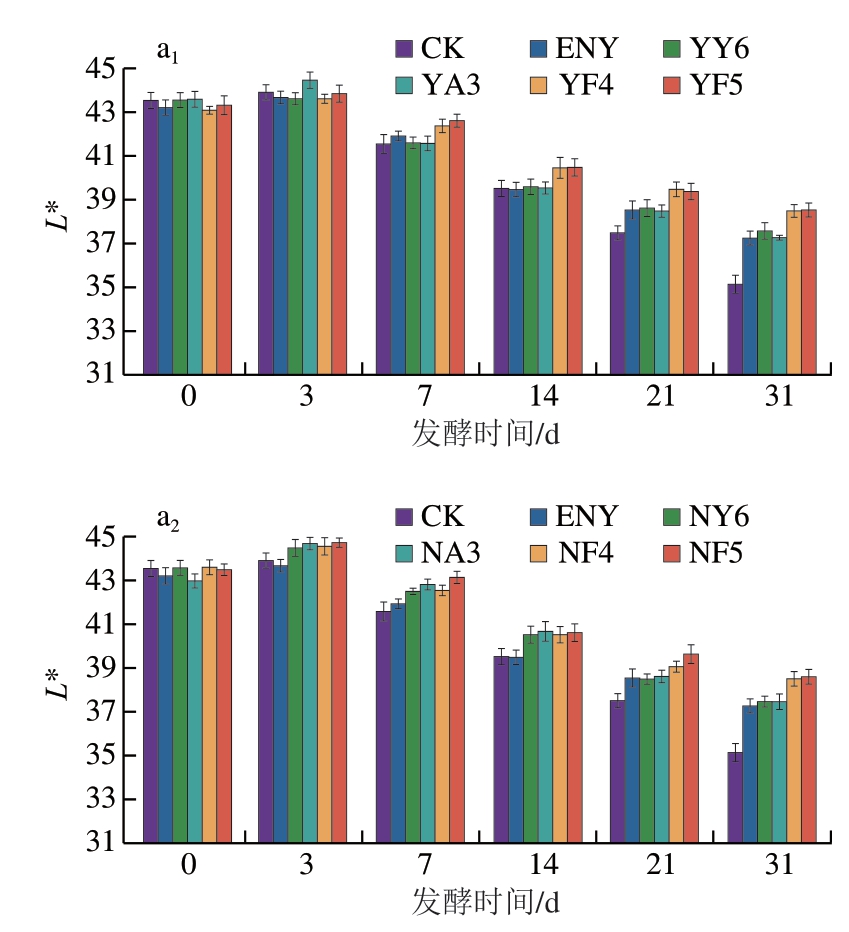
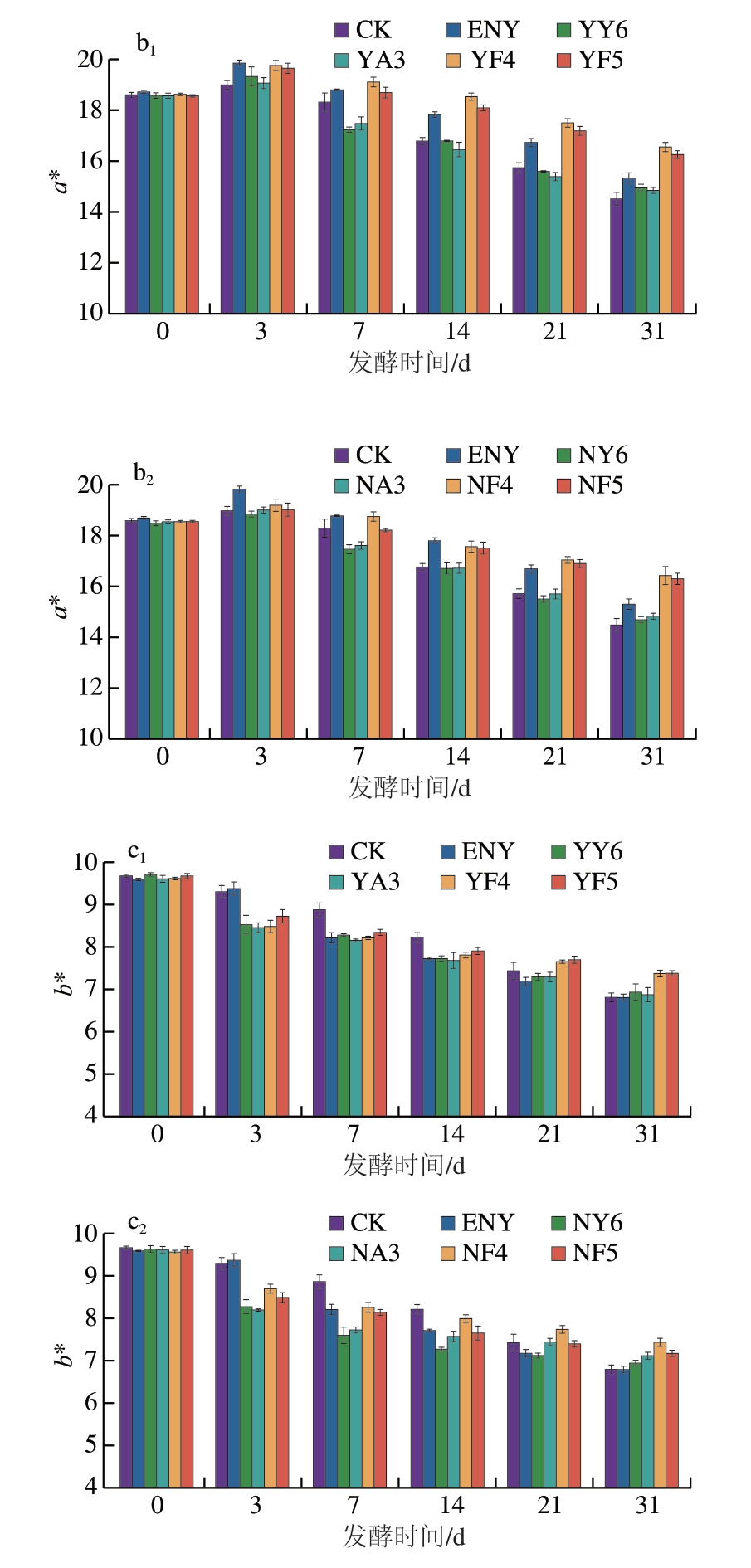
图4 不同处理组发酵香肠的L*(a)、a*(b)和b*(c)
Fig.4 Lightness (a), redness (b) and yellowness values (c) of fermented sausages from different treatment groups
2.4 不同酵母菌菌株及其接种方式对即食发酵香肠香气和滋味的影响
如图5a所示,所有处理组香肠均可被电子鼻传感器有效识别,说明传感器对香肠风味具有较高的灵敏度,其中,YF4组香肠在W5S和W2S传感器上的响应值高于其他组,表明表面喷涂D.hansenii MF4可能产生了更多的氮氧化合物、醇类和醛酮类物质。而ENY组香肠在W1C和W1W传感器上的响应较强,表明其可能含有较高含量的芳香族和含硫化合物。其他传感器(W3C、W6S、W5C、W2S、W2W和W3S)在各组间的响应值基本相同,说明这些传感器所对应的挥发性化合物在不同处理组中含量相近。
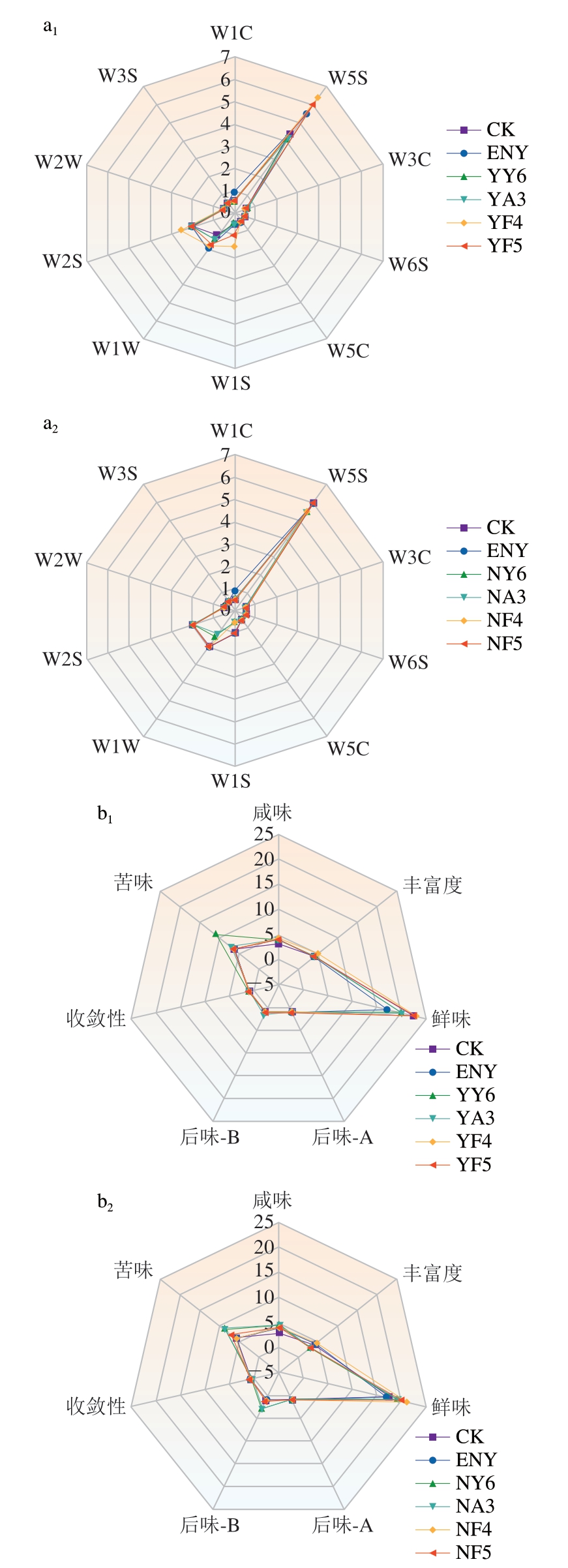
图5 不同处理组发酵香肠的电子鼻(a)和电子舌(b)传感器响应值雷达图
Fig.5 Radar charts of electronic nose (a) and electronic tongue (b)sensor responses for fermented sausages from different treatment groups
为进一步了解不同处理组发酵香肠在滋味上的差异,使用电子舌获得7 种有效的味觉响应值。如图5b所示,与CK和ENY组相比,接种酵母菌组香肠的味觉特性发生了变化,主要表现为鲜味、咸味和苦味的增强。相比之下,收敛性和后味-A(涩味回味)几乎没有变化。其中,YF4、YF5和NF4组香肠呈现出较高的鲜味响应值,这可能与D.hansenii在发酵过程中产生的鲜味氨基酸和风味活性肽有关[25],并且结合感官评价结果发现,鲜味较高的香肠可能更受感官评价人员青睐。此外,YY6组香肠的苦味和NA3组香肠的后味-B(苦味回味)高于其他组,这与感官评价结果中的高苦味评分相符。综合而言,电子鼻和电子舌均可快速、有效地区分不同处理组香肠在气味和滋味上的差异,而这些差异可能源于酵母菌在风味物质生成方面的菌株异质性[26]。
2.5 不同酵母菌菌株及其接种方式对即食发酵香肠微生物数量的影响
由表5可知,与CK和ENY组相比,接种酵母菌的香肠中含有显著较高的菌落总数和酵母菌数(P<0.05)。其中,表面喷涂D.hansenii组香肠的酵母菌数显著高于内部接种D.hansenii组(P<0.05)。在所有接种酵母菌的香肠中,无论是表面喷涂组还是内部接种组,均为D.hansenii MF4组酵母菌数最高,其次是C.parapsilosis MY6、D.hansenii MF5和C.parapsilosis MA3组,这一差异可能与不同酵母菌菌株在发酵香肠中的环境适应性及生长能力有关。YA3组和NA3组香肠的LAB数显著高于其他组(P<0.05),这与感官评价结果中的高酸味评分相吻合(图1c)。相较于ENY组,接种酵母菌组香肠的CNS数均有所降低,这可能归因于酵母菌与CNS在生长过程中对底物的竞争。
表5 不同处理组发酵香肠的微生物数量
Table 5 Microbial counts of fermented sausages from different treatment groupslg(CFU/g)
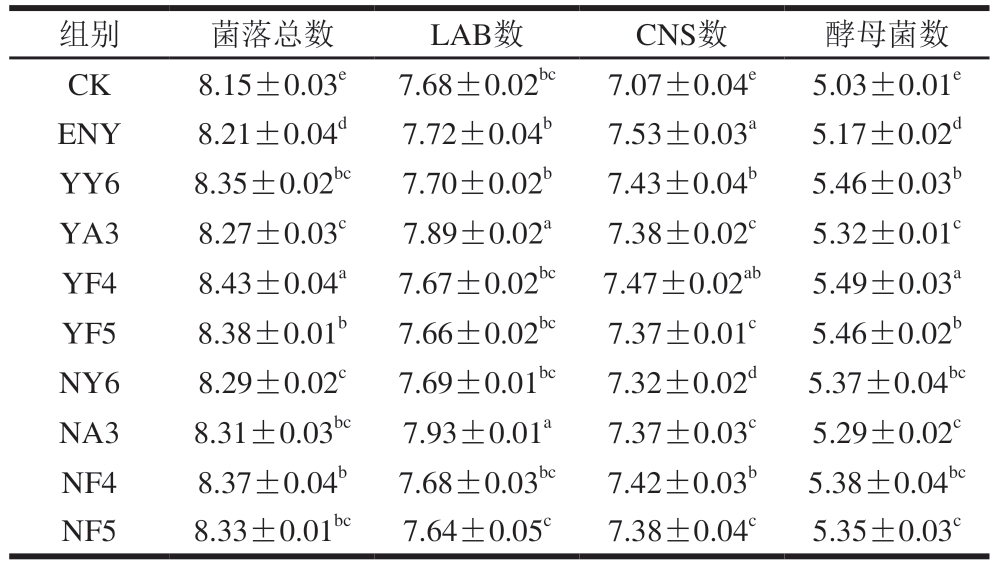
组别菌落总数LAB数CNS数酵母菌数CK8.15±0.03e7.68±0.02bc7.07±0.04e5.03±0.01e ENY8.21±0.04d7.72±0.04b7.53±0.03a5.17±0.02d YY68.35±0.02bc7.70±0.02b7.43±0.04b5.46±0.03b YA38.27±0.03c7.89±0.02a7.38±0.02c5.32±0.01c YF48.43±0.04a7.67±0.02bc7.47±0.02ab5.49±0.03a YF58.38±0.01b7.66±0.02bc7.37±0.01c5.46±0.02b NY68.29±0.02c7.69±0.01bc7.32±0.02d5.37±0.04bc NA38.31±0.03bc7.93±0.01a7.37±0.03c5.29±0.02c NF48.37±0.04b7.68±0.03bc7.42±0.03b5.38±0.04bc NF58.33±0.01bc7.64±0.05c7.38±0.04c5.35±0.03c
2.6 不同酵母菌菌株及其接种方式对即食发酵香肠挥发性风味物质的影响
如图6所示,不同组香肠中共检出83 种挥发性风味物质,分别属于酯类(20 种)、醛类(12 种)、酮类(7 种)、醇类(10 种)、烯烃类(16 种)、酸类(8 种)、苯类(2 种)、烷烃类(4 种)、酚类(1 种)、吡嗪类(2 种)和含硫化合物(1 种)。其中,10 组香肠中共有的挥发性风味物质有36 种(图6a),且所有接种组香肠的挥发性物质总含量均高于CK对照组(图6b),尤其是D.hansenii的接种使发酵香肠酯类物质含量增加。聚类热图(图6c)中,10 个香肠样本被聚为3 类,其中YF4、NF4和NF5被聚为一类,YF5、NY6和NA3被聚为一类,其余样本则被聚为另一类,表明不同酵母菌种类及其接种方式影响发酵香肠挥发性风味轮廓的形成。
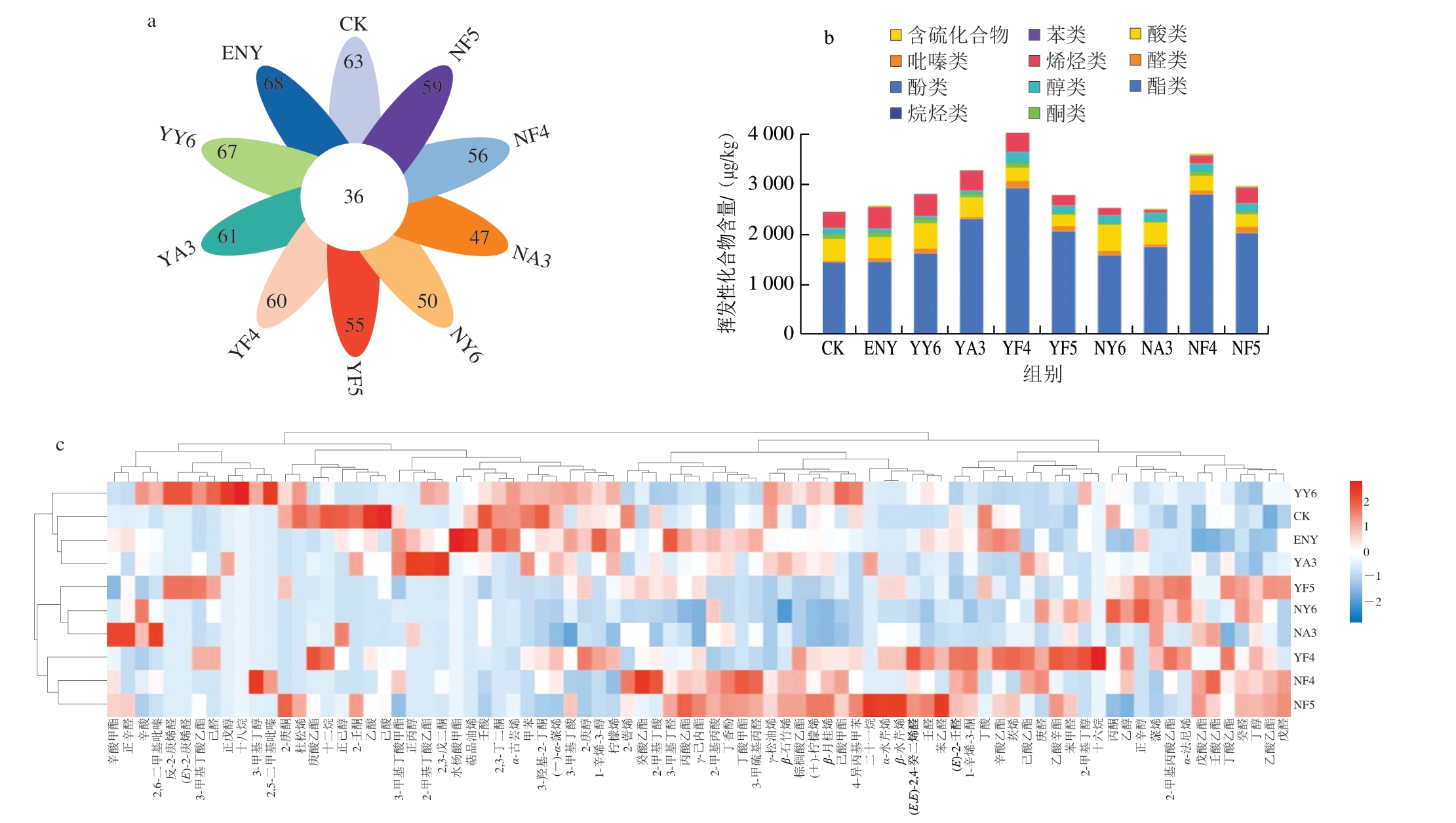
图6 不同处理组发酵香肠的挥发性风味化合物Venn图(a)、总含量(b)及聚类热图(c)
Fig.6 Venn diagram (a), total contents (b) and cluster heatmap (c) of volatile flavor compounds in fermented sausages from different treatment groups
与CK和ENY组相比,接种酵母菌组香肠的酯类物质含量均有所增加,其中,表面喷涂酵母菌(YY6、YA3、YF4、YF5)提高酯类物质含量的能力优于内部接种酵母菌(NY6、NA3、NF4、NF5)。以甜香味和果香味为主的2-甲基丙酸乙酯和3-甲基丁酸乙酯在YF4和YF5组香肠中的含量略高于其他组,使这2 组香肠在感官评价中获得较高的果香味评分。在所有组别中,接种D.hansenii MF4的香肠表现出最高的酯类物质含量,分别达到2 907.07 µg/kg(YF4组)和2 781.47 µg/kg(NF4组),表明D.hansenii MF4的接种能够促进酯类物质的生成,从而对发酵香肠的气味产生积极影响。
YF4组香肠的醛类物质总含量高于其他组。苯甲醛和苯乙醛主要在YF4和NF5组中检出,其源自苯丙氨酸的代谢,赋予香肠花香味和清新味[27]。3-甲基丁醛在YF5和NF5组中检出,其主要由亮氨酸和异亮氨酸代谢产生,具有较低的气味阈值,能够赋予香肠奶酪味和坚果味[28]。总体而言,与其他组别相比,接种D.hansenii的香肠中醛类物质含量较高。
在所有香肠中共检出8 种酸类物质,其中,接种C.parapsilosis的香肠(YY6、YA3、NY6、NA3)酸类物质含量较高,尤其是NY6(516.6 µg/kg)和YY6组(499.38 µg/kg)。相比之下,接种D.hansenii的香肠(YF4、YF5、NF4、NF5组)总酸含量相对较低,这说明D.hansenii的接种可能会降低发酵香肠的总酸含量。
接种酵母菌组香肠中的总酮含量均低于CK和ENY对照组。在检出的7 种酮类物质中,3-羟基-2-丁酮主要来源于碳水化合物的分解,被认为是发酵肉制品特有的风味物质[29],具有黄油味和奶香味,其可进一步被氧化成2,3-丁二酮。1-辛烯-3-醇主要存在于YY6和YF4组香肠中,尤其是YF4组含量较高,由于其较低的阈值被认为是发酵香肠香气的关键贡献者,具有强烈的蘑菇味[30-31]。
综上所述,酵母菌种类和接种方式均可在一定程度上影响切片即食发酵香肠的风味物质组成。其中,D.hansenii的接种可提升酯类和部分醛类物质(苯甲醛、苯乙醛、3-甲基丁醛)含量;而C.parapsilosis的接种则更倾向于促进酸类物质的积累。表面喷涂酵母菌(YY6、YA3、YF4、YF5)在促进酯类物质生成方面的效果优于内部接种酵母菌(NY6、NA3、NF4、NF5)。综合而言,表面喷涂D.hansenii MF4更有利于酯类、醛类和部分醇类物质(1-辛烯-3-醇)的生成,使香肠呈现出更突出的甜香味、花果香味和蘑菇味。
3 结 论
研究表明,不同酵母菌菌株及其接种方式对切片即食发酵香肠的感官属性、理化特征及风味具有不同程度的影响。相较于内部接种,表面喷涂酵母菌的香肠在pH值、水分含量、aw和整体感官评分方面均呈较高水平,尤其是D.hansenii MF4的表面喷涂不仅改善了香肠质构,还赋予其良好的色泽(切面呈宝石红色)和纹理(大理石花纹清晰)。此外,该菌株在风味物质生成方面表现出显著优势,能够提升香肠的甜香味、花果香味和蘑菇味,并有效减少酸类物质含量,使整体风味更加协调。综上所述,S.equorum E-1、S.xylosus NY-2、L.paracasei YL-1与表面喷涂D.hansenii MF4的发酵剂组合可改善传统即食发酵香肠品质缺陷。
[1] 田雅琴, 孙丁, 杨娟春, 等.不同原料肉对发酵香肠食用品质的影响[J].肉类研究, 2022, 36(1): 27-33.DOI:10.7506/rlyj1001-8123-20210729-191.
[2] 张诗意, 唐楠, 黄攀, 等.威宁火腿中微生物的分离鉴定及其耐受特性[J].肉类研究, 2019, 33(8): 12-17.DOI:10.7506/rlyj1001-8123-20190625-147.
[3] ZHAO S S, YUE J Z, WANG Y, et al.The regulation of volatile flavor compounds in fermented meat products mediated by microorganisms:a review[J].Food Bioscience, 2024, 62: 105180.DOI:10.1016/j.fbio.2024.105180.
[4] LEROY F, VERLUYTEN J, DE VUYST L.Functional meat starter cultures for improved sausage fermentation[J].International Journal of Food Microbiology, 2006, 106(3): 270-285.DOI:10.1016/j.ijfoodmicro.2005.06.027.
[5] CHEN Q, LIU Q, SUN Q X, et al.Flavour formation from hydrolysis of pork sarcoplasmic protein extract by a unique LAB culture isolated from Harbin dry sausage[J].Meat Science, 2015, 100: 110-117.DOI:10.1016/j.meatsci.2014.10.001.
[6] 孔保华, 李悦欣, 张欢, 等.乳酸菌抗氧化活性及其在发酵肉制品中的应用研究进展[J].肉类研究, 2022, 36(10): 35-42.DOI:10.7506/rlyj1001-8123-20220801-089.
[7] WEN R X, SUI Y M, LIU J Q, et al.Co-inoculation of Debaryomyces hansenii and lactic acid bacteria: a strategy to improve the taste and odour profiles of dry sausages[J].Food Science and Human Wellness,2024, 13(6): 3273-3283.DOI:10.26599/fshw.2023.9250014.
[8] LORENZO J M, GÓMEZ M, PURRIÑOS L, et al.Effect of commercial starter cultures on volatile compound profile and sensory characteristics of dry-cured foal sausage[J].Journal of the Science of Food and Agriculture, 2016, 96(4): 1194-1201.DOI:10.1002/jsfa.7203.
[9] RAMOS-MORENO L, RUIZ-PÉREZ F, RODRÍGUEZ-CASTRO E,et al.Debaryomyces hansenii is a real tool to improve a diversity of characteristics in sausages and dry-meat products[J].Microorganisms,2021, 9(7): 1512.DOI:10.3390/microorganisms9071512.
[10] CANO-GARCÍA L, BELLOCH C, FLORES M.Impact of Debaryomyces hansenii strains inoculation on the quality of slow dry-cured fermented sausages[J].Meat Science, 2014, 96(4): 1469-1477.DOI:10.1016/j.meatsci.2013.12.011.
[11] CANO-GARCÍA L, RIVERA-JIMÉNEZ S, BELLOCH C, et al.Generation of aroma compounds in a fermented sausage meat model system by Debaryomyces hansenii strains[J].Food Chemistry, 2014,151: 364-373.DOI:10.1016/j.foodchem.2013.11.051.
[12] WEN R X, DONG Z X, LÜ Y C, et al.Comparative evaluation of the flavour-promoting role of autochthonous yeast strains on dry sausages[J].LWT-Food Science and Technology, 2023, 184: 115032.DOI:10.1016/j.lwt.2023.115032.
[13] ANDRADE M J, CÓRDOBA J J, CASADO E M, et al.Effect of selected strains of Debaryomyces hansenii on the volatile compound production of dry fermented sausage “salchichón”[J].Meat Science,2010, 85(2): 256-264.DOI:10.1016/j.meatsci.2010.01.009.
[14] MURGIA M A, MARONGIU A, APONTE M, et al.Impact of a selected Debaryomyces hansenii strain’s inoculation on the quality of Sardinian fermented sausages[J].Food Research International, 2019,121: 144-150.DOI:10.1016/j.foodres.2019.03.042.
[15] SUI Y M, ZHANG B Y, LIU J Q, et al.Screening and evaluating yeast strains with antioxidant potential from the traditional dry sausage of northern China[J].LWT-Food Science and Technology, 2024, 203:116395.DOI:10.1016/j.lwt.2024.116395.
[16] 肖亚庆, 陈从贵, 徐梅, 等.接种戊糖乳杆菌对腊肠品质的影响[J].肉类研究, 2017, 31(9): 38-43.DOI:10.7506/rlyj1001-8123-201709007.
[17] ŠKRLEP M, ČANDEK-POTOKAR M, BATOREK-LUKAČ N, et al.Aromatic profile, physicochemical and sensory traits of dry-fermented sausages produced without nitrites using pork from Krškopolje pig reared in organic and conventional husbandry[J].Animals, 2019, 9(2):55.DOI:10.3390/ani9020055.
[18] WEN R X, YIN X Y, HU Y Y, et al.Technological properties and flavour formation potential of yeast strains isolated from traditional dry fermented sausages in Northeast China[J].LWT-Food Science and Technology, 2022, 154: 112853.DOI:10.1016/j.lwt.2021.112853.
[19] LI X A, KONG B H, WEN R X, et al.Flavour compensation role of yeast strains in reduced-salt dry sausages: taste and odour profiles[J].Foods, 2022, 11(5): 650.DOI:10.3390/foods11050650.
[20] YANG P, ZHONG G X, YANG J C, et al.Metagenomic and metabolomic profiling reveals the correlation between the microbiota and flavor compounds and nutrients in fermented sausages[J].Food Chemistry, 2022, 375: 131645.DOI:10.1016/j.foodchem.2021.131645.
[21] PATRIGNANI F, IUCCI L, VALLICELLI M, et al.Role of surfaceinoculated Debaryomyces hansenii and Yarrowia lipolytica strains in dried fermented sausage manufacture.Part 1: Evaluation of their effects on microbial evolution, lipolytic and proteolytic patterns[J].Meat Science, 2007, 75(4): 676-686.DOI:10.1016/j.meatsci.2006.09.017.
[22] CORRAL S, BELLOCH C, LÓPEZ-DÍEZ J J, et al.Yeast inoculation as a strategy to improve the physico-chemical and sensory properties of reduced salt fermented sausages produced with entire male fat[J].Meat Science, 2017, 123: 1-7.DOI:10.1016/j.meatsci.2016.08.007.
[23] YANG X Y, XIAO S, WANG J H.Debaryomyces hansenii strains from traditional Chinese dry-cured ham as good aroma enhancers in fermented sausage[J].Fermentation, 2024, 10(3): 152.DOI:10.3390/fermentation10030152.
[24] PEREA-SANZ L, LÓPEZ-DÍEZ J J, BELLOCH C, et al.Counteracting the effect of reducing nitrate/nitrite levels on dry fermented sausage aroma by Debaryomyces hansenii inoculation[J].Meat Science, 2020,164: 108103.DOI:10.1016/j.meatsci.2020.108103.
[25] GALLEGO M, TOLDRÁ F, MORA L.Quantification and in silico analysis of taste dipeptides generated during dry-cured ham processing[J].Food Chemistry, 2022, 370: 130977.DOI:10.1016/j.foodchem.2021.130977.
[26] FLORES M, CORRAL S, CANO-GARCÍA L, et al.Yeast strains as potential aroma enhancers in dry fermented sausages[J].International Journal of Food Microbiology, 2015, 212: 16-24.DOI:10.1016/j.ijfoodmicro.2015.02.028.
[27] SMID E J, KLEEREBEZEM M.Production of aroma compounds in lactic fermentations[J].Annual Review of Food Science and Technology, 2014, 5(1): 313-326.DOI:10.1146/annurevfood-030713-092339.
[28] ESTÉVEZ M, VENTANAS S, HEINONEN M.Formation of Strecker aldehydes between protein carbonyls-α-aminoadipic and γ-glutamic semialdehydes-and leucine and isoleucine[J].Food Chemistry, 2011,128(4): 1051-1057.DOI:10.1016/j.foodchem.2011.04.012.
[29] CHEN Q, KONG B H, HAN Q, et al.The role of bacterial fermentation in lipolysis and lipid oxidation in Harbin dry sausages and its flavour development[J].LWT-Food Science and Technology,2017, 77: 389-396.DOI:10.1016/j.lwt.2016.11.075.
[30] OLIVARES A, NAVARRO J L, FLORES M.Characterization of volatile compounds responsible for the aroma in naturally fermented sausages by gas chromatography-olfactometry[J].Food Science and Technology International, 2015, 21(2): 110-123.DOI:10.1177/1082013213515500.
[31] MARCO A, NAVARRO J L, FLORES M.Quantitation of selected odor-active constituents in dry fermented sausages prepared with different curing salts[J].Journal of Agricultural and Food Chemistry,2007, 55(8): 3058-3065.DOI:10.1021/jf0631880.