乳化肉制品因其蛋白质含量高、口感鲜嫩多汁等特点深受消费者喜爱。这类肉制品的制备通常基于肌原纤维蛋白(myofibrillar protein,MP)的乳化特性,将原料肉、盐和水混合,在低温条件下,MP作为天然乳化剂乳化动物脂肪,最终形成稳定的凝胶状产品[1]。然而,随着人们健康意识的提升,消费者对肉制品中高饱和脂肪酸及胆固醇可能引发的健康风险日益关注,因此开发动物脂肪替代策略成为肉品科学领域的研究热点。
亚麻籽油(linseed oil,LO)因富含亚油酸和α-亚麻酸等不饱和脂肪酸而备受关注[2],其中α-亚麻酸作为必需脂肪酸,具有降低胆固醇和预防心血管疾病等多种生理功能[3]。然而,Liu Dengmei等[4]发现植物油直接替代背膘会导致乳液型香肠储能模量(G’)与损耗模量(G”)比值下降,进而削弱产品质构特性。为解决这一问题,将植物油乳化制成稳定乳液后再替代动物脂肪成为可行方案。亚麻籽胶(flaxseed gum,FG)是从亚麻籽中提取的天然植物胶体,其黏度高且具有良好的乳化性能[5-7]。Wang Yong[8]、Zhao Qiangzhong[9]等研究表明,FG可通过与其他乳化剂协同作用提升乳液稳定性。本团队前期研究发现,FG与LO形成的预乳液可有效替代乳化肠中的动物脂肪,表现出良好的替代效果[10]。然而,MP作为肉糜乳化体系的核心功能蛋白,FG与MP在乳化过程中的相互作用机制,尤其是FG对MP界面吸附行为、构象变化及复合界面膜形成的影响尚未得到系统阐释。目前,关于FG的研究多集中于其提取参数、单一FG对大豆油/橄榄油/玉米油乳液的稳定作用,以及FG与其他蛋白乳化剂乳液的交互效应[11-13],而针对FG稳定LO乳液的界面行为及其在复合乳化体系(FG-MP)中的作用机制研究仍较匮乏。因此,本研究系统探究不同质量分数(0.8%、1.0%、1.2%)FG单一或与MP复配作为乳化剂对MP乳液界面特性与稳定性的影响,并从油-水界面特性角度解析其作用机制。
1 材料与方法
1.1 材料与试剂
新鲜猪里脊 市购。
LO 益海嘉里金龙鱼粮油食品股份有限公司;FG青岛德慧海洋生物科技有限公司;氯化镁、氯化钠、磷酸二氢钠、磷酸氢二钠、乙二胺四乙酸、氢氧化钠、酒石酸钾钠等试剂均为国产分析纯。
1.2 仪器与设备
T25数显型匀浆机 德国IKA集团;90Plus Zeta电位仪 美国Brookhaven仪器公司;Legend Micro21R台式微量离心机 美国Thermo Fisher Scientific公司;尼康80-i光学显微镜 北京瑞科中仪科技有限公司;HR-1流变仪 美国TA公司;F-V-1000激光共聚焦显微镜日本Olympus公司;OCA 25视频光学接触角测量仪北京东方德菲仪器有限公司。
1.3 方法
1.3.1 MP提取
根据Park等[14]的方法,在4 ℃下将新鲜猪里脊切碎,称质量后放入烧杯,加入4 倍体积的冰提取液(0.1 mol/L NaCl、2 mmol/L MgCl2、1 mmol/L乙二胺四乙酸、6.1 mmol/L Na2HPO4、3.9 mmol/L NaH2PO4,pH 7.0),匀浆2 次(每次30 s),5 000 r/min离心15 min,弃去上清液,重复上述操作2 次,得到粗纤维蛋白沉淀物。然后加入4 倍体积的冰洗液(0.1 mol/L NaCl),匀浆,5 000 r/min离心15 min,弃去上清液,重复上述操作1 次。最后加入4 倍体积的冰洗液,匀浆,4 层纱布过滤,采用0.1 mol/L HCl溶液调节pH值至6.0,5 000 r/min离心15 min得到MP。采用双缩脲法测定MP质量浓度,并用缓冲液(0.6 mol/L NaCl、50 mmol/L Na2HPO4/NaH2PO4,pH 7.0)将其调至10 mg/mL备用。
1.3.2 乳液制备
乳液制备参考Feng Meiqin等[12]的方法并略作调整。
FG乳液:将不同质量FG溶解于200 mL去离子水,采用磁力搅拌器充分搅拌以确保其完全水化,于4 ℃冰箱中隔夜水合。加入LO(LO∶FG=1∶9,m/m),12 500 r/min均质3 次,每次1 min,间隔30 s,得FG质量分数分别为0.8%、1.0%、1.2%,LO质量分数为10%的FG乳液。
FG-MP乳液:将不同质量FG加入MP溶液,300 r/min磁力搅拌2 h,充分混匀即得FG-MP混合物,将其与LO以9∶1(m/m)混合,12 500 r/min均质3 次,每次1 min,间隔30 s,得FG质量分数分别为0.8%、1.0%、1.2%,LO质量分数为10%,MP质量浓度为10 mg/mL的FG-MP乳液。
按上述方法制备不加FG的MP乳液,作为对照组。制备好的乳液于4 ℃贮藏备用。
1.3.3 贮藏稳定性测定
根据Liu Fu等[15]的方法并略作调整。将新鲜乳液转移至玻璃样品瓶中(10 mL),拧紧瓶盖防止样品蒸发,FG乳液、MP乳液、FG-MP乳液在室温下贮藏22 d,观察乳液分层情况,并拍照记录。
1.3.4 流变特性测定
参考Sun Jian等[11]的方法并略作调整。使用流变仪测定乳液的流变特性。在温度25 ℃、剪切速率0.01~100 s-1条件下测定样品表观黏度;在角频率1~100 rad/s、应力2%条件下测定样品G’和G”。
1.3.5 Zeta电位测定
参照Han Yu等[16]的方法并略作修改。使用去离子水将乳液稀释50 倍,充分混匀后转移至测定皿,使用Zeta电位仪测定乳液的Zeta电位,仪器参数:光散射角17°、激光波长633 nm、He/Ne气体激光源。
1.3.6 微观结构观察
1.3.6.1 光学显微镜观察
参照Xiong Wenfei等[17]的方法并略作修改。将未经稀释的乳液滴加到载玻片中央,为避免产生气泡,小心盖上盖玻片,轻轻放于载物台上,在10 倍放大倍数下进行观察。
1.3.6.2 激光共聚焦显微镜观察
采用Hu Hongyan等[18]的方法并略作修改。取0.5 mL新鲜乳液置于2 mL离心管中,使用等体积去离子水将样品稀释,均匀分散后,依次加入20 μL多糖染液(钙荧光白,10 mg/mL)、20 μL蛋白染液(尼罗蓝,10 mg/mL)及20 μL脂肪染液(尼罗红,10 mg/mL),涡旋1 min混合均匀,避光反应5 min,取20 μL混合物滴加于载玻片,采用40 倍物镜观察。激发波长分别为405 nm(钙荧光白)、633 nm(尼罗蓝)和488 nm(尼罗红)。
1.3.7 界面特性测定
1.3.7.1 界面蛋白吸附量测定
根据Liang Hanni等[19]的方法并略作修改。使用等体积去离子水将样品稀释,将一定量稀释后乳液转移至10 mL离心管中,4 ℃、10 000 r/min离心30 min。采用注射器吸取下层清液,过0.45 μm滤膜,使用BCA法测定蛋白质量浓度,按式(1)计算界面蛋白吸附量:
式中:ρi为总蛋白质量浓度/(mg/mL);ρf为未吸附蛋白质量浓度/(mg/mL);φ为油相体积分数;d3,2为乳液表面平均粒径/μm。
1.3.7.2 界面压力测定
根据Xiong Wenfei等[17]的方法并略作修改。采用注射器吸取一定量去离子水、10 mg/mL MP或0.8%、1.0%、1.2% FG与FG-MP溶液,排除气泡后,将1 滴10 μL液体注入装有LO的玻璃比色杯中,在针尖持续10 800 s以实现样品吸附。使用接触角测量仪持续记录液滴图像。按式(2)计算油-水界面压力(π):
式中:γ0为去离子水与油相间的界面张力/(mN/m);γ为MP、FG及FG-MP溶液与油相间的界面张力/(mN/m)。
为进一步分析FG在油-水界面的渗透速率常数(Kp)和重排速率常数(Kr),采用一阶方程拟合吸附过程,如式(3)所示:
式中:π10 800、π0、πt分别为吸附平衡、初始及任意时刻t的界面压力/(mN/m);Ki为一阶速率常数/s-1。
1.3.7.3 界面膨胀特性测定
依据Xiong Wenfei等[20]的方法并略作调整。样品处理同1.3.7.2节,采用接触角测量仪测定界面膨胀特性。参数设置:振幅10%、频率0.1 Hz、吸附时间10 800 s。通过5 次正弦振荡循环直至样品吸附,由系统软件计算扩张模量(E)、弹性模量(Ed)。
1.4 数据处理
实验重复3 次,每个实验均设置3 个平行,采用SPSS 26软件进行数据分析。采用方差分析进行组间差异比较,采用Duncan多重比较进行显著性分析,以P<0.05表示差异显著;采用Origin 2021软件绘图。
2 结果与分析
2.1 FG对MP乳液贮藏稳定性的影响
由图1A可知,在FG乳液中,随着FG含量的增加,乳液相分离时间呈现延长趋势。FG质量分数为0.8%时,乳液体系稳定性最低,仅贮藏7 d即出现分层现象;FG质量分数为1.0%时,贮藏17 d出现分层。由此可见,当FG质量分数超过0.8%时,乳液体系表现出抗分层稳定性,稳定性明显增强。其原因可能是:一方面,FG含量增加导致更多FG分子吸附于油滴界面,乳液体系黏度升高,油相分子运动受限,稳定性提高;另一方面,FG阴离子多糖的负电荷特性能够增强乳液体系的整体电位绝对值,静电斥力随之增大,进而有效阻止液滴聚集,稳定性提高。使用0.1%~0.5% FG乳化大豆油、橄榄油或猪油[11-12,21]时,同样观察到FG含量增加可延长相分离时间现象,提升乳液体系稳定性。

图1 贮藏过程中FG乳液(A)及MP乳液与FG-MP乳液(B)分层情况
Fig.1 Stratification of emulsions with FG (A), MP or their combination (B) during storage
由图1B可知,MP乳液体系在贮藏1 d即发生分层现象,这可能归因于MP在中性环境下携带微量负电荷,导致MP乳液体系的静电相互作用较弱,难以有效抑制液滴聚集,易发生分层。此时,FG-MP乳液体系未出现分层,表明FG的加入能够有效提高乳液的稳定性。其中,含0.8%、1.0% FG的乳液体系分别在贮藏12 d和贮藏22 d出现分层,明显晚于相同FG含量的单一FG乳液,表明FG与MP复配在稳定乳液方面具有协同效应。当FG质量分数升至1.2%时,无论是单一FG乳液还是FG-MP乳液,贮藏21 d后均未出现分层现象,表明FG质量分数为1.2%时形成的乳液具有较佳的长期贮藏稳定性。
2.2 FG对MP乳液流变特性的影响
由图2A可知,各组乳液均表现出典型的非牛顿流体特性,其表观黏度随剪切速率的增加而降低,表现出剪切稀释行为。剪切速率较低时,乳液体系中的液滴分子因剪切力作用发生拉伸变形并形成聚集体网络结构,导致连续相中产生较强的流动阻力,从而使乳液体系呈现较高的初始表观黏度。随着剪切速率增大,聚集态分子发生解离且解离速率大于重组速率,导致液滴间相互作用减弱、网络结构破坏,表观黏度快速下降。值得注意的是,相较于MP乳液,FG乳液与FG-MP乳液的表观黏度均明显提高,且表观黏度随FG含量的增加而增加。在相同FG含量条件下,FG-MP乳液表现出更高的表观黏度,表明FG-MP乳液的稳定性更强。黏度增加可通过降低乳化剂在油-水界面的扩散速率(Kdiff)、限制油滴在水相中的运动,有效防止油滴间碰撞与聚集,进而提升乳液体系稳定性[22]。
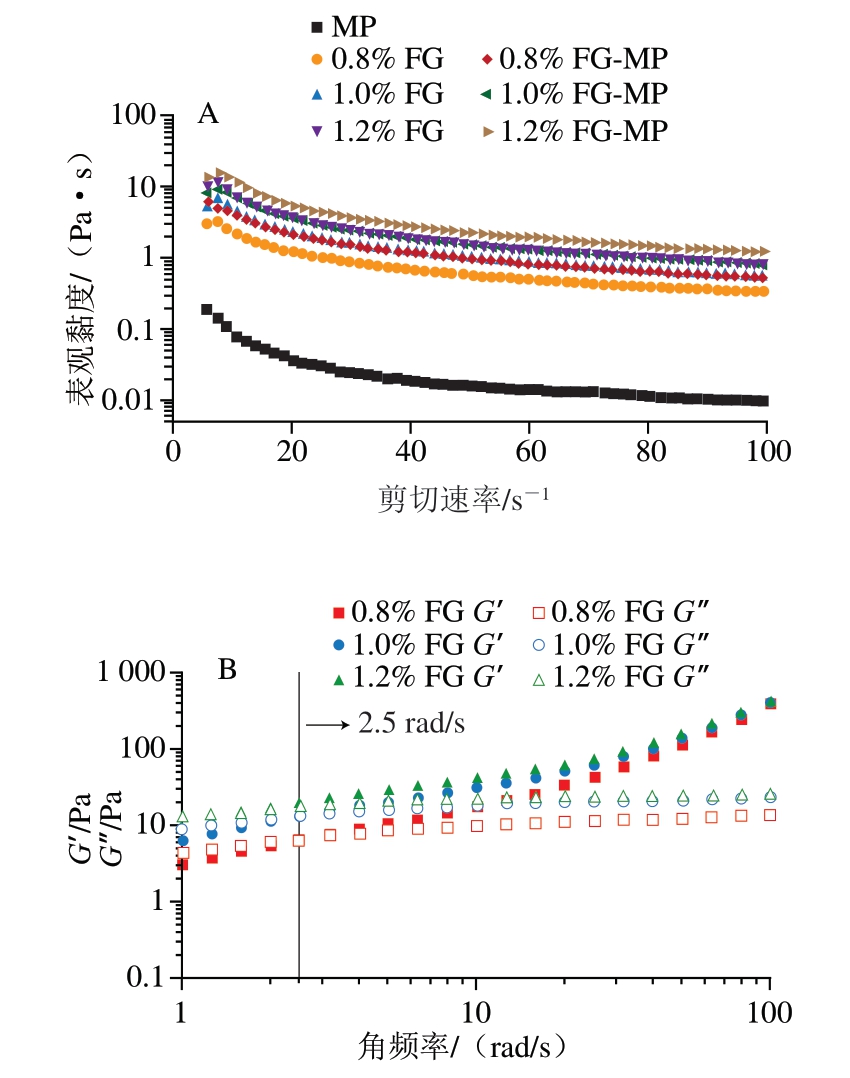
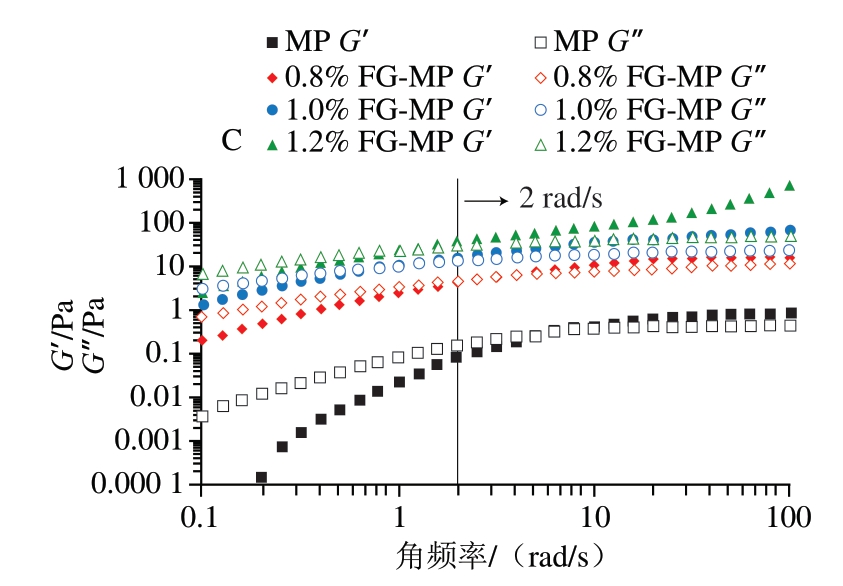
图2 MP乳液、FG乳液、FG-MP乳液的表观黏度(A)及FG乳液(B)与FG-MP乳液(C)的G’和G”
Fig.2 Apparent viscosity of MP, FG and FG-MP emulsions (A),storage modulus (G’) and loss modulus (G”) of FG (B) and FG-MP emulsions (C)
由图2B、C可知,较低角频率区,各组乳液G”均大于G’,表明此时乳液体系以黏性为主;随着角频率增大,G’与G”出现交叉点,最终所有乳液体系的G’均高于G”,这种模量转变行为证实乳液形成了具有类凝胶特性的三维网络结构。与MP乳液,FG-MP乳液中FG的存在显著提高了乳液的G’和G”(图2C)。值得注意的是,相较于MP乳液和单一FG乳液相比,FG-MP乳液的模量交叉点向低角频率方向移动,表明FG-MP乳液的刚性结构更强,稳定性更好,这与贮藏稳定性结果一致。可以推测FG与MP在稳定乳液方面具有协同作用,可能是由于FG能够促进油-水界面或连续相中MP与FG之间的相互作用,有利于乳液网络结构的形成。
2.3 FG对MP乳液Zeta电位的影响
Zeta电位是判断分散体系稳定性的重要指标,能够有效反映溶液中带电颗粒间的静电相互作用强度。由图3可知,FG乳液Zeta电位绝对值随着FG含量的增加呈现显著上升趋势(P<0.05)。该结果与前人研究[11-13]结果一致,这可能是由于FG作为一种阴离子多糖,随着其含量的增加,乳化体系中有足够的FG包裹油滴,液滴表面覆盖的FG增多,负电荷增加,液滴间静电斥力增强,Zeta电位绝对值增加,乳液稳定性得以提升。MP乳液的Zeta电位绝对值最低,表明仅含10 mg/mL MP的乳液体系静电相互作用较弱,不足以维持乳液稳定性。随着FG的不断加入,FG-MP乳液的Zeta电位绝对值显著升高(P<0.05),表明FG-MP可通过提高静电斥力维持乳液的稳定性。
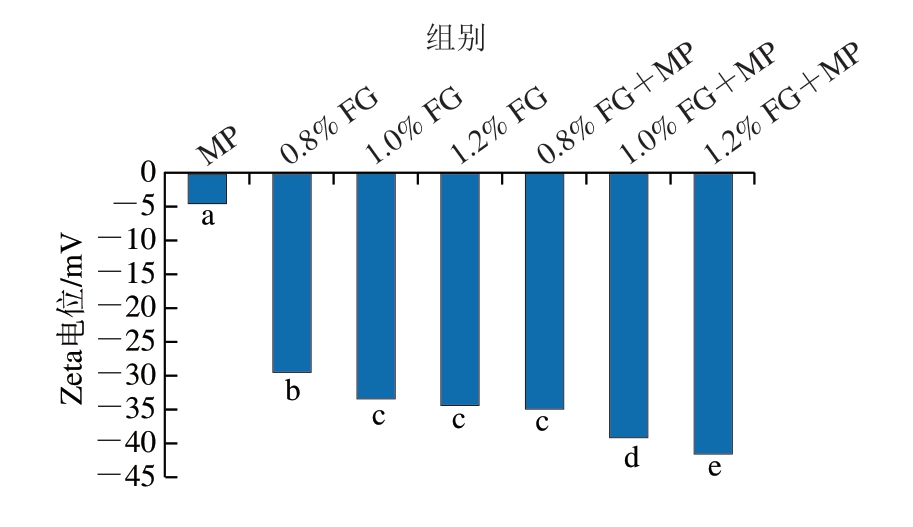
图3 FG乳液、MP乳液、FG-MP乳液的Zeta电位
Fig.3 Zeta potentials of FG, MP and FG-MP emulsions
小写字母不同表示差异显著(P<0.05)。
2.4 FG对MP乳液微观结构的影响
由图4A可知,MP乳液体系中存在较大液滴,且存在明显的絮凝与聚集现象,乳液失稳,表明10 mg/mL MP不足以覆盖油滴形成稳定乳液。FG乳液中,含0.8% FG乳液的液滴较大,但随着FG含量的增加,液滴尺寸逐渐变小,分布趋于均匀。相较于FG乳液,FG-MP乳液的液滴尺寸更小、分布更均匀且集中,表明FG与MP复配作为乳化剂可有效降低液滴大小,提高乳液体系的稳定性。这一现象进一步证明FG与MP对乳液体系的协同稳定效应。FG的阴离子多糖特性通过增强静电斥力防止液滴聚集,而MP分子则通过疏水相互作用在界面形成更致密的吸附层,二者的复配使用可有效降低界面张力,促进乳滴细化。这与流变学特性和Zeta电位结果相互印证。
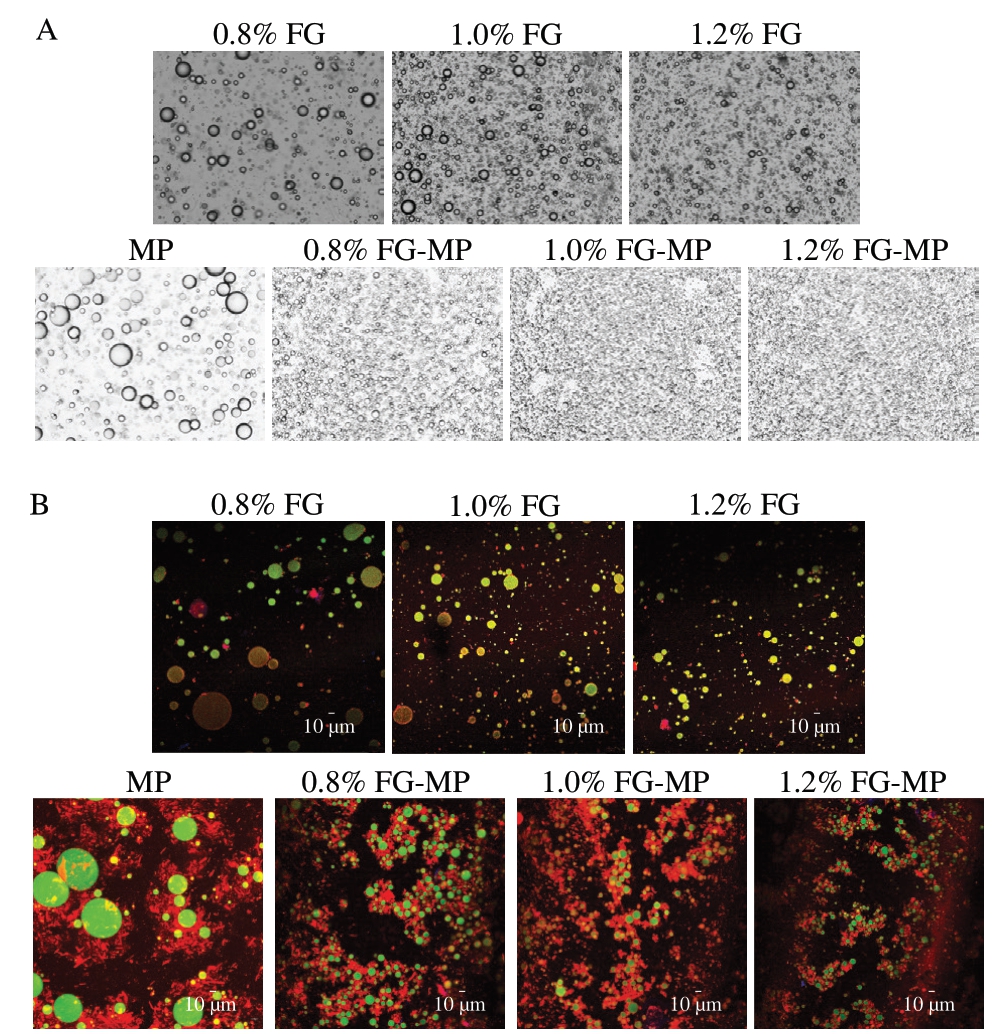
图4 FG乳液、MP乳液、FG-MP乳液的光学显微镜图(A)和激光共聚焦显微镜图(B)
Fig.4 Optical microscope images (A) and laser confocal microscope images (B) of FG, MP and FG-MP emulsions
绿色区域为油滴,红色区域为蛋白质组分。
由图4B可知,MP乳液体系中的油滴表面(绿色)并未形成完整的蛋白吸附层(红色区域分布不均),油滴尺寸较大且分布不均,表明10 mg/mL MP作为乳化剂不足以乳化全部油滴,未被乳化的油滴易聚集形成大油滴,造成乳液失稳。在FG乳液中,当FG含量较低时,乳液中可观察到较大的游离油滴,一些油滴表面甚至无蛋白吸附。随着FG含量的增加,油滴尺寸逐渐降低且分布趋于均一,乳液稳定性提高,FG乳业体系的高黏度效应可减少界面分子之间的相互接触和碰撞,阻止油滴聚集,从而导致油滴尺寸较小。在FG-MP乳液中,可明显观察到油滴被完整的蛋白质膜包覆,并均匀分散在三维凝胶网络结构中。
2.5 FG对MP乳液界面特性的影响
2.5.1 界面蛋白吸附量
由图5可知,随着FG含量的增加,界面蛋白吸附量略有增加,但各组间差异不显著(P>0.05),表明FG对乳液稳定性的影响机制并非以界面蛋白吸附量变化为主导。FG作为一种酸性阴离子多糖,其结构中的羧酸根基团可在水相中解离并携带负电荷,在MP乳液体系中,FG可能通过静电相互作用与带负电荷的MP结合,二者共同吸附于油-水界面,从而在一定程度上提高界面蛋白吸附量。此外,随着FG含量的增加,未吸附至界面的FG分子与MP可能发生热力学不相容现象,引发相分离并进一步促使蛋白质向界面扩散吸附,导致界面蛋白吸附量进一步上升[23-24]。缪雨雁等[23]在MP乳液中添加阿拉伯胶和瓜尔豆胶,当多糖质量分数超过0.2%时,界面蛋白吸附量略有提升,但无显著差异,与本研究结果相一致。
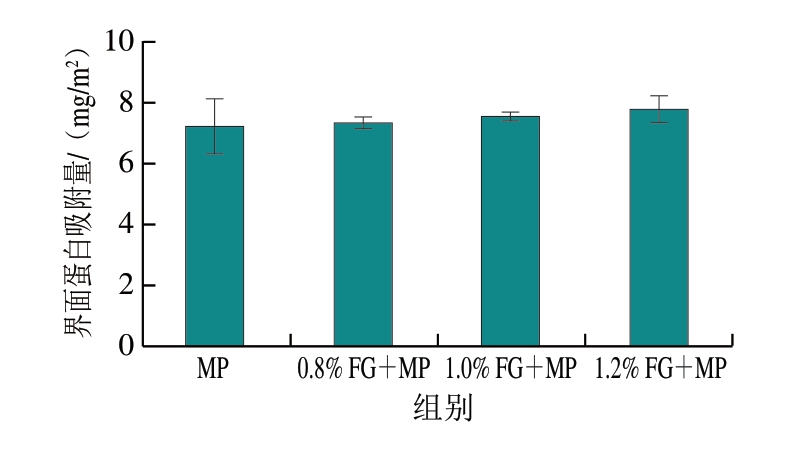
图5 MP与FG-MP乳液的界面蛋白吸附量
Fig.5 Interfacial protein adsorption amount of MP and FG-MP emulsions
2.5.2 界面压力与吸附动力学
由图6可知,所有乳液的π均随吸附时间的延长而呈上升趋势,表明MP、FG-MP、FG在油-水界面的吸附量逐渐增加[25]。值得注意的是,FG乳液的π始终低于MP乳液,这可能与FG的胶体复杂性有关:其分子结构不利于形成致密的界面膜,且疏水基团含量相对较少,导致其与油相的相互作用较弱[26]。相比之下,MP分子结构中含有大量疏水氨基酸,能够与油相产生较强的相互作用,从而形成更稳定的界面蛋白膜。然而,MP乳液的π低于FG-MP乳液,表明FG-MP乳液的界面活性明显提高,这可能是由于FG作为具有表面活性的乳化剂可与MP协同乳化油滴,提升油-水界面的界面活性,从而使FG-MP乳液的π增加。随着FG含量的增加,FG乳液的π增大,这可能是由于油-水界面吸附的FG分子增多,乳液静电斥力增强[9],这与Zeta电位结果一致。当FG质量分数为0.8%时,FG-MP乳液的π最大,这可能是由于乳液黏度随FG含量的增加而增加,FG质量分数为1.0%、1.2%时,乳液更加黏稠,阻碍MP扩散。
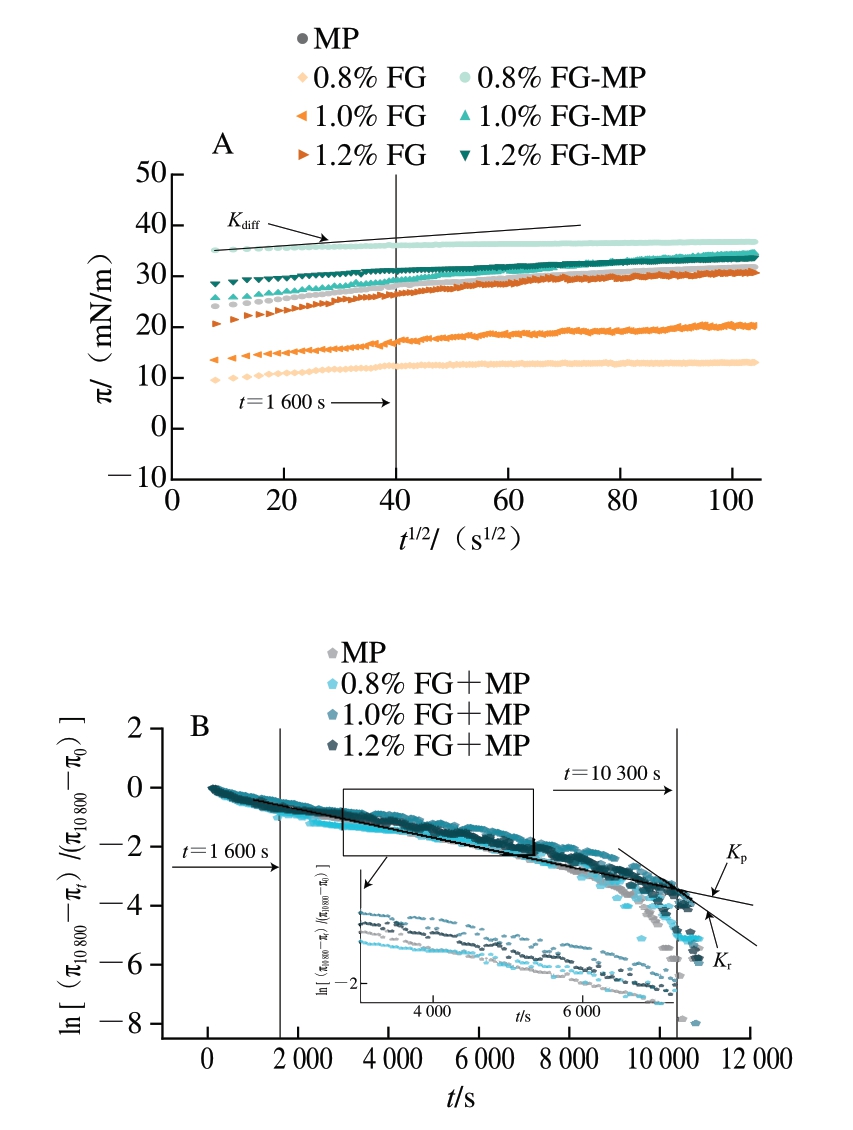
图6 FG、MP和FG-MP乳液的界面压力动力学曲线(A)及MP、FG-MP在油-水界面的分子渗透和构象重排动力学曲线(B)
Fig.6 Kinetic curves of interfacial pressure of FG, MP and FG-MP emulsions (A), and kinetic curves of molecular permeation and conformational rearrangement of MP and FG-MP emulsions at the oil-water interface (B)
由表1可知,与MP相比,FG-MP的Kdiff、Kp和Kr绝对值均显著降低(P<0.05),表明FG的加入能够影响MP分子在油-水界面的吸附动力学行为,具体表现为扩散、渗透和重排过程受到抑制。Kdiff降低可能是由于FG作为高分子多糖,在界面可能与MP发生竞争性吸附,同时复合乳液体系黏度增强,FG-MP复合物分子向界面的迁移运动受到阻碍,Kdiff降低,该结果和Wang Shengnan等[27]的研究结果一致,其在0.05%~0.15%(m/m)大豆壳多糖对大豆分离蛋白乳液吸附动力学行为的影响研究中也观察到π上升而Kdiff下降现象,这可能是由于大豆壳多糖对大豆分离蛋白分子在油-水界面的扩散具有阻碍作用。随着FG含量的增加,FG-MP在油-水界面的Kdiff呈增大趋势,这可能源于FG含量的持续增加促使FG和MP之间发生热力学不相容性,引发容积排阻效应,从而促使蛋白质分子更易向界面迁移与扩散,Kdiff增大。由FG含量增加引起的Kp和Kr绝对值下降可能是因为FG作为高黏性亲水胶体,含量增加将引起其与MP分子在油-水界面发生缠结,导致分子在界面的渗透嵌入行为和构象重排能力受到抑制。
表1 MP和FG-MP乳液的界面吸附动力学参数
Table 1 Interfacial adsorption kinetic parameters of MP and FG-MP emulsions

注:同列小写字母不同表示差异显著(P<0.05)。
组别Kdiff/(mN/(m·s1/2))Kp/(104 s-1)Kr/(104 s-1)MP0.126±0.006a-6.421±0.140d-26.23±1.51d 0.8% FG-MP0.029±0.004d-4.246±0.321c-22.17±2.68c 1.0% FG-MP0.093±0.008c-3.082±0.019a-8.50±0.33b 1.2% FG-MP0.109±0.006b-3.807±0.124b-5.38±0.32a
2.5.3 界面膨胀特性
界面膜的膨胀流变特性可有效反映生物聚合物分子在油-水界面的吸附行为与界面膜力学性能,是预测乳液稳定性及分子间相互作用的重要指标[28]。由图7A、B可知,随着吸附时间的延长,乳液体系的E和Ed均逐渐增加,表明油-水界面吸附的生物聚合物逐渐增多,且形成的界面膜弹性逐渐增强。有研究[29]表明,油-水界面吸附的分子间作用力(如静电斥力、空间位阻和疏水相互作用等)增强可破坏分子中蛋白质的原始构象,促使其展开和重排,并在界面上彼此交联形成具有一定厚度和黏弹性的界面膜,最终表现为界面黏弹性增强。Ed接近E,表明乳液的界面膜主要表现为弹性。值得注意的是,FG的引入有效提高了界面膜的Ed,表明界面弹性增强,可能是由于界面吸附的FG和MP分子之间发生相互作用,且这种相互作用随FG含量增加而逐渐增强[30]。
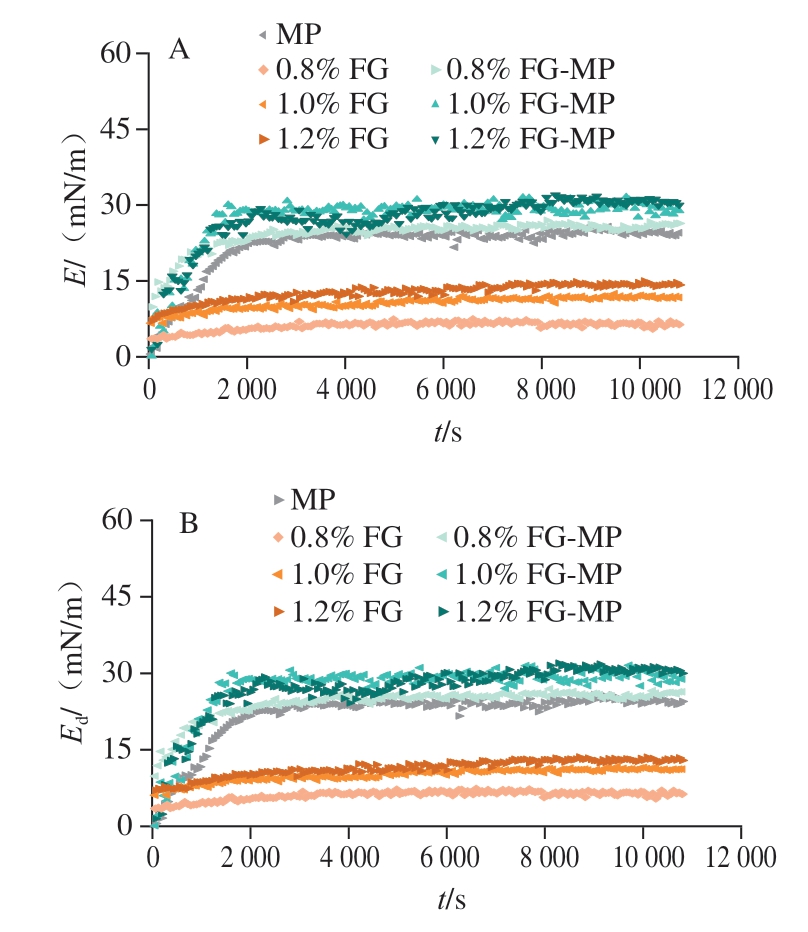
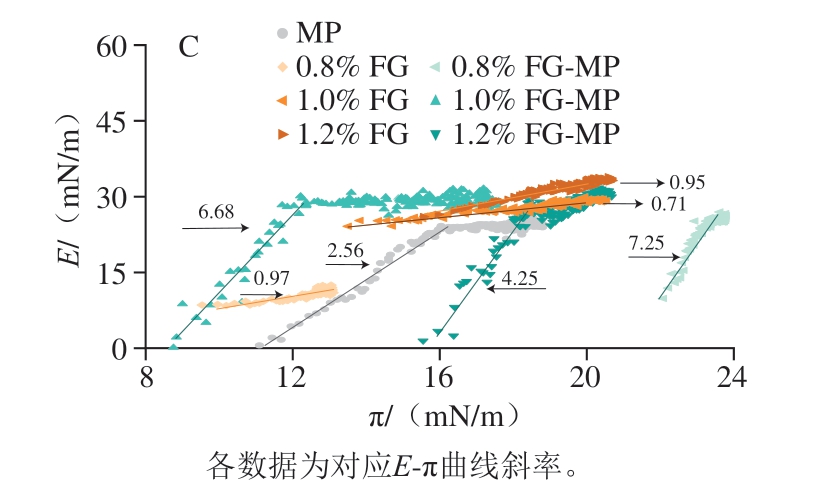
图7 FG、MP和FG-MP乳液油-水界面E(A)和Ed(B)动态演变及E随界面压力的变化(C)
Fig.7 Dilational modulus (A) and elastic modulus (B) at the oil-water interface of FG, MP, and FG-MP emulsions as a function of adsorption time and changes in dilational modulus with interfacial pressure (C)
由图7C可知,FG乳液E随π的增加而增加,且各组E-π曲线斜率均小于1.0,表明油-水界面处的FG之间的相互作用较弱。相反,FG-MP乳液的E-π曲线斜率均大于1.0,表明MP和FG分子之间存在较强的相互作用[31]。相比于MP乳液,FG-MP乳液的E-π曲线斜率增大,表明FG的加入使油-水界面处的蛋白质吸附量增加,分子间相互作用增强,有利于形成更致密、稳定的界面膜结构,从而提升乳液的整体稳定性。
3 结 论
FG质量分数为1.2%时,MP乳液的贮藏稳定性最好,随着FG含量的增加,各液滴之间的静电相互作用增强;同时FG作为亲水胶体可通过增加连续相黏度提升乳液的表观黏度,增强乳液的刚性结构,并使乳液的界面蛋白吸附量增加。激光共聚焦显微镜图像表明,较高含量的FG与MP形成的乳液油滴分布更为均匀、一致。FG和MP在油-水界面处的吸附行为表明,FG对MP分子的扩散、渗透和重排行为存在负面影响,但可通过与MP分子的相互作用在油-水界面形成高弹性界面膜。综上,FG主要基于提高乳化体系的黏度与增强界面分子间相互作用提高MP乳液稳定性。本研究可为FG-LO预乳液作为脂肪替代物在低脂肉制品中的应用提供理论参考。
[1] YANG B R, LIU J, LAN M, et al.Unravelling the enhancement of myofibrillar protein gel properties induced by marine phospholipids:a structure, water state and intermolecular interactions study[J].LWTFood Science and Technology, 2025, 223: 117681.DOI:10.1016/j.lwt.2025.117681.
[2] 孙宏涛, 马燕, 郭洪涛, 等.乳液体系包埋亚麻籽油研究进展[J].食品工业科技, 2022, 43(24): 444-451.DOI:10.13386/j.issn1002-0306.2021120221.
[3] 赖玉萍, 姜福全, 黄思苑, 等.亚麻籽油的营养成分、功能活性及应用研究进展[J].中国油脂, 2022, 47(8): 109-115.DOI:10.19902/j.cnki.zgyz.1003-7969.210389.
[4] LIU D M, XU Y, ZENG X M, et al., Replacement of backfat with vegetable oils or their oleogels in emulsion-type sausage significantly change the digestibility of meat protein[J].Food Chemistry, 2025,463(Pt 1): 141149.DOI:10.1016/j.foodchem.2024.141149.
[5] 马兰雪, 李曦, 邹玉峰, 等.亚麻籽胶功能性质及其在食品中的应用进展[J].食品安全质量检测学报, 2021, 12(7): 2722-2727.DOI:10.19812/j.cnki.jfsq11-5956/ts.2021.07.034.
[6] 王维义, 许帅强, 何宏燕, 等.亚麻籽的营养成分及功能研究进展[J].中国油脂, 2020, 45(4): 83-85.DOI:10.12166/j.zgyz.1003-7969/2020.04.017.
[7] 杨振东, 李文博, 程婕, 等.亚麻籽胶-魔芋胶复合凝胶体系的制备及特性研究[J].天津科技大学学报, 2024, 39(2): 8-15.DOI:10.13364/j.issn.1672-6510.20230018.
[8] WANG Y, LI D, WANG L J, et al.The effect of addition of flaxseed gum on the emulsion properties of soybean protein isolate (SPI)[J].Journal of Food Engineering, 2011, 104(1): 56-62.DOI:10.1016/j.jfoodeng.2010.11.027.
[9] ZHAO Q Z, LONG Z, KONG J, et al.Sodium caseinate/flaxseed gum interactions at oil-water interface: effect on protein adsorption and functions in oil-in-water emulsion[J].Food Hydrocolloids, 2015, 43:137-145.DOI:10.1016/j.foodhyd.2014.05.009.
[10] 唐月利, 贾娜, 杨松涛, 等.亚麻籽胶-亚麻籽油乳液替代脂肪对乳化肠品质特性的影响[J].食品科学, 2023, 44(10): 64-72.DOI:10.7506/spkx1002-6630-20220818-207.
[11] SUN J, LIU W Y, FENG M Q, et al.Characterization of olive oil emulsions stabilized by flaxseed gum[J].Journal of Food Engineering,2019, 247: 74-79.DOI:10.1016/j.jfoodeng.2018.11.023.
[12] FENG M Q, WANG M, SUN J, et al.Stabilization of soybean oil by flaxseed gum and NMR characterization of its oil-water interface[J].CyTA-Journal of Food, 2019, 17(1): 892-899.DOI:10.1080/19476337.2019.1663266.
[13] 冯美琴, 孙健, 杨勇胜, 等.亚麻籽胶对玉米油乳状液乳化特性的影响[J].南京农业大学学报, 2019, 42(6): 1167-1172.DOI:10.7685/jnau.201906015.
[14] PARK D, XIONG Y L, ALDERTON A L.Concentration effects of hydroxyl radical oxidizing systems on biochemical properties of porcine muscle myofibrillar protein[J].Food Chemistry, 2007, 101(3):1239-1246.DOI:10.1016/j.foodchem.2006.03.028.
[15] LIU F, TANG C H.Emulsifying properties of soy protein nanoparticles: influence of the protein concentration and/or emulsification process[J].Journal of Agricultural and Food Chemistry,2014, 62(12): 2644-2654.DOI:10.1021/jf405348k.
[16] HAN Y, CHENG Z, ZHANG Y T, et al.Effect of metal ions and pH on the emulsifying properties of polysaccharide conjugates prepared from low-grade green tea[J].Food Hydrocolloids, 2020, 102: 105624.DOI:10.1016/j.foodhyd.2019.105624.
[17] XIONG W F, REN C, TIAN M, et al.Emulsion stability and dilatational viscoelasticity of ovalbumin/chitosan complexes at the oil-in-water interface[J].Food Chemistry, 2018, 252: 181-188.DOI:10.1016/j.foodchem.2018.01.067.
[18] HU H Y, XING L J, HU Y Y, et al.Effects of regenerated cellulose on oil-in-water emulsions stabilized by sodium caseinate[J].Food Hydrocolloids, 2016, 52: 38-46.DOI:10.1016/j.foodhyd.2015.06.019.
[19] LIANG H N, TANG C H.Emulsifying and interfacial properties of vicilins: role of conformational flexibility at quaternary and/or tertiary levels[J].Journal of Agricultural and Food Chemistry, 2013, 61(46):11140-11150.DOI:10.1021/jf403847k.
[20] XIONG W F, REN C, LI J, et al.Characterization and interfacial rheological properties of nanoparticles prepared by heat treatment of ovalbumin-carboxymethylcellulose complexes[J].Food Hydrocolloids,2018, 82: 355-362.DOI:10.1016/j.foodhyd.2018.03.048.
[21] LIU W Y, FENG M Q, WANG M, et al.Influence of flaxseed gum and NaCl concentrations on the stability of oil-in-water emulsions[J].Food Hydrocolloids, 2018, 79: 371-381.DOI:10.1016/j.foodhyd.2018.01.010.
[22] TAMNAK S, MIRHOSSEINI H, TAN C P, et al.Physicochemical properties, rheological behavior and morphology of pectin-pea protein isolate mixtures and conjugates in aqueous system and oil in water emulsion[J].Food Hydrocolloids, 2016, 56: 405-416.DOI:10.1016/j.foodhyd.2015.12.033.
[23] 缪雨雁, 曹燕, 立静芝, 等.不同黏度多糖阿拉伯胶和瓜尔胶对肌原纤维蛋白乳化性质的影响[J].食品科学, 2023, 44(6): 57-64.DOI:10.7506/spkx1002-6630-20220710-103.
[24] DU F F, QI Y, HUANG H B, et al.Stabilization of O/W emulsions via interfacial protein concentrating induced by thermodynamic incompatibility between sarcoplasmic proteins and xanthan gum[J].Food Hydrocolloids, 2022, 124: 107242.DOI:10.1016/j.foodhyd.2021.107242.
[25] CUEVAS-BERNARDINO J C, LOBATO-CALLEROS C, ROMÁNGUERRERO A, et al.Physicochemical characterisation of hawthorn pectins and their performing in stabilising oil-in-water emulsions[J].Reactive and Functional Polymers, 2016, 103: 63-71.DOI:10.1016/j.reactfunctpolym.2016.03.024.
[26] 杨书会, 王延圣, 王文亮, 等.多糖乳液的制备、乳化特性的影响因素及其应用研究进展[J].食品工业科技, 2024, 45(14): 398-407.DOI:10.13386/j.issn1002-0306.2023080229.
[27] WANG S N, YANG J J, SHAO G Q, et al.Soy protein isolatedsoy hull polysaccharides stabilized O/W emulsion: effect of polysaccharides concentration on the storage stability and interfacial rheological properties[J].Food Hydrocolloids, 2020, 101: 105490.DOI:10.1016/j.foodhyd.2019.105490.
[28] CHEN W P, LIANG G J, LI X, et al.Impact of soy proteins,hydrolysates and monoglycerides at the oil/water interface in emulsions on interfacial properties and emulsion stability[J].Colloids and Surfaces B: Biointerfaces, 2019, 177: 550-558.DOI:10.1016/j.colsurfb.2019.02.020.
[29] ZHU L J, XU Q Y, LIU X Y, et al.Oil-water interfacial behavior of soy β-conglycinin-soyasaponin mixtures and their effect on emulsion stability[J].Food Hydrocolloids, 2020, 101: 105531.DOI:10.1016/j.foodhyd.2019.105531.
[30] 张小影, 齐宝坤, 孙禹凡, 等.盐离子对大豆-乳清混合蛋白乳液的稳定性及界面特性的影响[J].食品工业科技, 2021, 42(6): 22-28.DOI:10.13386/j.issn1002-0306.2020060098.
[31] PEREZ A A, CARRARA C R, SÁNCHEZ C C, et al.Interfacial dynamic properties of whey protein concentrate/polysaccharide mixtures at neutral pH[J].Food Hydrocolloids, 2009, 23(5): 1253-1262.DOI:10.1016/j.foodhyd.2008.08.013.