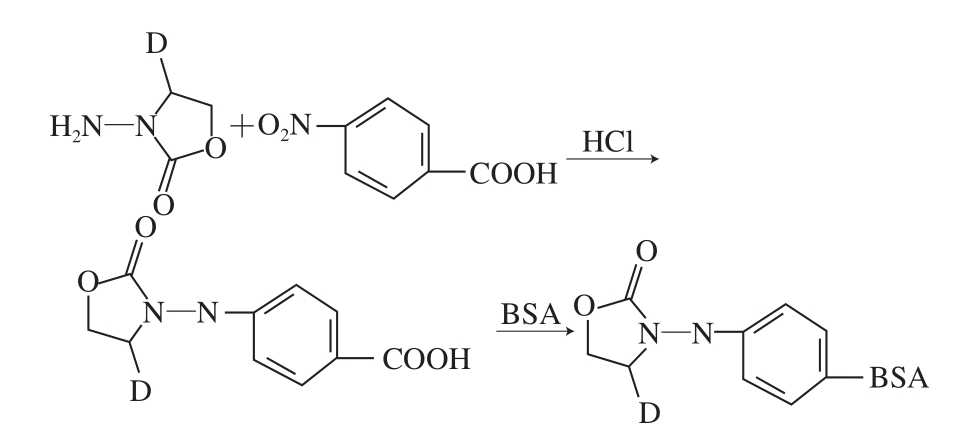
图1 AOZ抗原合成路线图
Fig. 1 Synthetic route of AOZ antigen
硝基呋喃类抗生素作为一类由人工合成、具有5-硝基特定结构的广谱抗菌类药物,被广泛应用在畜禽胃肠道疾病的治疗[1],或者作为饲料添加剂使用。硝基呋喃类抗生素主要包括呋喃唑酮(Furazolidone)、呋喃西林(Nitrofurazone)、呋喃它酮(Furaltadone)及呋喃妥因(Nitrofurantoin)等,此类药物也是一类具有潜在致癌性和能够诱导突变的物质[2]。欧盟于1995年发布了一项关于禁止使用呋喃类抗菌物质的指令,规定不得在动物源性食品中检出呋喃类物质。我国农业部第235号公告[3]中列出的禁止使用药物清单中包括呋喃它酮和呋喃唑酮,且规定在动物性食品中不得检出。硝基呋喃类药物在机体内代谢速度很快且半衰期短、仅持续数小时的特点,造成了检测机体内硝基呋喃类药物相当困难。呋喃唑酮的代谢物为3-氨基-2-恶唑烷酮(3-amino-2-oxazolidinone,AOZ),呋喃它酮的代谢物为5-甲基吗啉-3-氨基-2-唑烷基酮(5-morpholine-methyl-3-amino-2-oxazolidinone,AMOZ),呋喃妥因的代谢物为1-氨基-2-乙内酰(1-aminohydantoin,AHD),呋喃西林的代谢物为氨基脲(semicarbazid,SEM),以上代谢产物能够与机体的组织蛋白质反应,形成稳定的蛋白质结合物,在机体内残留很长时间,其代谢物则通过水解反应从蛋白质中游离出来。因此,硝基呋喃类药物的真实残留状况由检测得到的其代谢物的含量来体现。同时,检测硝基呋喃类药物的代谢产物对硝基呋喃类药物的残留起到监控作用。目前,欧盟对硝基呋喃类代谢物的检测方法灵敏度做出了规定,要求检测方法灵敏度为1 μg/kg。我国目前采用国家标准GB/T 21311—2007《动物源性食品中硝基呋喃类药物代谢物残留量检测方法 高效液相色谱/串联质谱法》[4],此方法的SEM、AOZ、AMOZ和AHD检出限(limits of detection,LOD)均为0.5 μg/kg。
硝基呋喃类代谢物残留的检测方法多种多样,仪器法主要有高效液相色谱(high performance liquid chromatography,HPLC)法[5-6]、液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LCMS/MS)法[7-9]、液相色谱-质谱(liquid chromatographymass spectrometry,LC-MS)法和分光光度法,免疫法主要有酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)法[10-11]、免疫层析技术等。仪器法的优点是自动化程度高、精确度高、假阳性率低,缺点是价格昂贵、成本高、操作繁琐、样品处理复杂、需要专业分析人员。ELISA法虽然具有快速、简便、灵敏、高特异性的特点,但其缺点是易出现假阳性结果。近年来,免疫层析技术成为热门检测技术,主要包括以胶体金、荧光、磁珠为基础的免疫层析技术,研究比较多的是胶体金免疫层析技术,以胶体金为示踪物标记抗原或抗体,用于半定量或定性检测,此方法灵敏度不高,在针对心血管标志物、肿标等对灵敏度有高要求的领域受限。柳爱春等[12]研制的4 种硝基呋喃代谢物快速胶体金检测试纸条的LOD分别为AOZ 0.5 μg/kg、SEM 1.0 μg/kg、AMOZ 1.0 μg/kg、AHD 2.0 μg/kg,肉眼观察结果只能做到半定量检测。免疫磁珠层析技术以磁性微球与抗原或抗体特异性结合,靠外界磁场产生定向移动,通过检测磁信号代替光信号,优点是敏感性高,缺点是价格昂贵、技术复杂、工艺实施难度高,目前尚无研究报道将此项技术应用到硝基呋喃类代谢物的检测中。荧光免疫层析技术又分为量子点(quantum dots,QDs)层析技术和上传发光技术。上传发光技术以镧系元素掺杂入陶瓷颗粒,构成上转化颗粒(upconversion particle,UCP),作为标记物实现免疫层析,优点是安全、稳定、灵敏,缺点是价格昂贵、工艺要求高。袁建等[13]利用铕(Ⅲ)元素的纳米粒子标记抗体建立快速检测4 种硝基呋喃代谢物的免疫层析法,此方法用肉眼观察只能达到半定量检测,4 种代谢物的LOD分别为CPSEM(CP(羧基苯甲醛)与SEM的衍生物))0.5 ng/g、CPAMOZ(CP与AMOZ的衍生物))0.5 ng/g、CPAHD(CP与AHD的衍生物)0.1 ng/g、CPAOZ(CP与AOZ的衍生物)0.5 ng/g,同时该免疫层析法是试纸条和微量滴定孔组合的形式,在加样时比较繁琐,需要人工吸取4 种铕(Eu)纳米球标记抗体及待检样品,一起加入到微量滴定孔进行反应,很容易造成人为误差,且操作繁琐、重复性差。量子点荧光层析技术以主族Ⅱ~Ⅵ(如CdSe)、Ⅲ~Ⅴ(InAs、GaSe、InP)元素构成荧光探针标记物,通过能量跃迁可以发出多种不同颜色的光,很适合作为多组分检测的标记物,再加上准确性好、灵敏度高、检测时间短、成本低,被广泛用于食品、医药、兽药等行业,成为热门研究方向[14]。
本研究以量子点荧光免疫层析技术为基础,建立4 种硝基呋喃代谢物残留的复合荧光免疫分析技术,通过性能测试对试纸条进行全面评价,对该多元荧光免疫层析检测技术在兽药残留领域的广泛应用具有重要意义。
BALB/c小鼠购自河北医科大学。
AOZ、AMOZ、1-氨基-乙内酰脲盐酸盐(1-aminohydantoin hydrochloride,AHD·HCl)、盐酸氨基脲(semicarbazide hydrochloride,SEM·HCl)(纯度≥99.0%)、牛血清白蛋白(bovine serum albumin,BSA) 美国Sigma公司;量子点荧光微球美国Ocean NanoTech公司;N,N-二甲基甲酰胺(N,N-dimethylformamide,DMF)、无水甲醇 天津永大化学试剂有限公司;邻醛基苯甲酸(2-carboxybenzaldehyde,2-CBA)、对醛基苯甲酸(4-carboxybenzaldehyde,4-CBA) 阿拉丁试剂(上海)有限公司;N-羟基琥珀酰亚胺(N-hydroxysuccinimide,NHS) 南京化学试剂股份有限公司;1-乙基-3-(3-二甲氨基丙基)碳二亚胺盐酸盐(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride,EDC) 上海思域化工科技有限公司。
RF-6000荧光分光光度计 日本岛津公司、NanoDrop 2000紫外扫描仪、Micro17超速离心机 美国Thermo公司;CR-GIII高速离心机 日本Hitachi公司;MiLLi-QingegraLLo超纯水系统 德国密理博公司;JA3003电子精密天平 上海衡平仪器仪表厂;T-Meter I荧光免疫分析仪 河北特温特生物科技发展有限公司。
1.3.1 免疫抗原的制备
半抗原的合成[15]:以CPAOZ为例,合成半抗原。将0.4 g 4-CBA用2 mL纯水溶解,缓缓加DMF至上述溶液,边滴加边搅拌,直至4-CBA完全溶解;称取0.5 g AOZ缓慢倾入上述反应液中,室温反应5 h,3 000 r/min离心,保留沉淀弃上清液,沉淀为淡黄色,再加入0.01 mol/L PBS重悬沉淀,洗涤3 次,50 ℃烘干,得半抗原CPAOZ。同理,用AMOZ、AHD·HCl和SEM·HCl置换上述步骤中的AOZ,即可得到半抗原CPAMOZ、CPAHD和CPSEM。
免疫抗原的合成[16]:称取24 mg的CPAOZ,用2 mL DMF溶解,缓慢加入溶有18 mg NHS的PBS缓冲液,充分搅拌,反应5 min;缓慢加入溶有40 mg EDC的PBS缓冲液,室温搅拌2 h;称取60 mg BSA溶于2 mL PBS中,然后将上述反应溶液缓慢加入,4 ℃搅拌反应过夜;0.01 mol/L PBS透析3 d,-20 ℃保存备用。AOZ抗原合成路线图如图1所示。检测原同法制备。

图1 AOZ抗原合成路线图
Fig. 1 Synthetic route of AOZ antigen
1.3.2 量子点荧光微球(quantum dot submicrobeads,QBs)标记抗体
采用EDC-NHS一步法[17]将QBs分别与4 种硝基呋喃类代谢物偶联[18]:将1 mg QBs用5 mL磷酸(PB)缓冲液(含0.5% 吐温-20、0.01 mol/L、pH值为6.0)进行悬浮,10 000 r/min离心30 min,收集沉淀;沉淀用5 mL PB缓冲液溶解后,加入1.0 μg EDC和0.8 μg NHS,混匀后避光反应1 h,将100 μg抗体加入到混合液中,混合搅拌3 h,再加入0.1 mL 0.3 mol/L的甘氨酸封闭2 h,10 000 r/min离心30 min,收集沉淀;沉淀用750 μL复溶液(含5%蔗糖、5% BSA、2% 吐温-20和1% ProClin的PB缓冲液)复溶,4 ℃保存备用。
1.3.3 QBs标记抗体偶联物的表征
通过荧光分光光度计测定QBs(8 pmol/L)[19],光电倍增管电压为700 V,响应时间为0.5 s,激发波长为350 nm,发射起始波长为500~650 nm,发射狭缝与激发狭缝均为5 nm,扫描速率为240 nm/min。
1.3.4 偶联pH值的优化
在1.3.2节QBs标记抗体过程中,分别选用pH值为5.5、6.0、6.5、7.0、7.5的0.01 mol/L PB缓冲液[20]。用标记好的抗体测试试纸条,检测不同标记pH值条件下的荧光强度变化,每个pH值重复检测5 次,确定最佳标记pH值。
1.3.5 饱和标记量的优化
在1.3.2节QBs标记抗体过程中,保持QBs的量不变,分别加入25、50、100、125、150、200、300 μg的抗体进行偶联,测定方法同1.3.4节,结果采用Sigmaplot软件绘制曲线图,横坐标为抗体饱和标记量,纵坐标为T线荧光强度,确定最佳饱和标记量。
1.3.6 试纸条的组成
QBs荧光免疫层析试纸条的组成如图2所示,其中QBs探针包被在结合垫上[21-22],AOZ抗原、AMOZ抗原、AHD抗原和SEM抗原分别作为T线,羊抗兔二抗作为C线,依次喷涂在NC膜上。
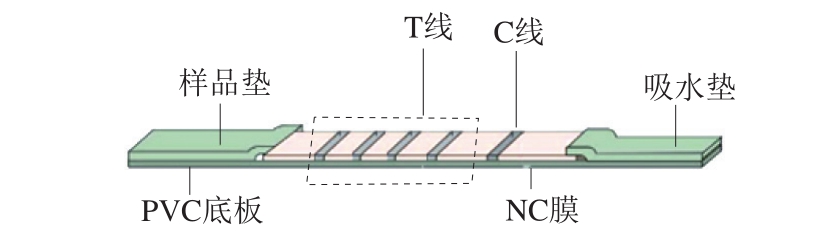
图2 荧光免疫层析试纸条示意图
Fig. 2 Schematic illustration of the fluorescent immunochromatographic test strip
1.3.7 样品预处理
1)衍生[23]:称取5.0 g鱼肉样品,加入10 mL HCl溶液(1 mol/L),进行均质处理后放入50 mL离心管中,加入500 μL邻硝基苯甲醛溶液(30 mmol/L),50 ℃混匀反应60 min;
2)萃取[24]:将上述反应溶液用1 mol/L的NaOH调至pH 7.0,加入10 mL乙酸乙酯,涡旋萃取1 min,8 000 r/min离心20 min,留取乙酸乙酯层,60 ℃氮气吹干;用1 mL正己烷复溶,加入1 mL 0.1 mol/L的PBS缓冲液进行萃取,8 000 r/min离心20 min,留取缓冲液层用于检测。
1.3.8 试纸条性能测试
1.3.8.1 标准曲线的制作及检测限测定
分别制备4 种硝基呋喃代谢物的系列标准溶液,以AOZ为例,将1 mg/mL的AOZ母液稀释成系列标准溶液(质量浓度分别为0、0.10、0.25、0.50、1.00、2.00、5.00 μg/L),进行QBs荧光免疫层析试纸条测试,每个质量浓度测定5 个平行,用干式荧光分析仪进行检测,并读取数值。设定质量浓度为0 μg/L时的标准溶液FIT/FIC比值为B0,其他加标质量浓度的FIT/FIC比值为B,以B/B0×100为纵坐标,质量浓度为横坐标作图,绘制竞争抑制曲线,确定定量范围、抑制率半抑制质量浓度(half maximal inhibitory concentration,IC50)及检测限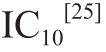 。
。
1.3.8.2 准确度和精密度实验
通过鱼肉样本添加回收实验检测QBs荧光免疫层析试纸条的准确度和精密度[26-28],在空白鱼肉组织中添加0.5、2.0、4.0 μg/L 3 个质量浓度的4 种硝基呋喃代谢物,按照1.3.7节的方法进行样品预处理,每个质量浓度重复测定5 次,共测定3 个批次,计算加标回收率、批内变异系数和批间变异系数。
1.3.8.3 特异性实验
分别测试其中1 种硝基呋喃代谢物与其他3 种代谢物的交叉反应性,将4 种硝基呋喃代谢物分别配制成0.5、10.0、100.0 μg/L的标准溶液,用荧光免疫层析试纸条进行测试,用干式荧光分析仪进行结果判读。
1.3.8.4 与LC-MS/MS法的对比实验
为验证本研究中量子点复合荧光免疫层析试纸条在鱼肉样本检测中的可用性,对来自石家庄市兽药监察所的5 份已知样品分别用自制试纸条和GB/T 21311—2007中描述的LC-MS/MS法(样品前处理和检测方法)进行检测。
采用SPSS统计软件进行数据处理,Origin制图软件绘制标准曲线。
由图3可知,BSA的最大吸收峰在280 nm波长处,CPAOZ的最大吸收峰在330 nm波长处,BSA和CPAOZ偶联后,在波长280 nm和330 nm处均叠加出现吸收峰,表明偶联成功。根据朗伯-比尔定律,计算出CPAOZ-BSA的分子结合比为15∶1。同理,CPSEM-BSA、CPAHDBSA和CPAMOZ-BSA的紫外扫描图如图4~6所示,均表明偶联成功,CPSEM-BSA分子结合比为13.5∶1、CPAHD-BSA分子结合比为19.7∶1、CPAMOZ-BSA分子结合比为19.6∶1。
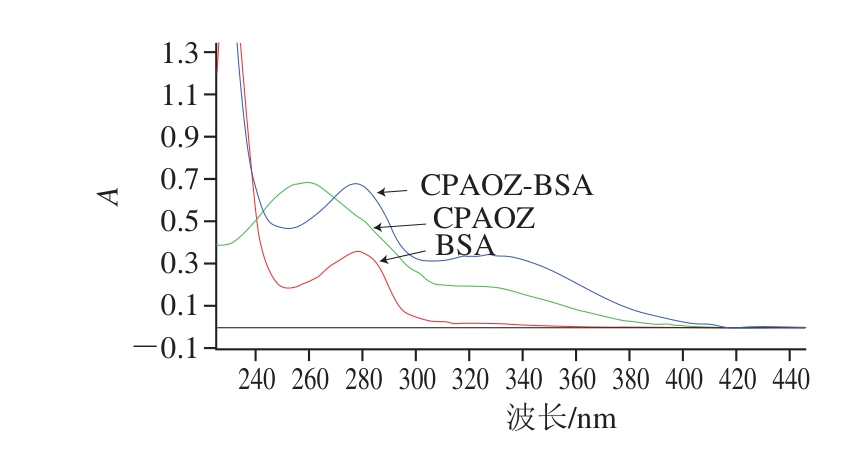
图3 CPAOZ-BSA紫外扫描图
Fig. 3 Ultraviolet (UV) absorption spectrum of CPAOZ-BSA
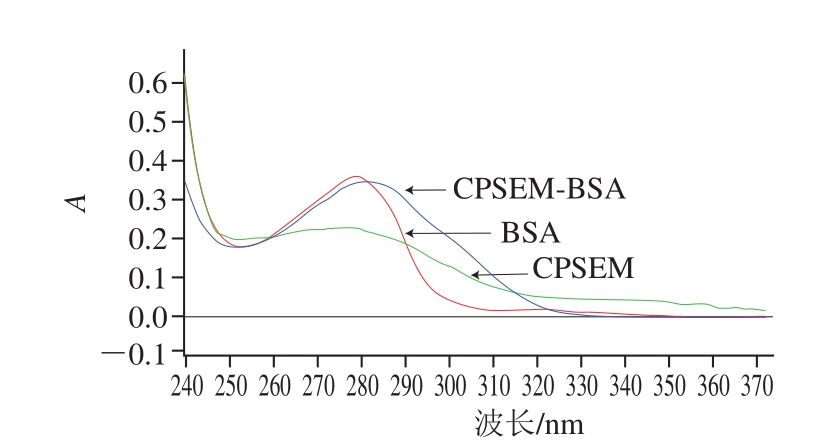
图4 CPSEM-BSA紫外扫描图
Fig. 4 UV absorption spectrum of CPSEM-BSA
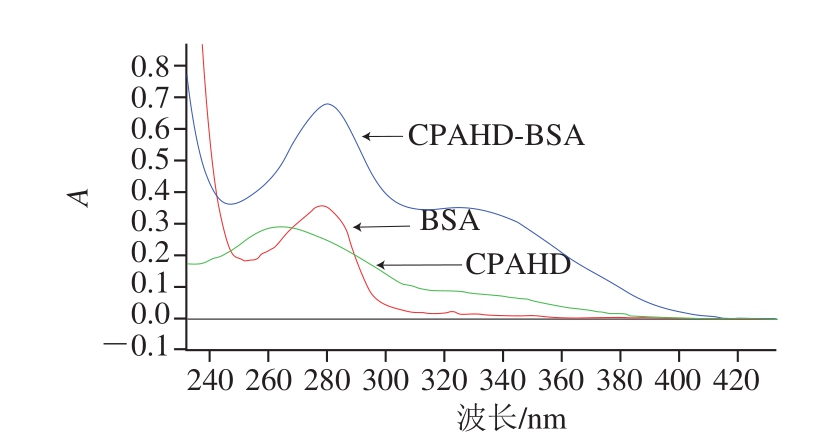
图5 CPAHD-BSA紫外扫描图
Fig. 5 UV absorption spectrum of CPAHD-BSA
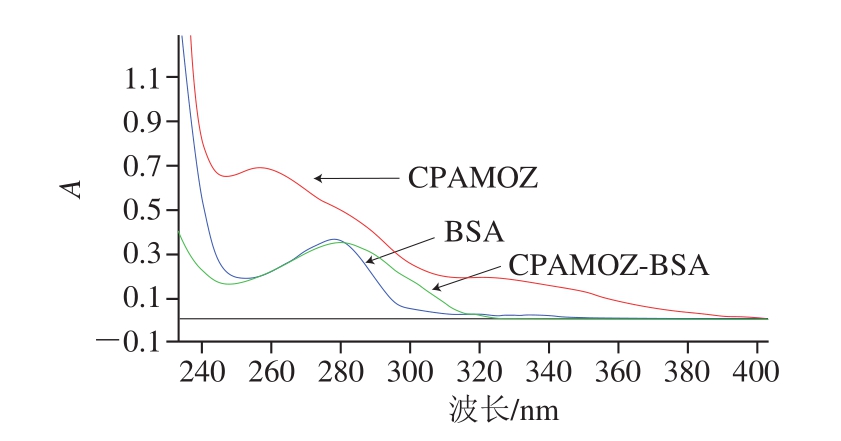
图6 CPAMOZ-BSA紫外扫描图
Fig. 6 UV absorption spectrum of CPAMOZ-BSA
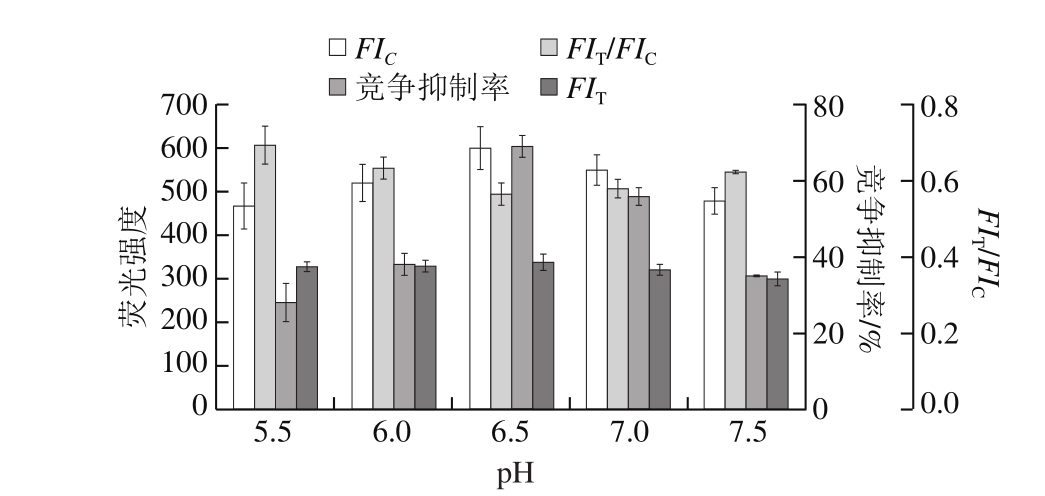
图7 pH值对试纸条的影响
Fig. 7 Effect of pH value on the test srip
pH值会影响偶联过程中抗体的生物活性,通过评价pH值对荧光免疫层析试纸条检测FIT、FIC、FIT/FIC值和竞争抑制率的影响,确定最佳偶联pH值[29]。由图7可知,pH值对荧光免疫层析试纸条的FIT/FIC值影响不大,但是对FIT、FIC和竞争抑制率有较大影响。当pH值为6.5时,试纸条C线、T线荧光强度最高,且竞争抑制率最好,达69%。因此,选择pH值为6.5的缓冲液作为偶联缓冲液。
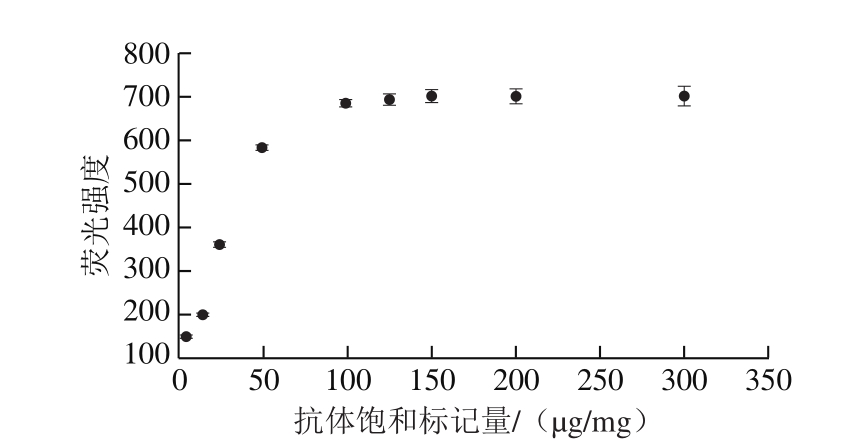
图8 抗体饱和标记量的优化
Fig. 8 Optimization of saturated labeling amount of antibody
将1 mg QBs与不同量的抗体进行偶联,检测阴性样本试纸条T线的荧光强度变化[30]。由图8可知,T线的荧光强度随抗体饱和标记量的增加而增强,在100 μg时强度趋于稳定。因此确定100 μg/mg是最佳抗体饱和标记量。
2.4.1 标准曲线的建立
为了减少基质效应,本研究采用鱼肉组织阴性样本添加系列标准品,绘制QBs荧光免疫层析试纸条定量标准曲线。得到CPAOZ的线性范围为0.1~5.0 μg/L,线性方程为y=1.783 1x+2.115 1(R²=0.997 7),IC50为1.54 μg/L,IC10为0.4 μg/L;CPAHD的线性范围为0.1~5.0 μg/L,线性方程为y=1.675 0x+1.968 8(R2=0.994 7),IC50为1.4 μg/L,IC10为0.4 μg/L;CPSEM的线性范围为0.1~5.0 μg/L,线性方程为y=1.906 6x+2.323 6(R²=0.996 1),IC50为1.75 μg/L,IC10为0.5 μg/L;CPAMOZ的线性范围为0.1~5.0 μg/L,线性方程为y=1.995 9x+2.442 1(R²=0.998 0),IC50为1.87 μg/L,IC10为0.5 μg/L。通过计算IC10得出的AOZ、AHD、SEM和AMOZ的方法检出限分别为0.4、0.4、0.5、0.5 μg/L。
2.4.2 准确度及精密度
表1 准确度及精密度测定结果
Table 1 Results of accuracy and precision test

添加物 添加量/(μg/L)批内 批间±s 回收率/% 变异系数/%±s 回收率/% 变异系数/%AOZ 0.5 0.42±0.02 84.2 4.75 0.43±0.04 86.8 9.22 2.0 1.83±0.16 91.5 8.74 1.79±0.14 89.5 7.82 4.0 3.89±0.29 97.3 7.46 3.74±0.18 93.5 4.81 AHD 0.5 0.41±0.04 81.2 9.85 0.44±0.04 88.4 9.05 2.0 1.86±0.18 93.2 9.68 1.91±0.11 95.5 5.76 4.0 3.59±0.22 89.7 6.13 3.59±0.21 89.8 5.85 SEM 0.5 0.42±0.03 83.4 7.19 0.40±0.03 80.4 7.46 2.0 1.89±0.16 94.5 8.47 1.85±0.14 92.5 7.57 4.0 3.87±0.23 96.7 5.94 3.68±0.23 92.0 6.25 AMOZ 0.5 0.41±0.03 82.4 7.28 0.41±0.03 82.4 7.28 2.0 2.03±0.13 101.5 6.40 1.80±0.18 90.0 10.00 4.0 3.75±0.19 93.7 5.07 3.75±0.24 93.8 6.40
通过加标回收实验对批内和批间重复性和准确度进行评价。由表1可知,该QBs荧光免疫层析试纸条的批内检测回收率为80%~110%,批内变异系数在15%以内,批间回收率为80%~100%,批间变异系数在15%以内,表明该试纸条具有较好的精密度和准确度,符合《食品中兽药残留检测指南》规定的兽药残留检测方法的回收率为80%~120%、变异系数在15%以内的要求。
2.4.3 特异性
用QBs荧光免疫层析试纸条分别测试4 种代谢物的系列标准溶液,结果表明,某1 种硝基呋喃代谢物对其他代谢物的测试未出现阳性结果,4 种硝基呋喃代谢物AOZ、AHD、SEM和AMOZ之间的交叉反应率小于0.1%,表明试纸条具有较好的特异性[31-32]。
2.4.4 与LC-MS/MS法的比较结果
表2 QBs荧光免疫层析试纸条与LC-MS/MS法的检测结果对比
Table 2 Comparison of results of QB-ICA and LC-MS/MS for the determination of nitrofuran metabolites

注:N. 阴性。
药物名称 方法 样品测定结果/(μg/L)1 2 3 4 5 AOZ LC-MS/MS N 5.67±0.47 6.47±0.51 2.35±0.06 N试纸条 N 5.59±0.45 6.96±0.38 2.08±0.12 N AHD LC-MS/MS N 3.46±0.32 4.39±0.34 0.98±0.14 N试纸条 N 3.24±0.36 4.35±0.53 1.06±0.18 N SEM LC-MS/MS N 3.74±0.29 5.42±0.41 0.73±0.06 N试纸条 N 3.59±0.12 5.39±0.44 0.64±0.05 N AMOZ LC-MS/MS N 4.34±0.29 7.88±0.21 1.23±0.11 N试纸条 N 4.39±0.29 7.67±0.27 1.27±0.08 N
为验证试纸条能够满足实际样品检测的要求,将其与GB/T 21311—2007中描述的LC-MS/MS仪器法进行对比。由表2可知,QBs荧光免疫层析试纸条与LC-MS/MS法的检测结果有很好的相关性,2 种方法均检出2 份阴性样本,分别为样品1和样品5,检出3 份阳性样本,分别为样品2~4,2 次重复测定结果一致。上述结果证明,自制的QBs荧光免疫层析试纸条可以满足实际样品的检测要求。
免疫层析技术由于其检测周期短、成本低、配套仪器简单,已经在食品安全、兽药残留、生物医药等行业广泛应用,但其检测灵敏度相对于仪器法(电化学传感、色谱技术、微阵列技术)较低。目前,主要研究从以下几个方面提高方法的灵敏度:1)选用高特异、高亲和性的抗体,在处理过程中采取适当的保护措施,减少生物活性的损失,从而提高方法自身的检测灵敏度;2)改进层析的方法,去掉结合垫,处理样品垫,使其具有良好的稳定性和释放性,同时可以增加待检样本与标记抗体在液相中的反应时间,使反应更充分,提高竞争效率,从而提高方法的检测灵敏度;3)选用新型可替代、超灵敏的标记物,目前大众所熟知的标记物质有胶体金颗粒、彩色乳胶微球,近年新发展起来的量子点、量子点微球,由于其独特的光学特性及高强度的发射光谱特性,逐渐作为新标记物被应用。QBs是将量子点荧光染料通过包埋或吸附的方式固定在高聚物载体上,在高聚物载体的壳结构下性质稳定,不易发生聚沉和猝灭。Xiang等[33]构建载体包埋量子点染料,形成荧光微球,并成功利用电化学方法对尿道病原菌进行了检测,其研制的量子点荧光微球的检测灵敏度比市售的商业化标记物高出10多倍。
多元检测体系是研究者为了提高检测效率,节约成本,而将多种物质在同一试纸条上进行检测,且相互之间互不干扰,对多种待测物含量相关性的研究意义深远。Song Suquan等[34]实现了在同一胶体金试纸条上同时检测玉米中的呕吐毒素、玉米赤霉烯酮和黄曲霉毒素B1,肉眼观察到的LOD分别为1、50、60 μg/kg,仪器读取的LOD为0.05、1.00、3.00 μg/kg。李丹妮等[35]制备的荧光免疫层析定量试纸条同时检测克伦特罗、莱克多巴胺和沙丁胺醇3 种瘦肉精物质的LOD分别可达0.2、0.4、0.5 μg/L,且与其他同类药物交叉反应率很低,具有良好的特异性。
通过EDC-NHS一步法将QBs分别与AOZ、AHD、SEM和AMOZ偶联,得到相应的QBs探针,在此基础上结合多元检测体系和QBs荧光免疫检测层析技术,制备硝基呋喃代谢物复合荧光免疫层析试纸条。通过绘制标准曲线,得出AOZ、AHD、SEM和AMOZ的LOD分别为0.4、0.4、0.5、0.5 μg/L;通过加标回收实验对批内和批间的重复性和准确度进行评价,得出试纸条的批内检测回收率为80%~110%,批内变异系数在15%以内,批间回收率为80%~100%,批间变异系数在15%以内;且4 种硝基呋喃代谢物AOZ、AHD、SEM和AMOZ之间的交叉反应率小于0.1%。
[1] 李军, 张会彩, 刘聚祥, 等. 酶联免疫吸附检测动物饲料中呋喃唑酮[J]. 中国兽医杂志, 2009, 45(8): 85-87. DOI:10.3969/j.issn.0529-6005.2009.08.034.
[2] 蒋宏伟. 酶联免疫技术在动物产品中硝基呋喃类药物残留检测的应用[J]. 陕西农业科学, 2006(5): 53-55.
[3] 农业部. 中华人民共和国农业部公告第235号[EB/OL]. (2002-10-24)[2019-03-20]. https://www.docin.com/p-1666487561.html.
[4] 中华人民共和国质量监督检验检疫总局, 中国国家标准化管理委员会. 动物源性食品中硝基呋喃药物代谢物残留检测方法 高效液相色谱/串联质谱法: GB/T 21311—2007[S]. 北京: 中国标准出版社, 2007.
[5] 于慧娟, 蔡友琼, 毕士川, 等. 高效液相色谱法测定水产品中呋喃唑酮的残留量[J]. 色谱, 2005, 23(1): 114-117. DOI:10.3321/j.issn:1000-8713.2005.01.031.
[6] 农业部. 中华人民共和国农业部1077号公告-2-2008[EB/OL]. (2008-8-11)[2019-03-20]. http://bbs.foodmate.net/thread-301120-1-902.html.
[7] 彭涛, 邱月明, 李淑娟, 等. 高效液相色谱-串联质谱法测定动物肌肉中硝基呋喃类抗生素代谢物[J]. 检验检疫科学, 2003, 13(6): 23-28.DOI:10.3969/j.issn.1674-5354.2003.06.007.
[8] 王丽娜, 刘凯, 杜柏林, 等. UPLC/MS/MS测定动物尿液中9 种β-受体激动剂残留量[J]. 现代畜牧兽医, 2013(8): 42-46. DOI:10.3969/j.issn.1672-9692.2013.08.018.
[9] 农业部. 中华人民共和国农业部781号公告-4-2006[EB/OL]. (2006-12-16)[2019-03-20]. http://down.foodmate.net/standard/sort/3/17156.html.
[10] 宋丽丽, 张晓辉, 张海琪, 等. 酶联免疫法快速测定水产品中呋喃唑酮、呋喃它酮代谢物[J]. 浙江农业学报, 2008, 20(4): 296-299.
[11] 农业部. 中华人民共和国农业部1025号公告-17-2008[EB/OL].(2008-04-29) [2019-03-20]. http://down.foodmate.net/standard/sort/9/19354.html.
[12] 柳爱春, 刘超, 桑丽雅, 等. 硝基呋喃类代谢物抗原合成及在胶体金试纸条上的应用[J]. 现代农业科技, 2012(23): 265-267.DOI:10.3969/j.issn.1007-5739.2012.23.171.
[13] 袁建, 董雪, 邢常瑞, 等. 一种快速检测四种硝基呋喃代谢物的免疫层析法: 中国, CN 109239328 A[P]. 2019-01-18.
[14] 祝伟霞, 刘亚风, 梁伟, 等. 动物性食品中硝基呋喃类药物残留检测研究进展[J]. 动物医学进展, 2010, 31(2): 99-102. DOI:10.3969/j.issn.1007-5038.2010.02.023.
[15] 赵亦静, 傅小伟, 张明洲, 等. 呋喃西林免疫抗原的合成与鉴定[J]. 现代农业科技, 2008(14): 197-199. DOI:10.3969/j.issn.1007-5739.2008.14.151.
[16] 任海涛, 沈玉栋, 徐振林, 等. 呋喃唑酮代谢物单克隆抗体制备及酶联免疫吸附分析方法[J]. 分析化学, 2012, 40(5): 745-751.DOI:10.3724/SP.J.1096.2012.10409.
[17] 丁桥棋, 李丽, 范文韬, 等. 基于新型量子点荧光微球的氯霉素免疫层析试纸条的制备和应用[J]. 分析化学研究报告, 2017, 45(11):1686-1693. DOI:10.11895/j.issn.0253-3820.170300.
[18] 解泉源, 赖卫华, 刘春梅, 等. 大肠杆菌O157:H7荧光微球免疫层析试纸条的研制[J]. 食品科学, 2013, 34(16): 353-357. DOI:10.7506/spkx1002-6630-201316072.
[19] 唐海波, 齐维, 唐诗幸, 等. 荧光定量快速检测鲜奶中四环素总量残留[J]. 现代食品科技, 2012, 28(11): 1600-1602.
[20] 郭诗静, 唐海波, 齐维, 等. 免疫荧光层析法快速检测猪尿中克伦特罗含量[J]. 现代食品科技, 2013, 29(5): 1154-1156.
[21] 方琦, 黄锡荣, 李凯, 等. 降钙素原荧光免疫层析定量检测方法的建立及性能评估[J]. 中华检验医学杂志, 2012, 35(12): 1102-1107.DOI:10.3760/cma.j.issn.1009-9158.2012.12.011.
[22] 李军, 刘莲娜, 孟晓璐, 等. 硝基呋喃类药物胶体金免疫层析试纸条的研制[J]. 畜牧与兽医, 2014, 4(1): 74-77.
[23] 李春生, 刘静静, 杜顺丰, 等. 呋喃唑酮代谢物单克隆抗体和胶体金免疫层析试纸条的研制[J]. 现代食品科技, 2017, 43(3): 326-331.DOI:10.13982/j.mfst.1673-9078.2017.6.048.
[24] 葛怀礼, 王莲, 李金卿, 等. 盐酸克伦特罗荧光定量检测试剂盒质量评价[J]. 中国畜牧兽医, 2014, 41(10): 285-289.
[25] 郭艳宏, 李飞, 邹明强, 等. 用于检测氯霉素类残留物的荧光免疫检测试纸条的研制[J]. 化学试剂, 2010, 32(6): 496-498. DOI:10.3969/j.issn.0258-3283.2010.06.005.
[26] 范放, 朱海, 洪小柳, 等. 氯霉素荧光纳米颗粒免疫层析法的建立[J].现代农业科学, 2009, 16(9): 13-14.
[27] 段宏, 陈雪岚, 江湖, 等. 量子点荧光微球免疫层析试纸条定量检测恶性恶性疟原虫[J]. 分析化学, 2015, 43(3): 338-343. DOI:10.11895i ssn.0253-3820.140848.
[28] ZHANG Mingxia, LI Cun, WU Yinliang. Determination of phenylethanolamine A in animal hair, tissues and feeds by reversed phase liquid chromatography tandem mass spectrometry with QuEChERS[J]. Journal of Chromatogrephy B, 2012, 900: 94-99.DOI:10.1016/j.jchromb.2012.05.030.
[29] 胡佳丽, 于东升, 刘小雷, 等. 荧光免疫层析法快速测定牛奶中头孢氨苄残留量[J]. 中国食品卫生杂志, 2014, 26(4): 362-366.DOI:10.13590/j.cjfh.2014.04.015.
[30] 胡华军, 付涛, 张明洲, 等. CdTe/ZnSe壳核量子点免疫层析试纸条检测科伦特伦的研究[J]. 分析化学, 2010, 38(12): 1727-1731.DOI:10.3724/SP.J.1096.2010.01727.
[31] 何方洋, 冯才伟, 孙震, 等. 饲料中硝基呋喃类药物免疫胶体金检测试纸条的研制[J]. 饲料工业, 2012, 33(23): 35-38.
[32] 赵正苗, 罗晓琴, 汪善良, 等. 应用胶体金免疫层析法检测动物组织中呋喃西林代谢物的残留[J]. 上海畜牧兽医通讯, 2012, 5: 4-5.
[33] XIANG Y, ZHANG H X, JIANG B Y, et al.Quantum dot layer-bylayer assemblies as signal amplification labels for ultrasensitive electronic detection of uropathogens[J]. Analytical Chemistry, 2011,83(11): 4302-4306.
[34] SONG Suquan, LIU Na, ZHAO Zhiyong, et al. Multiplex lateral flow immunoassay for mycotoxin determination[J]. Analytical Chemistry,2014, 86(10): 4995-5001.
[35] 李丹妮, 黄华, 张倩, 等. 3 种β-受体激动剂荧光免疫层析试纸条的制备及特性研究[J]. 中国畜牧兽医, 2017, 44(8): 2437-2442.DOI:10.16431/j.cnki.1671-7236.2017.08.031.
Preparation of a Fluorescent Immunochromatographic Strip for Simultaneous Detection of Four Nitrofuran Metabolites
郭会灿. 4 种硝基呋喃代谢物复合荧光免疫层析试纸条的制备[J]. 肉类研究, 2019, 33(4): 29-35. DOI:10.7506/rlyj1001-8123-20190322-065. http://www.rlyj.net.cn
GUO Huican. Preparation of a fluorescent immunochromatographic strip for simultaneous detection of four nitrofuran metabolites[J]. Meat Research, 2019, 33(4): 29-35. DOI:10.7506/rlyj1001-8123-20190322-065. http://www.rlyj.net.cn