
图 1 骨骼肌肌内结缔组织中Ⅴ型胶原蛋白SDS-PAGE图
Fig. 1 SDS-PAGE pattern of type V collagen from intramuscular connective tissues in skeleton muscles
家畜肌肉硬度有固有硬度和尸僵硬度,其中固有硬度主要来自于骨骼肌肌内结缔组织(intramuscular connective tissue,IMCT)的胶原蛋白[1]。不同品种、甚至同一品种不同年龄阶段的家畜肌肉组织中胶原蛋白的含量、热稳定性、胶原蛋白分子内和分子间的交联程度等均有很大差距。IMCT的热稳定性和机械稳定性随动物的生长而增加,这与胶原蛋白分子间共价交联的化学性质和胶原蛋白的氨基酸组成有关[2]。在幼龄动物的结缔组织中,大多数交联以不稳定的席夫碱形式存在,对酸和热不稳定,容易受到胶原蛋白酶和离子强度的变化及温度的作用而降解[3]。随着动物的生长,可还原交联被转化为更稳定的非还原交联,结缔组织对酸和热的敏感性降低,加热后的胶原蛋白可溶性下降,降低了肌肉的嫩度[4]。研究发现,骨骼肌IMCT中主要有Ⅰ、Ⅲ、Ⅳ、Ⅴ型胶原蛋白,其中含量较多的是Ⅰ、Ⅲ型胶原蛋白[5],因此对于不同品种骨骼肌中Ⅰ、Ⅲ型胶原蛋白的研究较多[6-7],但对于含量较少、提取过程较为复杂的Ⅴ型胶原蛋白特性的研究报道较少。Ⅴ型胶原蛋白和Ⅰ、Ⅲ型胶原蛋白均属于纤维状胶原蛋白,纤维状胶原蛋白的共同结构特征是中心有一个长的胶原结构域,含有1 000多个氨基酸,由Gly-Xaa-Yaa重复序列组成,其中Xaa和Yaa位置是任一种氨基酸(或亚氨基酸)残基[8]。当Xaa位和Yaa位均为亚氨基酸时(Gly-Pro-Pro、Gly-Pro-Hyp),胶原蛋白的热稳定性最高[9]。分析胶原蛋白氨基酸组成发现,甘氨酸含量最高,其含量随着来源的不同在28.6%~35.6%之间变化,不含色氨酸,亚氨基酸(脯氨酸和羟脯氨酸)含量较高,羟脯氨酸含量是衡量胶原蛋白热稳定性的重要指标,其含量越高,胶原蛋白的热稳定性越高[10]。本研究采用放牧饲养的不同月龄(6、9、12、18 月)的乌珠穆沁羊,提取半腱肌(Semitendinosus,ST)和背最长肌(Longissimus dorsi,LD)中Ⅴ型胶原蛋白,对其进行蛋白质含量、热变性温度、氨基酸组成及傅里叶红外光谱分析,解析骨骼肌肌内结缔组织Ⅴ型胶原蛋白的特性。这对胶原蛋白特性与肉品质的关系研究具有重要意义。
样品来自内蒙古自治区锡林郭勒盟东乌珠穆沁旗,选取6、9、12、18 月龄乌珠穆沁羊,所选的各月龄肉羊是同一个羊群中年龄相同的去势公羊,每个月龄选取6 只羊作为平行。将肉羊屠宰后取半腱肌和背最长肌,适当分割后于液氮中速冻,然后存放于-80 ℃冰箱,冷冻保存备用。
胃蛋白酶(1∶10 000)、N-马来乙酰胺、苯甲基磺酰氟(phenylmethanesulfonyl fluoride,PMSF)、对二甲基苯甲醛 北京索莱宝科技有限公司;三羟基氨基甲烷(Tris碱)、过硫酸铵(ammonium sulfate,APS)、四甲基乙二胺(N,N,N’,N’-tetramethylethylenediamine,TEMED) 美国Sigma公司;乙二胺四乙酸二钠(ethylenediaminetetraacetic acid disodium salt,EDTA)天津市科盟化工工贸有限公司;氯胺T 国药集团化学试剂有限公司;L-羟脯氨酸 北京酷来搏科技有限公司;所有分离用有机溶剂均为国产分析纯。
XHF-DY高速分散器 宁波新芝生物科技股份有限公司;CP-100超速离心机、L-8900全自动氨基酸分析仪 日本Hitachi公司;BG-Power电泳仪 北京白晶生物技术有限公司;DZ-3335差示扫描量热仪(differential scanning calorimeter,DSC) 南京大展机电技术有限公司;IRAffinity-1傅里叶红外光谱仪 日本Shimadzu公司;TU-1810紫外-可见分光光度计 北京普析通用仪器有限公司。
1.3.1 Ⅴ型胶原蛋白的提取
参考Chandra[11]、永井裕[12]等的方法,并做适当调整。整个提取过程均在4 ℃条件下进行。样品在4 ℃条件下解冻,称取150 g骨骼肌组织,剔除肌外膜和脂肪后切碎,加入10 倍量的匀浆液(用5 mmol/L Tris-HCl缓冲液(pH 7.4)配制的10 g/100 mL NaCl),在3 000 r/min条件下匀浆30 s,此步骤重复3 次;搅拌之后离心(10 000×g,5 min),去除脂肪等其他组织,取沉淀加入10 倍量的洗净液(含10 mmol/L EDTA、10 mmol/L PMSF、12.5 μg/mL N-马来酰胺),反复冲洗5 次;10 000×g离心15 min,取沉淀加入胃蛋白酶(胃蛋白酶质量∶样品湿质量=1.5∶1),15 ℃消化48 h,100 000×g离心1 h,取上清液,加NaCl至浓度为0.7 mol/L,搅拌过夜;100 000×g离心1 h,取上清液,加NaCl至浓度为0.5 mol/L,搅拌过夜;100 000×g离心1 h,取沉淀,沉淀溶解于用0.05 mol/L Tris-HCl缓冲液(pH 7.4)配制的1.0 mol/L NaCl中;100 000×g离心1 h,取上清液,加入NaCl至浓度为4.5 mol/L,搅拌过夜;100 000×g离心1 h,取沉淀,沉淀溶解于0.1 mol/L的HAc,加NaCl至浓度为1.2 mol/L,搅拌过夜;100 000×g离心1 h,取沉淀,沉淀溶解于用0.05 mol/L Tris-HCl缓冲液(pH 7.4)配制的1.0 mol/L NaCl中,在同一个缓冲液中进行透析,100 000×g离心1 h取沉淀,沉淀即为Ⅴ型胶原蛋白。冷冻干燥后-20 ℃保存备用。
1.3.2 Ⅴ型胶原蛋白十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electropheresis,SDS-PAGE)分析
参考Leammli[13]的方法。采用不连续Tris-HCl/甘氨酸缓冲系统、8%的分离胶和5%的浓缩胶,称取一定量的冷冻干燥Ⅴ型胶原蛋白待测样,溶解于0.5 mol/L醋酸,与5×上样缓冲液(1 mol/L pH 6.8 Tris-HCl,50%丙三醇,β-巯基乙醇,1%溴酚蓝,10% SDS)以4∶1的比例混合,使Ⅴ型胶原蛋白的质量浓度为1 mg/mL,100 ℃水浴5 min;在10 000 r/min转速下离心10 min后取上清液,抽取15 μL分别加入加样孔,以同样的量取Marker加入样品孔,100 V恒压电泳,待指示液移到离边缘约1 cm处,停止电泳;凝胶用0.1%考马斯亮蓝R-250(含60 mL无水乙醇、14 mL冰乙酸、0.14 g考马斯亮蓝R-250、60 mL蒸馏水)进行染色,染色结束后在醋酸脱色液(含100 mL无水乙醇、30 mL冰乙酸和270 mL蒸馏水)中进行脱色,凝胶成像仪扫描分析。
1.3.3 Ⅴ型胶原蛋白含量的测定
参考Bergman等[14]的方法,并稍作调整。准确称取冷冻干燥的Ⅴ型胶原蛋白待测样30 mg置于具塞试管中,加入6 mol/L HCl,115 ℃水解12 h后加入2 mL氧化剂(含7 g/100 mL氯胺T、74% 26%异丙醇、0.629 mol/L NaOH、0.14 mol/L柠檬酸、0.453 mol/L乙酸钠和0.112 mol/L冰乙酸)充分混合,静置20 min,加入30 mL对二甲基苯甲醛(将2 g对二甲基苯甲醛溶解于3 mL 60%高氯酸,与异丙醇按3∶13的比例混合),65 ℃水浴20 min,冷却后采用紫外分光光度计于558 nm波长处测定吸光度。
1.3.4 傅里叶红外光谱检测
将2 mg冷冻干燥的Ⅴ型胶原蛋白待测样与2 mg KBr混合,研磨成粉并压制成薄片,置于傅里叶红外光谱仪内,在400~4 000 cm-1频率范围内进行扫描,分辨率为4 cm-1,扫描信号累加200 次[15]。
1.3.5 Ⅴ型胶原蛋白热变性温度的测定
准确称取冷冻干燥的Ⅴ型胶原蛋白待测样10 mg,置于铝坩埚并压实密封后以相同质量的铝坩埚为空白组,置于差式扫描热量仪内,在20~150 ℃温度范围内以1 ℃/min的速率进行测定[16]。
1.3.6 Ⅴ型胶原蛋白氨基酸组成分析
参考GB/T 5009.124—2003《食品中氨基酸的测定》[17]。将80 mg冷冻干燥的Ⅴ型胶原蛋白待测样置于具塞试管内,加入6 mol/L HCl至15 mL,抽真空封管,110 ℃水解24 h后,过滤,定容至50 mL;取1 mL减压蒸干后,加入0.02 mol/L的盐酸溶解,利用氨基酸自动分析仪测定胶原蛋白氨基酸组成。实验条件为:4.6 mm×60 mm分析柱,2622#树脂;柱温57 ℃;反应温度135 ℃。其中以柠檬酸-柠檬酸钠作为缓冲液,以茚三酮作为显色液。
实验数据用平均值±标准差(n=3)表示。2 组间比较采用T-test检验,P<0.05表示有显著差异。采用SPSS软件对数据进行分析,傅里叶红外光谱图线采用Origin 7.0软件进行分析。

图 1 骨骼肌肌内结缔组织中Ⅴ型胶原蛋白SDS-PAGE图
Fig. 1 SDS-PAGE pattern of type V collagen from intramuscular connective tissues in skeleton muscles
由图1可知,Ⅴ型胶原蛋白条带清晰,均出现了3 条肽链,推测其亚基组成为α1(Ⅴ)、α2(Ⅴ)、α3(Ⅴ),符合Ⅴ型胶原蛋白的结构特征,是Ⅴ型胶原蛋白常见的一种亚型。研究发现,Ⅴ型胶原是一种含量较少、组织分布广的纤维型胶原,并且至少有4 种同分异构体,包括2α1(Ⅴ)α2(Ⅴ)、α1(Ⅴ)α2(Ⅴ)α3(Ⅴ)、3α3(Ⅴ)、Ⅴ型胶原蛋白α链和Ⅺ型胶原蛋白α链的混合[18]。不同月龄、不同骨骼肌中Ⅴ型胶原蛋白3 种肽链呈现出相同的分子质量,条带及其颜色深浅差别不大。
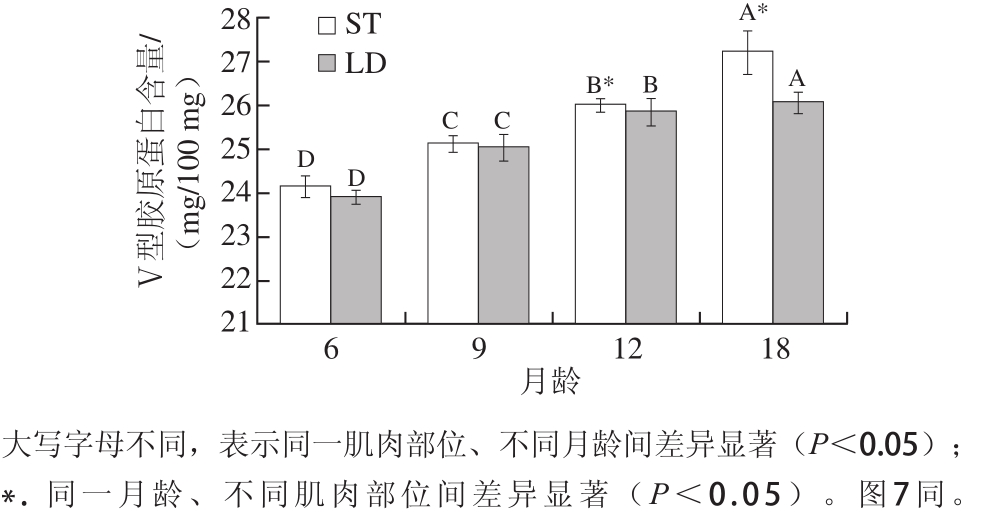
图 2 骨骼肌肌内结缔组织中Ⅴ型胶原蛋白的含量
Fig. 2 Content of type V collagen in intramuscular connective tissues in skeleton muscles
由图2可知:ST和LD肌内结缔组织中的Ⅴ型胶原蛋白含量随着月龄的增长而增加,且各月龄间差异显著(P<0.05);同一月龄,ST肌内Ⅴ型胶原蛋白的含量均高于LD;6 月龄和9 月龄ST和LD中肌内Ⅴ型胶原蛋白的含量没有显著差异(P>0.05),12 月龄和18 月龄时差异显著(P<0.05)。研究表明,胶原蛋白的含量受肌肉运动量的影响,与运动量较少的肌肉相比,经常运动的肌肉中肌束膜由更多胶原纤维束组成且较发达[19],胶原蛋白含量较高,肌束较粗,肉质较硬。各部位肉中所含胶原蛋白的含量不同,其嫩度也不同。Dubost等[20]的研究发现,股二头肌内胶原蛋白含量最高,其次是ST和LD。
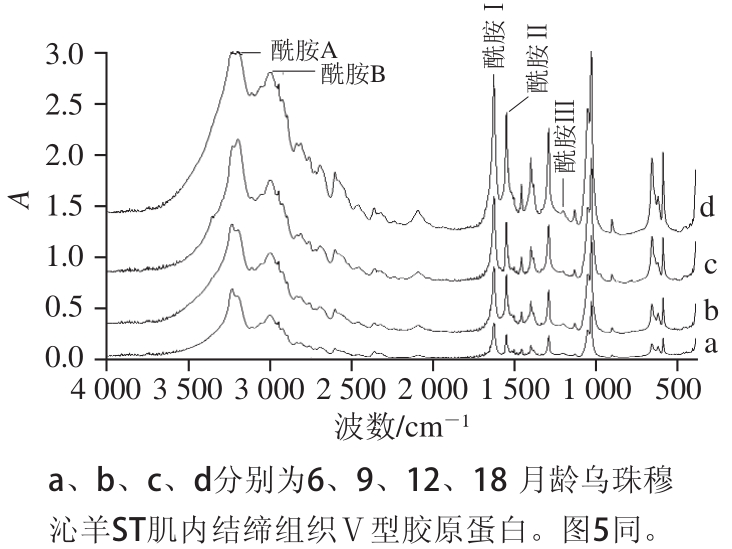
图 3 ST肌内结缔组织中Ⅴ型胶原蛋白的红外吸收光谱
Fig. 3 FTIR spectra of type V collagen in intramuscular connective tissue of ST
采用傅里叶红外光谱分别分析6、9、12、18 月龄乌珠穆沁羊ST和LD肌内结缔组织中Ⅴ型胶原蛋白的二级结构(三股螺旋结构)。由图3~4可知,各月龄乌珠穆沁羊骨骼肌肌内结缔组织中Ⅴ型胶原蛋白的红外光谱特征基本一致,均具有Ⅴ型胶原蛋白的特征红外吸收峰。
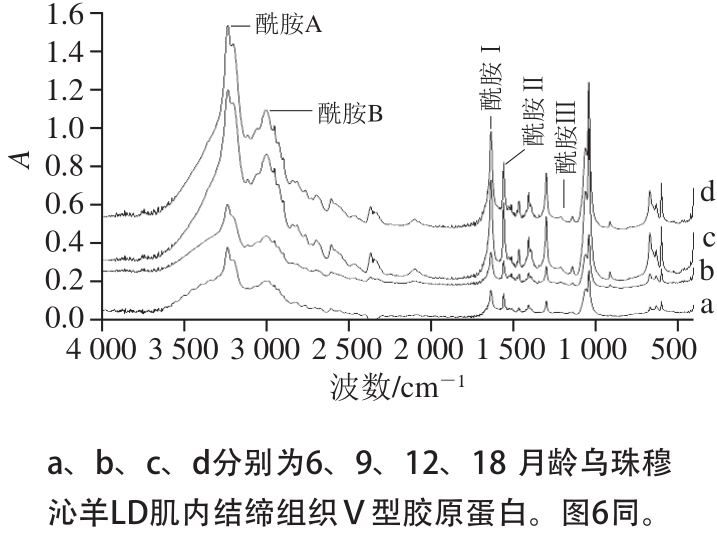
图 4 LD肌内结缔组织中Ⅴ型胶原蛋白的红外吸收光谱
Fig. 4 FTIR spectra of type Ⅴ collagen in intramuscular connective tissue of LD
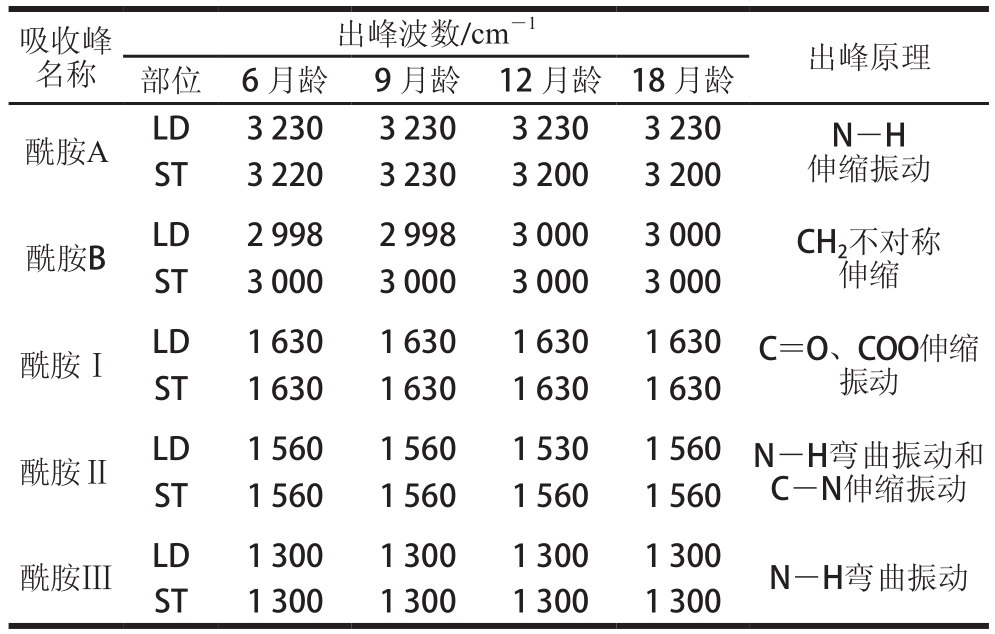
表 1 骨骼肌肌内结缔组织中Ⅴ型胶原蛋白红外光谱的出峰位置与形成原理
Table 1 FTIR spectral peak location and assignment for type Ⅴcollagen in intramuscular connective tissues of skeleton muscles
吸收峰名称出峰原理部位 6 月龄 9 月龄 12 月龄 18 月龄出峰波数/cm-1酰胺A LD 3 230 3 230 3 230 3 230 N-H伸缩振动ST 3 220 3 230 3 200 3 200酰胺B LD 2 998 2 998 3 000 3 000 CH2不对称伸缩ST 3 000 3 000 3 000 3 000酰胺Ⅰ LD 1 630 1 630 1 630 1 630 C=O、COO伸缩振动ST 1 630 1 630 1 630 1 630酰胺Ⅱ LD 1 560 1 560 1 530 1 560 N-H弯曲振动和C-N伸缩振动ST 1 560 1 560 1 560 1 560酰胺Ⅲ LD 1 300 1 300 1 300 1 300 N-H弯曲振动ST 1 300 1 300 1 300 1 300
由表1可知,酰胺A是由肽链上羰基的N-H基团伸缩振动而引起的特征峰[21],在3 400~3 440 cm-1范围内N-H基团发生自由的伸缩振动,然而,当N-H基团参与氢键的形成时N-H伸缩振动出峰的波数向低频移动[22]。各月龄LD中Ⅴ型胶原蛋白酰胺A的吸收峰均在波数3 230 cm-1处,但12和18 月龄ST中酰胺A出现略微向低频移动现象,说明有更多的N-H基团参与氢键的形成,从而使胶原蛋白螺旋结构结合在一起[23],这也是随着月龄的增加,胶原蛋白的热变性温度增大的可能原因。酰胺B是由CH2不对称伸缩振动引起的特征峰[24],各月龄Ⅴ型胶原蛋白均在波数3 000 cm-1处有吸收峰,但6、9 月龄LD中有向低频移动现象,说明随着月龄的增长,Ⅴ型胶原蛋白羧基之间有更多的分子结合[25]。
酰胺Ⅰ主要与胶原蛋白多肽链的羧基C=O伸缩振动有关[26],是胶原蛋白二级结构变化的敏感区域,与胶原蛋白分子的序度有关。Ⅴ型胶原蛋白酰胺Ⅰ的波数在各月龄及不同部位骨骼肌之间无差异,均在波数1 630 cm-1处,说明在胶原蛋白的提取过程中采用胃蛋白酶处理,原蛋白的三螺旋结构没有改变。酰胺Ⅱ的吸收峰均出现在波数1 560 cm-1处,正常情况下胶原蛋白酰胺Ⅱ的波数在1 550~1 600 cm-1范围内[27],主要来源于C-N伸缩振动和N-H弯曲振动,与酰胺Ⅰ带相比,酰胺Ⅱ带对胶原蛋白的二级结构不敏感[25],12 月龄LD中有略微向低频移动现象,但也在正常波数范围内。酰胺Ⅲ带是N-H弯曲振动引起的特征峰,属于甘氨酸骨架和脯氨酸侧链的CH2摇摆振动的体现[28]。各月龄Ⅴ型胶原蛋白的酰胺Ⅲ带在波数1 300 cm-1处出现吸收峰。经傅里叶红外光谱仪分析其二级结构发现,各月龄Ⅴ型胶原蛋白均出现了主要吸收峰,且峰形相似,吸收峰出现的波数有所不同。相对来讲,ST波数与LD相比发生了微小的向低频移动现象。ST酰胺A的波频低于LD,这说明ST与LD相比有更多的N-H基团参与胶原蛋白分子内氢键的形成。
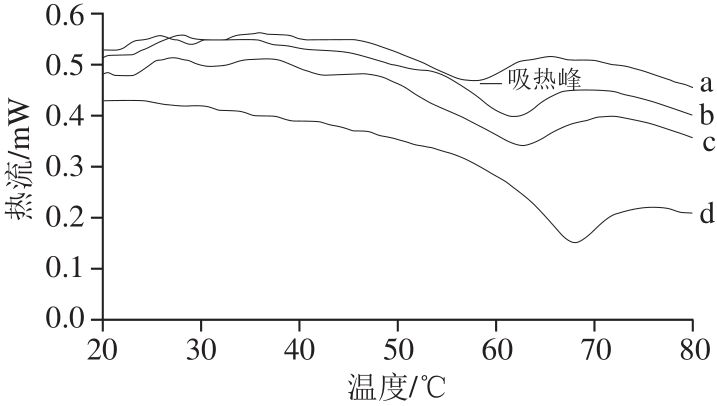
图 5 ST肌内结缔组织中Ⅴ型胶原蛋白的DSC结果图
Fig. 5 DSC thermograms of type V collagen in intramuscular connective tissue of ST
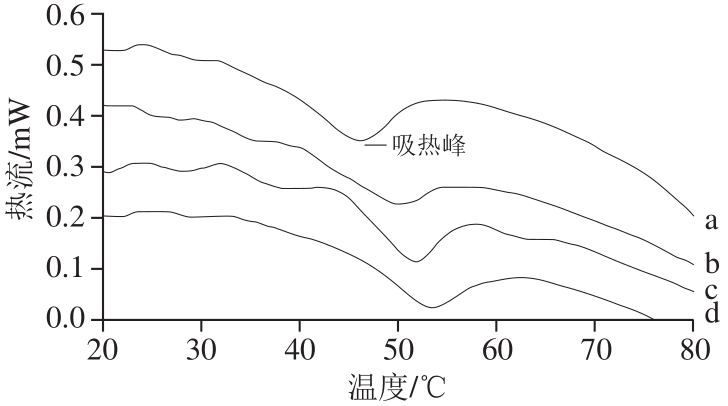
图 6 LD肌内结缔组织中Ⅴ型胶原蛋白的DSC结果图
Fig. 6 DSC thermograms of type V collagen in intramuscular connective tissue of LD
胶原蛋白的热变性温度是指胶原蛋白在介质中受热,到达一定温度后,三螺旋结构发生解旋,各自形成单链,三螺旋解旋到50%时的温度。由图5~6可知,不同月龄乌珠穆沁羊骨骼肌肌肌内结缔组织中Ⅴ型胶原蛋的DSC热流分析曲线均出现了明显的吸热峰,为Ⅴ型胶原蛋白的热变性温度,其与胶原的被破坏程度有关[29]。
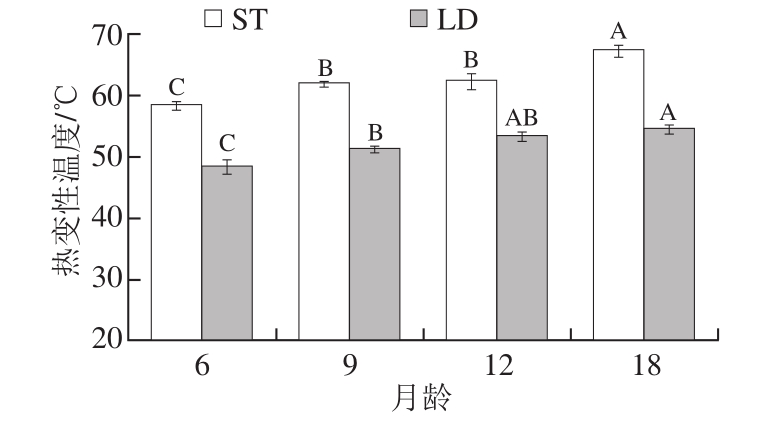
图 7 骨骼肌肌内结缔组织中Ⅴ型胶原蛋白的热变性温度
Fig. 7 Td of type V collagen in intramuscular connective tissues of skeleton muscles
由图7可知:乌珠穆沁羊ST肌内结缔组织中Ⅴ型胶原蛋白的热变性温度随着月龄的增长而升高,9 月龄和12 月龄之间没有显著差异(P>0.05),其他月龄间均有显著差异(P<0.05);LD肌内结缔组织中Ⅴ型胶原蛋白的热变性温度随着月龄的增长而显著升高(P<0.05),但9 月龄和12 月龄及12 月龄和18 月龄间均无显著差异(P>0.05)。这可能与胶原蛋白脯氨酸的羟基化程度和胶原蛋白共价交联的数量和交联的性质有关[30]。因此,同一月龄ST的热变性温度高于LD。
胶原蛋白的理化特性,特别是热变性温度与其氨基酸组成密切相关。由表2可知:ST内每100 mgⅤ型胶原蛋白样品(干质量)的氨基酸含量分别为25.11、27.20、28.22、29.50 mg,随着月龄的增长而增加,且各月龄间有显著差异(P<0.05);Ⅴ型胶原蛋白中甘氨酸含量较多,在胶原的螺旋结构中起着重要作用,约占氨基酸总量的20%,在6、9、12、18 月龄间,其含量随着月龄的增加呈增加趋势。胶原中脯氨酸(Pro)、甘氨酸(Gly)和羟脯氨酸(Hyp)含量较高,这是由于胶原(Gly-Pro-Hyp)n三重螺旋重复的特征性所致[31]。每100 mgⅤ型胶原蛋白样品的亚氨基酸含量分别为4.71、5.12、5.18、5.66 mg,随着月龄的增长而增长,且各月龄间有显著差异(P<0.05)。丙氨酸、谷氨酸是Ⅴ型胶原蛋白的主要构成氨基酸,丙氨酸含量随着月龄的增加而显著增加(P<0.05),而谷氨酸含量随着月龄的增长有上升的趋势,12、18 月龄间差异不显著(P>0.05),其他月龄间均有显著差异(P<0.05)。然而,Ⅴ型胶原蛋白样品的酪氨酸和蛋氨酸含量较低,只占总氨基酸含量的2%,检出极少量的半胱氨酸。胶原蛋白亚氨基酸含量与胶原蛋白热变性温度有关,这一结果也证实了随着月龄的增长骨骼肌肌内结缔组织中Ⅴ型胶原蛋白的热变性温度增加这一结论。
表 2 骨骼肌肌内结缔组织中Ⅴ型胶原蛋白的氨基酸组成
Table 2 Amino acid composition of collagen type Ⅴ in intramuscular connectives tissues of skeleton muscles mg/100 mg
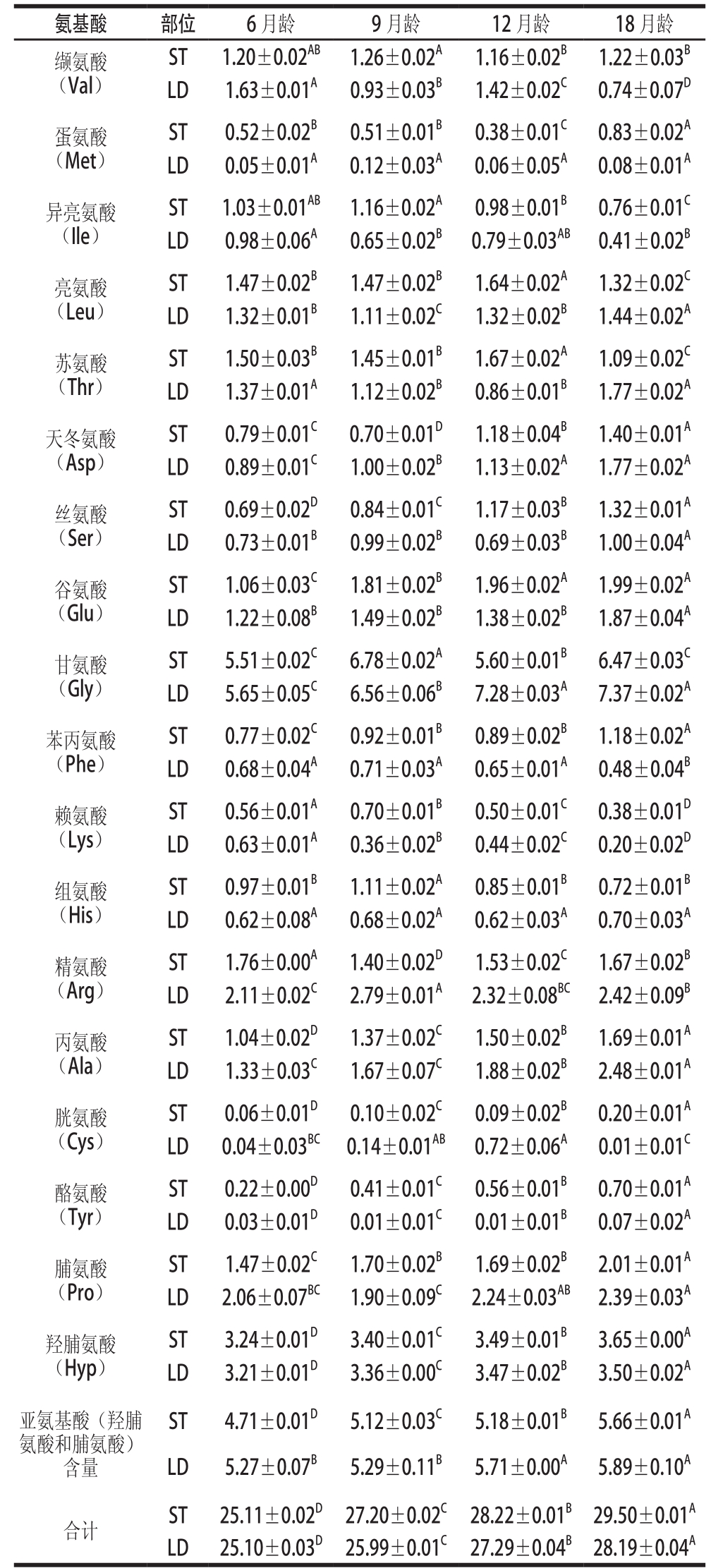
注:同行大写字母不同,表示同一肌肉部位、不同月龄间差异显著(P<0.05)。
ST 0.52±0.02B 0.51±0.01B 0.38±0.01C 0.83±0.02A LD 0.05±0.01A 0.12±0.03A 0.06±0.05A 0.08±0.01A异亮氨酸(Ile)氨基酸 部位 6 月龄 9 月龄 12 月龄 18 月龄ST 1.20±0.02AB 1.26±0.02A 1.16±0.02B 1.22±0.03B LD 1.63±0.01A 0.93±0.03B 1.42±0.02C 0.74±0.07D蛋氨酸(Met)缬氨酸(Val)ST 1.03±0.01AB 1.16±0.02A 0.98±0.01B 0.76±0.01C LD 0.98±0.06A 0.65±0.02B 0.79±0.03AB 0.41±0.02B亮氨酸(Leu)ST 1.50±0.03B 1.45±0.01B 1.67±0.02A 1.09±0.02C LD 1.37±0.01A 1.12±0.02B 0.86±0.01B 1.77±0.02A天冬氨酸(Asp)ST 1.47±0.02B 1.47±0.02B 1.64±0.02A 1.32±0.02C LD 1.32±0.01B 1.11±0.02C 1.32±0.02B 1.44±0.02A苏氨酸(Thr)ST 0.69±0.02D 0.84±0.01C 1.17±0.03B 1.32±0.01A LD 0.73±0.01B 0.99±0.02B 0.69±0.03B 1.00±0.04A谷氨酸(Glu)ST 0.79±0.01C 0.70±0.01D 1.18±0.04B 1.40±0.01A LD 0.89±0.01C 1.00±0.02B 1.13±0.02A 1.77±0.02A丝氨酸(Ser)ST 5.51±0.02C 6.78±0.02A 5.60±0.01B 6.47±0.03C LD 5.65±0.05C 6.56±0.06B 7.28±0.03A 7.37±0.02A苯丙氨酸(Phe)ST 1.06±0.03C 1.81±0.02B 1.96±0.02A 1.99±0.02A LD 1.22±0.08B 1.49±0.02B 1.38±0.02B 1.87±0.04A甘氨酸(Gly)ST 0.77±0.02C 0.92±0.01B 0.89±0.02B 1.18±0.02A LD 0.68±0.04A 0.71±0.03A 0.65±0.01A 0.48±0.04B赖氨酸(Lys)ST 0.97±0.01B 1.11±0.02A 0.85±0.01B 0.72±0.01B LD 0.62±0.08A 0.68±0.02A 0.62±0.03A 0.70±0.03A精氨酸(Arg)ST 0.56±0.01A 0.70±0.01B 0.50±0.01C 0.38±0.01D LD 0.63±0.01A 0.36±0.02B 0.44±0.02C 0.20±0.02D组氨酸(His)ST 1.04±0.02D 1.37±0.02C 1.50±0.02B 1.69±0.01A LD 1.33±0.03C 1.67±0.07C 1.88±0.02B 2.48±0.01A胱氨酸(Cys)ST 1.76±0.00A 1.40±0.02D 1.53±0.02C 1.67±0.02B LD 2.11±0.02C 2.79±0.01A 2.32±0.08BC 2.42±0.09B丙氨酸(Ala)ST 1.47±0.02C 1.70±0.02B 1.69±0.02B 2.01±0.01A LD 2.06±0.07BC 1.90±0.09C 2.24±0.03AB 2.39±0.03A羟脯氨酸(Hyp)ST 0.22±0.00D 0.41±0.01C 0.56±0.01B 0.70±0.01A LD 0.03±0.01D 0.01±0.01C 0.01±0.01B 0.07±0.02A脯氨酸(Pro)ST 0.06±0.01D 0.10±0.02C 0.09±0.02B 0.20±0.01A LD 0.04±0.03BC 0.14±0.01AB 0.72±0.06A 0.01±0.01C酪氨酸(Tyr)ST 3.24±0.01D 3.40±0.01C 3.49±0.01B 3.65±0.00A LD 3.21±0.01D 3.36±0.00C 3.47±0.02B 3.50±0.02A ST 4.71±0.01D 5.12±0.03C 5.18±0.01B 5.66±0.01A LD 5.27±0.07B 5.29±0.11B 5.71±0.00A 5.89±0.10A合计 ST 25.11±0.02D 27.20±0.02C 28.22±0.01B 29.50±0.01A LD 25.10±0.03D 25.99±0.01C 27.29±0.04B 28.19±0.04A亚氨基酸(羟脯氨酸和脯氨酸)含量
研究表明,胶原蛋白亚氨基酸含量与胶原蛋白的热变性温度具有正相关性,羟脯氨酸含量越高,胶原蛋白的热稳定性越高[32]。胶原蛋白亚氨基酸含量以及脯氨酸和赖氨酸的羟基化程度对胶原蛋白的热变性起着重要的作用,主要原因是脯氨酸和羟脯氨酸含有的吡咯环限制性改变胶原蛋白多肽链的二级结构,吡咯环越多的胶原蛋白热稳性越高[33]。对于LD肌内结缔组织中的Ⅴ型胶原蛋白,其氨基酸总量为每100 mg Ⅴ型胶原蛋白样品(干质量)中氨基酸总量分别为21.90、22.63、23.83、24.70 mg,随着月龄增长而增加,且各月龄间差异显著(P<0.05);其甘氨酸随着月龄的增长而增加,除了12 月龄和18 月龄无显著差异(P>0.05)外,其他月龄间均差异显著(P<0.05);其亚氨基酸含量分别为5.27、5.29、5.71、5.89 mg/100 mg,随着月龄的增长而增长,6 月龄和9 月龄、12 月龄和18 月龄间无显著差异(P>0.05)。
对不同月龄肌内结缔组织中Ⅴ型胶原蛋白的氨基酸组成进行分析发现,甘氨酸的含量占氨基酸总量的1/3左右,甘氨酸、天冬氨酸、脯氨酸的含量较高,蛋氨酸、酪氨酸的含量较低。氨基酸组成与Wang Lin等[34]的研究结果一致,其研究指出Ⅴ型胶原蛋白的谷氨酸、脯氨酸含量较高(每1 000 个氨基酸残基中分别含有321.78、112.23 个残基),酪氨酸和蛋氨酸含量较低(每1 000 个氨基酸残基中分别含有2.35、6.69 个残基)。总体来看,ST中的氨基酸含量略高于LD。
本研究通过酸溶、胃蛋白酶酶解和盐析等方法,从乌珠穆沁羊骨骼肌肌内结缔组织中提取出Ⅴ型胶原蛋白。SDS-PAGE结果显示,所提取的Ⅴ型胶原蛋白均出现3 条肽链,推测其亚基组成为α1(Ⅴ)、α2(Ⅴ)、α3(Ⅴ)。傅里叶变换红外光谱分析Ⅴ型胶原蛋白在酰胺A、B和酰胺Ⅰ、Ⅱ、Ⅲ带出现的特征吸收峰,结果表明,提取过程中胶原蛋白的三螺旋结构保持完整。乌珠穆沁羊骨骼肌肌内结缔组织中Ⅴ型胶原蛋白含量随着月龄的增长而增长,并且各月龄间有显著差异(P<0.05)。不同月龄乌珠穆沁羊ST和LD肌内结缔组织中Ⅴ型胶原蛋白的热变性温度随着月龄的增长而升高。Ⅴ型胶原蛋白的总氨基酸含量、亚氨基酸含量、羟脯氨酸含量随着月龄的增长而呈上升趋势,且各月龄间有显著差异(P<0.05)。ST中Ⅴ型胶原蛋白含量、热变性温度和氨基酸含量等均高于LD。
[1] GILLIES A R, LIEBER R L. Structure and function of the skeletal muscle extracellular matrix[J]. Muscle and Nerve, 2011, 44(3):318-331. DOI:10.1002/mus.22094.
[2] NISHIMURA T. Role of extracellular matrix in development of skeletal muscle and postmortem aging of meat[J]. Meat Science, 2015,109: 48-55. DOI:10.1016/j.meatsci.2015.05.015.
[3] DUBOST A, MICOL D, MEUNIER B, et al. Relationships between structural characteristics of bovine intramuscular connective tissue assessed by image analysis and collagen and proteoglycan content[J]. Meat Science, 2013, 93(3): 378-386. DOI:10.1016/j.meatsci.2012.09.020.
[4] 帕提姑·阿布都克热. 新疆羊肉食用品质特性及相关影响因素的研究[D]. 乌鲁木齐: 新疆农业大学, 2012: 9-11.
[5] VELLEMAN S G. The role of the extracellular matrix in skeletal muscle development[J]. Poultry Science, 1999, 78(5): 778-784.DOI:10.1093/ps/78.5.778.
[6] 吴琼. 乌珠穆沁羊骨骼肌肌内结缔组织中Ⅰ、Ⅲ型胶原蛋白特性研究[D]. 呼和浩特: 内蒙古农业大学, 2016: 19-41.
[7] 吕雅琼, 张冬梅, 格日勒图. 乌珠穆沁羊生长过程中肌内结缔组织中Ⅰ型胶原蛋白变化研究[J]. 农产品加工(学刊), 2013(15): 13-16.DOI:10.3969/jissn.1671-9646(X).2013.08.005.
[8] MIZUNO K, BACHINGER H P, IMAMURA Y, et al. Fragility of reconstituted type V collagen fibrils with the chain composition of α1(Ⅴ)α2(Ⅴ)α3(Ⅴ) respective of theD-periodic banding pattern[J].Connective Tissue Research, 2013, 54(1): 41-48. DOI:10.3109/030082 07.2012.734876.
[9] 高玲玲, 侯成立, 高远, 等. 胶原蛋白热稳定性研究进展[J].中国食品学报, 2018, 18(5): 200-212. DOI:10.16429/j.1009-7848.2018.05.024.
[10] MYLLYHARJU J. Intracellular post-translational modifications of collagens[J]. Topics in Current Chemistry, 2005, 247: 115-147.DOI:10.1007/b103821.
[11] CHANDRA RAJAN J. Separation of type Ⅲ collagen from type Ⅰcollagen and pepsin by differential denaturation and renaturation[J].Biochemical and Biophysical Research Communications, 1978, 83(1):180-186. DOI:10.1016/0006-291X(78)90414-X.
[12] 永井裕, 藤本大三郎. 胶原蛋白实验方法[M]. 刘平, 译. 上海: 上海中医学院出版社, 1992: 39-48.
[13] LAEMMLI U K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4[J]. Nature, 1970, 227: 680-685.
[14] BERGMAN I, LOXLEY R. Two improved and simplified methods for the spectrophotometric determination of hydroxyproline[J]. Analytical Chemistry, 1963, 35(12): 1961-1965. DOI:10.1021/ac60205a053.
[15] 温慧芳, 陈丽丽, 白春清, 等. 基于不同提取方法的鮰鱼皮胶原蛋白理化性质的比较研究[J]. 食品科学, 2016, 37(1): 74-81.DOI:10.7506/spkx1002-6630-201601014.
[16] WU Xiaomeng, LIU Yaowen, LIU Anjun, et al. Improved thermalstability and mechanical properties of type Ⅰ collagen by crosslinking with casein, keratin and soy protein isolate using transglutaminase[J].International Journal of Biological Macromolecules, 2017, 98:292-301. DOI:10.1016/j.ijbiomac.2017.01.127.
[17] 中国预防医学科学院营养与食品卫生研究所. 食品中氨基酸的测定: GB/T 5009.124—2003[S]. 北京: 中国标准出版社, 2003.
[18] 汤克勇. 胶原物理与化学[M]. 北京: 科学出版社, 2012: 116-117.
[19] 黄明. 牛肉成熟机制及食用品质研究[D]. 南京: 南京农业大学,2003: 81-91.
[20] DUBOST A, MICOL D, MEUNIER B, et al. Relationships between structural characteristics of bovine intramuscular connective tissue assessed by image analysis and collagen and proteoglycan content[J]. Meat Science, 2013, 93(3): 378-386. DOI:10.1016/j.meatsci.2012.09.020.
[21] 蔡路昀, 马帅, 李秀霞, 等. 不同提取方法对鲽鱼皮胶原蛋白结构特征和功能性质的影响[J]. 食品与发酵工业, 2017, 43(5): 240-246.DOI:10.13995/j.cnki.11-1802/ts.201705039.
[22] 马帅, 王静, 曹爱玲, 等. 不同部位鲽鱼皮酸溶性胶原蛋白的制备及理化特性分析[J]. 中国食品学报, 2018, 18(8): 154-161.DOI:10.7506/spkx1002-6630-201711009.
[23] WANG Zhenbin, WANG Lin, LIN Shiman, et al. Isolation and characterization of collagen from the muscle of Amur sturgeon(Acipenser schrenckii)[J]. Biotechnology and Bioprocess Engineering,2014, 19(5): 935-941. DOI:10.1007/s12257-013-0638-0.
[24] JEEVITHAN E, BU Y S, BAO B, et al. Effect of chemical and biological cross-linkers on mechanical and functional properties of shark catfish skin collagen films[J]. Food Bioscience, 2017, 17: 42-51.DOI:10.1016/j.fbio.2016.12.002.
[25] DOYLE B B, BENDIT E G, BLOUT E R. Infrared spectroscopy of collagen and collagen-like polypeptides[J]. Biopolymers, 1975, 14:937-957. DOI:10.1002/bip.1975.360140505.
[26] SI Leilei, FAN Yan, WANG Yuekun, et al. Thermal degradation behavior of collagen from sea cucumber (Stichopus japonicus) using TG-FTIR analysis[J]. Thermochimica Acta, 2017, 659: 166-171.DOI:10.1016/j.tca.2017.12.004.
[27] PATI F, ADHIKARI B, DHARA S. Isolation and characterization of fish scale collagen of higher thermal stability[J]. Bioresource Technology, 2010, 101(10): 3737-3742. DOI:10.1016/j.biortech.2009.12.133.
[28] THUY L T M, OKAZAKI E, OSAKO K. Isolation and characterization of acid-soluble collagen from the scales of marine fishes from Japan and Vietnam[J]. Food Chemistry, 2014, 149:264-270. DOI:10.1016/j.foodchem.2013.10.094.
[29] SAFANDWSKA M, PIETRUCHA K. Effect of fish collagen modification on its thermal and rheological properties[J]. International Journal of Biological Macromollecules, 2013, 53: 32-37. DOI:10.1016/j.ijbiomac.2012.10.026.
[30] HADIAN M, CORCORAN B M, BRADSHAW J P. Molecular changes in fibrillar collagen in myxomatous mitral valve disease[J].Cardiovascular Pathology, 2010, 19(5): e141-e148. DOI:10.1016/j.carpath.2009.05.001.
[31] ZHANG Fengxiang, WANG Anning, LI Zhihua, et al. Preparation and characterisation of collagen from freshwater fish scales[J].Food and Nutrition Sciences, 2011, 2(8): 1810-1817. DOI:10.4236/fns.2011.28112.
[32] IKOMA T, KOBAYASHI H, TANAKA J, et al. Physical properties of type Ⅰ collagen extracted from fish scales of Pagrus major andOreochromis niloticas[J]. International Journal of Biological Macromolecules, 2003, 32(3): 199-204. DOI:10.1016/s0141-8130(03)00054-0.
[33] 张悦容, 胡玲萍, 刘文, 等. 处理方法对仿刺参体壁蛋白纤维超微结构的影响[J]. 中国食品学报, 2015, 15(5): 219-224. DOI:10.16429/j.1009-7848.2015.05.030.
[34] WANG Lin, LIANG Qiufang, WANG Zhenbin, et al. Preparation and characterisation of type Ⅰand Ⅴ collagens from the skin of Amur sturgeon (Scipenser schrenckii)[J]. Food Chemistry, 2014, 148:410-414. DOI:10.1016/j.foodchem.2013.10.074.
Characteristics of Type Ⅴ Collagens in Intramuscular Connective Tissue from Sheep of Different Ages
薛文俊, 曹欣宇, 吴琼, 等. 不同月龄肉羊肌内结缔组织中Ⅴ型胶原蛋白的特性[J]. 肉类研究, 2019, 33(3): 7-13.DOI:10.7506/rlyj1001-8123-20190117-015. http://www.rlyj.net.cn
XUE Wenjun, CAO Xinyu, WU Qiong, et al. Characteristics of type Ⅴ collagens in intramuscular connective tissue from sheep of different ages[J]. Meat Research, 2019, 33(3): 7-13. DOI:10.7506/rlyj1001-8123-20190117-015. http://www.rlyj.net.cn