氧化是导致肉制品在加工和贮藏过程中品质被破坏的主要因素之一。肉制品的氧化可分为脂肪氧化和蛋白氧化,二者具有相似的氧化过程,均包括起始、传递和终止3 个阶段[1-2]。脂肪氧化最终产生小分子的醛、酮等有机化合物,过度氧化使肉制品产生不愉快气味[3]。蛋白氧化会影响蛋白质的理化性质,对肉制品的营养价值、风味及加工特性产生不利影响[4]。抑制脂肪氧化在一定程度上可以抑制蛋白氧化。在肉制品加工过程中,可以通过添加抗氧化剂和采用合适的包装方法来抑制肉制品的氧化[5]。抗氧化剂按来源可分为人工抗氧化剂和天然抗氧化剂,天然抗氧化剂由于更符合消费者要求、更加安全健康而备受关注[6]。
没食子酸(3,4,5-三羟基苯甲酸)别名棓酸、五倍子酸等,是一种白色或淡黄色的粉末,通常以单宁的形式存在于如蔬菜、水果、五倍子、白芍及漆树叶等植物中[7]。没食子酸具有较好的抑菌、抗炎、抗病毒、抗氧化及抗肿瘤等生物活性[8],其中抗氧化特性在食品工业中尤其受到关注。Cao等[9]在没食子酸对猪肉肌原纤维蛋白氧化和凝胶特性的影响研究中,发现没食子酸能抑制蛋白质羰基的形成,但高浓度的没食子酸降低了蛋白质的凝胶性能。蛋白质的凝胶特性与肉制品的食用品质密切相关,因此,在研究天然抗氧化剂对肉制品氧化抑制作用的同时,有必要研究其对肉品品质特性的影响。本研究通过测定猪肉糜硫代巴比妥酸反应物(thiobarbituric acid reactive substance,TBARs)值、羰基含量、表面疏水性、总巯基含量、蒸煮损失及色差,探讨没食子酸对猪肉糜贮藏过程中脂肪和蛋白氧化的抑制作用,同时考察其对猪肉糜品质特性的影响,为深入研究多酚类抗氧化剂在肉及肉制品中的应用提供理论基础。
猪背最长肌、猪肥膘,购于当地超市。
丁基羟基茴香醚(butyl hydroxyanisole,BHA)(分析纯) 国药集团化学试剂有限公司;没食子酸(分析纯) 美国Sigma公司;氯化钠、磷酸二氢钠和乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)(均为分析纯) 天津市风船化学试剂科技有限公司;氯化镁、甲醇(均为分析纯) 天津市津东天正精细化学试剂厂。
Allegra 64R高速冷冻离心机 美国贝克曼库尔特公司;TA-XT2i质构仪 英国Stable Micro Systems公司;FE20 pH计、PL203电子天平 梅特勒-托利多仪器(上海)有限公司:UV2550紫外-可见分光光度计 日本Shimadzu公司;T25均质乳化机 德国IKA集团;CR-400色彩色差计 日本Konica Minolta公司;奥克斯HX-J3011绞肉机 佛山市海迅电器有限公司。
1.3.1 肉糜的制备
肉糜的制备在4 ℃冷库中进行。肉糜的基础配方为猪背最长肌(70%)、猪肥膘(10%)、水(18%)和氯化钠(2%)。将猪背最长肌与猪肥膘分别加入绞肉机中绞碎(30 s,快速档),按比例添加原料和辅料,充分混匀,将混匀的猪肉糜分为5 组,第1组为空白对照组(不添加抗氧化剂),第2~4组分别加入0.05、0.10、0.20 g/kg没食子酸,第5组加入0.20 g/kg BHA作为阳性对照;混匀,取质量为50 g的肉糜,制成肉饼(直径约为7 cm,厚度约为1 cm),将肉饼放入包装盒(CT盒)中(3 个/盒),再用保鲜膜封好,置于冰箱中冷藏(4 ℃),分别在1、3、6、9 d测定各项指标。
1.3.2 肌原纤维蛋白的提取
参照Park等[10]的方法进行,作适当修改。称取适量的猪肉糜,加入4 倍体积的10 mmol/L磷酸盐提取液(含1 mmol/L EDTA、100 mmol/L NaCl和2 mmol/L MgCl2,pH 7.0),于4 ℃条件下匀浆,3 500 r/min离心15 min(4 ℃);去上清液,取沉淀,将上述步骤重复2 次;将得到的粗肌原纤维蛋白样品用4 倍体积洗液(100 mmol/L NaCl,4 ℃)清洗,离心,取沉淀,重复1 次后,加入洗液,用4 层纱布过滤,用盐酸溶液(0.1 mol/L)调节pH值为6.0,离心(15 min,3 500 r/min,4 ℃);去上清液,沉淀称质量,于4 ℃保存,24 h内用完。
1.3.3 TBARs值的测定
参照Jongberg等[11]的方法。称取5 g肉糜加入到离心管中,再加入15 mL混合溶液(含7.5%三氯乙酸、0.1%没食子酸和0.1% EDTA),均质60 s(9 000 r/min),离心(5 min,3 500 r/min,4 ℃),过滤;取2.5 mL滤液加入试管中,再加入2.5 mL 0.02 mol/L硫代巴比妥酸溶液,水浴(90 ℃,50 min),冷却,532 nm波长处测定吸光度。以每千克肉糜样品中丙二醛的含量表示TBARs值,按照公式(1)计算。
式中:A为溶液的吸光度;ε为摩尔吸光系数(156 000 L/(mol·cm));V为样品体积/mL;I为光程(1 cm);M为丙二醛的分子质量(72.063 g/mol);m为肉糜质量/kg。
1.3.4 总巯基含量的测定
将Ellman[12]的方法稍作修改。量取8 mL Tris-甘氨酸溶液(含10.4 g/L Tris、0.9 g/L甘氨酸、1.2 g/L EDTA和8 mol/L尿素,pH 8.0)和1 mL 5 mg/mL肌原纤维蛋白溶液,置于塑料离心管中;均质后,在10 000 r/min条件下离心15 min(4 ℃),除去不溶性蛋白;量取4.5 mL上清液,加入0.5 mL Ellman试剂,充分混匀,室温下静置30 min,412 nm波长处测定吸光度,计算肌原纤维蛋白中总巯基含量,使用的分子吸光系数为13 600 L/(mol·cm)。
1.3.5 羰基含量的测定
参照Ortuño等[13]的方法,并略加修改。取1 mL 10 mmol/L 2,4-二硝基苯肼溶液,加入装有3 mL 5 mg/mL肌原纤维蛋白溶液的塑料离心管中,空白对照组加入1 mL HCl溶液(2 mol/L),室温下静置1 h(每15 min振荡1 次),然后加入1 mL 20%三氯乙酸溶液,在10 000 r/min条件下离心5 min(4 ℃),取沉淀,用乙酸乙酯-乙醇(5 mL)洗涤3 次,以除去未反应的试剂,然后加入盐酸胍溶液(3 mL,6 mol/L),溶解蛋白沉淀(37 ℃),在10 000 r/min条件下离心5 min(4 ℃),过滤,去沉淀,滤液在370 nm波长处测定吸光度,计算肌原纤维蛋白中羰基含量,分子吸光系数为22 000 L/(mol·cm)。
1.3.6 表面疏水性的测定
参照Chelh等[14]的方法。取一定量的肌原纤维蛋白样品溶于20 mmol/L磷酸缓冲溶液(pH 7.0),配制成质量浓度为5 mg/mL的蛋白溶液;取1 mL蛋白溶液,加入200 μL溴酚蓝(1 mg/mL),充分混匀,冷冻离心15 min(6 000 r/min);取上清液稀释10 倍,以未添加蛋白溶液的磷酸盐缓冲溶液为对照组,595 nm波长处测定吸光度。表面疏水性用溴酚蓝结合量来表示,按照公式(2)计算。
1.3.7 色差的测定
使用色差仪对肉糜中心部位进行颜色测定,先用标准白板进行校正,将样品放置于平面上,将色差仪镜面垂直紧扣于肉糜上,在样品上随机测量(3 次),记录数据,分别得到亮度值(L*)、红度值(a*),将3 次测量的平均值作为色差值。
1.3.8 蒸煮损失率的测定
称取肉糜样品,质量记为m1(g),置于离心管中,1 000 r/min离心5 min,然后将肉样置于水浴锅中蒸煮(85 ℃,30 min);蒸煮后取出样品,冷却至室温,用吸水纸吸干肉样表面水分,然后称肉糜质量,记为m2(g);肉糜放在4 ℃环境中保存。蒸煮损失率按照公式(3)计算。
每个实验重复3 次,结果表示为平均值±标准差。采用Sigmaplot 12.5软件作图,采用SPSS 19.0软件中的Tukey HSD程序进行显著性分析(P<0.05)。
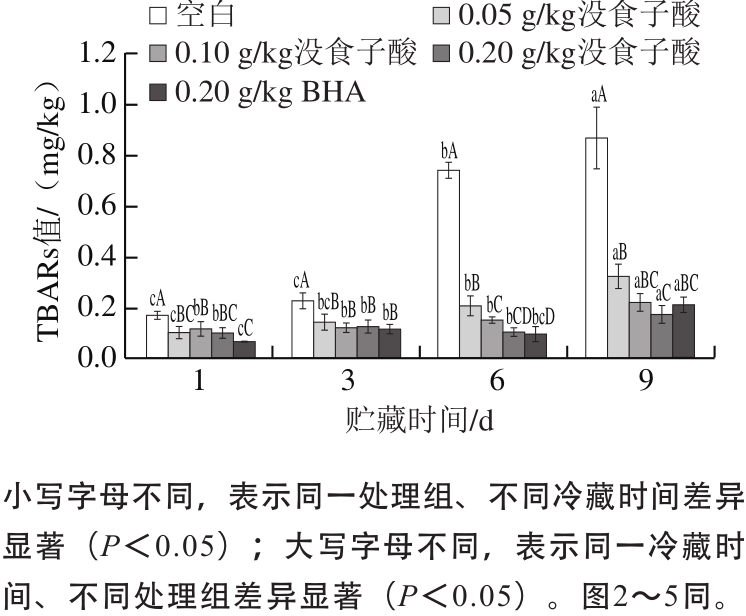
图 1 没食子酸对冷藏猪肉糜TBARs值的影响
Fig. 1 Effect of gallic acid on TBARs value of pork patties during chilled storage
由图1可知,随着贮藏时间的延长,所有处理组猪肉糜的TBARs值均增加,而添加没食子酸和BHA使TBARs值增加的幅度降低。在整个贮藏期间,处理组猪肉糜的TBARs值始终显著小于空白组(P<0.05),并且当贮藏时间达到第9天时0.20 g/kg没食子酸组的TBARs值最小,说明没食子酸能够抑制脂肪氧化,减少丙二醛等次级氧化产物的生成,且在一定浓度范围内,其抑制效果与添加量呈正比。0.20 g/kg没食子酸组和BHA组猪肉糜的TBARs值差异不显著(P>0.05),说明没食子酸对脂肪氧化的抑制效果与BHA相当,没食子酸能够显著降低预加工猪肉TBARs值的增加,其原因是没食子酸结构中的三酚羟基结构能猝灭自由基,这与De Jong等[15]的研究结果一致。Yen等[16]研究表明,低浓度没食子酸促进金属离子Fe2+的生成,形成促氧化环境;而高浓度没食子酸通过自由基清除作用减少氧化产物的生成,抑制脂肪氧化,说明没食子酸的抗氧化活性与其浓度密切相关。
蛋白氧化会造成疏基含量减少,因此疏基含量是描述蛋白氧化程度的一个重要指标[17]。由图2可知,冷藏猪肉糜的巯基含量在冷藏过程中不断减少,贮藏到第9天时,空白组猪肉糜的巯基含量由最初的86.67 nmol/mg显著下降至31.76 nmol/mg(P<0.05),说明内部巯基基团被氧化成二硫键,时间延长,氧化加剧[18]。贮藏第1~6天时,除第1天0.05 g/kg没食子酸组和第3天0.20 g/kg没食子酸组外,其他组的总巯基含量均低于空白组,说明没食子酸和BHA不能减弱巯基的损失程度,这可能是由于没食子酸或BHA与巯基发生反应,也可能是由于巯基发生脱氢反应,形成分子间的二硫键或者是巯基氧化成非二硫键,从而降低了巯基含量[19]。至贮藏第9天时,没食子酸组和BHA组猪肉糜的总疏基含量均高于空白组,说明随着贮藏时间延长,没食子酸逐渐发挥其结构特点,自身的羟基基团与过氧自由基相互反应,猝灭自由基团,保护巯基不受损失[18]。
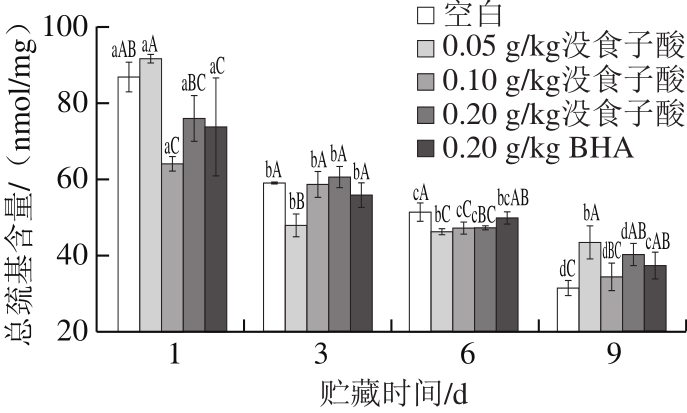
图 2 没食子酸对冷藏猪肉糜总巯基含量的影响
Fig. 2 Effect of gallic acid on total sulfhydryl group content of pork patties during chilled storage
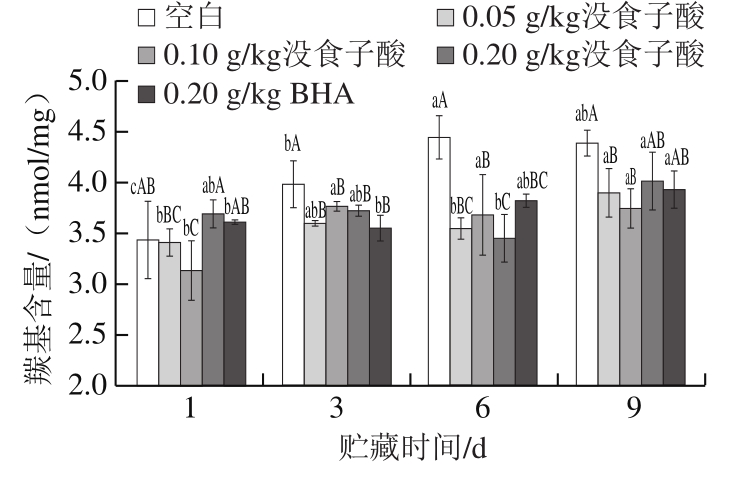
图 3 没食子酸对冷藏猪肉糜羰基含量的影响
Fig. 3 Effect of gallic acid on protein carbonyl content of pork patties during chilled storage
羰基含量常被用来评价蛋白质氧化程度[20-22]。由图3可知,随着贮藏时间的延长,空白组猪肉糜的羰基含量增加幅度最大,在第9天虽略有下降,但和第6天比差异不显著(P>0.05),说明在冷藏过程中,猪肉糜的蛋白质氧化程度不断加深。在贮藏第3天和第6天时,没食子酸和BHA处理组的羰基含量均显著低于空白组(P<0.05),说明没食子酸能有效抑制蛋白质羰基化合物的生成,而不同添加量之间差异不显著(P>0.05)。贮藏第9天时,没食子酸和BHA处理组的羰基含量也低于空白组,但0.20 g/kg没食子酸组和0.20 g/kg BHA组与空白组差异不显著(P>0.05)。这是由于没食子酸添加量较低时,能够发挥其羟自由基清除作用,阻碍蛋白质羰基化进程,这与Utrera等[23]研究结果一致,并且Utrera在研究中指出,没食子酸能抑制羰基化合物α-氨基己二酸半醛(aminoadipate semialdehyde,AAS)和α-氨基己二酸(aminoadipic acid,AAA)的生成。
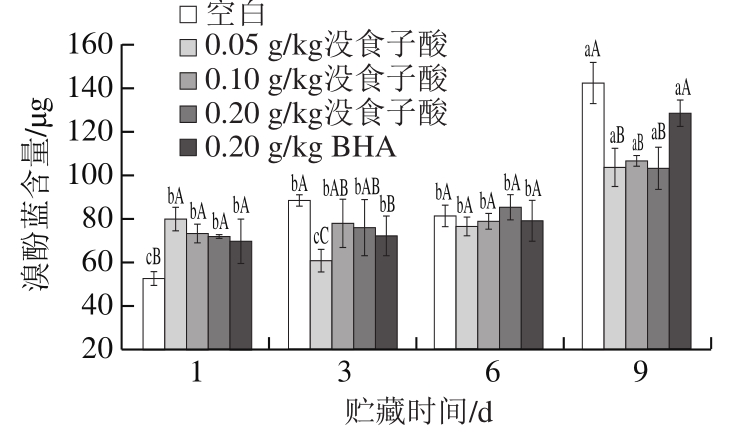
图 4 没食子酸对冷藏猪肉糜表面疏水性的影响
Fig. 4 Effect of gallic acid on surface hydrophobicity of pork patties during chilled storage
蛋白质分子的表面疏水性与其功能特性密切相关。由图4可知,随着贮藏时间延长,各处理组猪肉糜的表面疏水性整体呈上升趋势,尤其是空白组在贮藏第9天时大幅度增加,说明蛋白质稳定性变差。在贮藏初期(第1天),没食子酸和BHA处理组猪肉糜的表面疏水性显著高于空白组(P<0.05),这可能是由于没食子酸或BHA与蛋白质相互作用,促进蛋白质构象发生改变,导致部分疏水基团暴露,表面疏水性升高[24-25]。贮藏时间延长至贮藏后期(第9天),没食子酸组猪肉糜的表面疏水性显著低于空白组(P<0.05),说明贮藏过程中,没食子酸能够减少疏水性氨基酸残基的暴露,降低表面疏水性的增加程度[26]。这与Rawel等[27]的研究结果一致,没食子酸能够降低大豆蛋白的表面疏水性,主要是由于没食子酸与大豆蛋白相互作用改变蛋白质构象,且与疏水性基团相结合,促使亲水性羧基残基暴露,从而使表面疏水性降低。
表 1 没食子酸对冷藏猪肉糜色差的影响
Table 1 Effect of gallic acid on color of pork patties during chilled storage
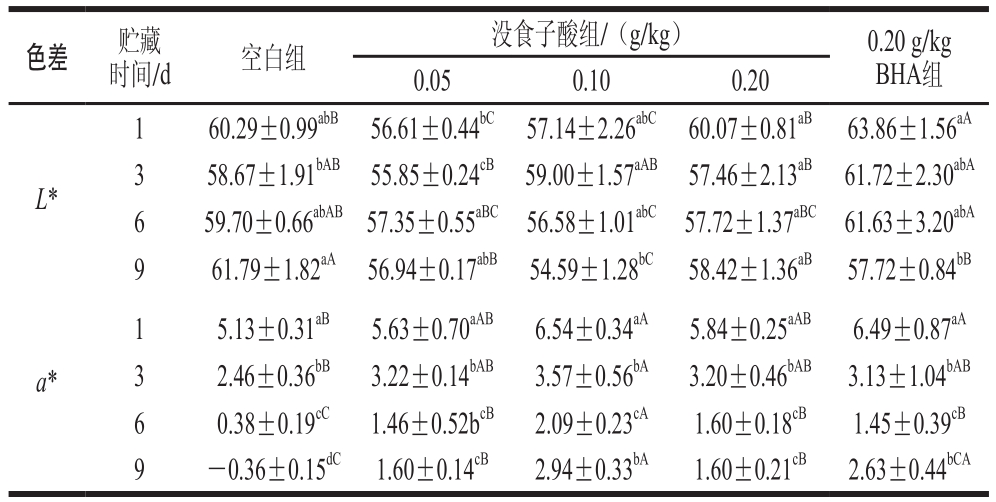
注:同列小写字母不同,表示同一处理组、不同冷藏时间差异显著(P<0.05);同行大写字母不同,表示同一冷藏时间、不同处理组差异显著(P<0.05)。
色差 贮藏时间/d 空白组 没食子酸组/(g/kg) 0.20 g/kg BHA组0.05 0.10 0.20 L*1 60.29±0.99abB 56.61±0.44bC 57.14±2.26abC 60.07±0.81aB 63.86±1.56aA 3 58.67±1.91bAB 55.85±0.24cB 59.00±1.57aAB 57.46±2.13aB 61.72±2.30abA 6 59.70±0.66abAB 57.35±0.55aBC 56.58±1.01abC 57.72±1.37aBC 61.63±3.20abA 9 61.79±1.82aA 56.94±0.17abB 54.59±1.28bC 58.42±1.36aB 57.72±0.84bB 1 5.13±0.31aB 5.63±0.70aAB 6.54±0.34aA 5.84±0.25aAB 6.49±0.87aA 3 2.46±0.36bB 3.22±0.14bAB 3.57±0.56bA 3.20±0.46bAB 3.13±1.04bAB 6 0.38±0.19cC 1.46±0.52bcB 2.09±0.23cA 1.60±0.18cB 1.45±0.39cB 9 -0.36±0.15dC 1.60±0.14cB 2.94±0.33bA 1.60±0.21cB 2.63±0.44bCA a*
肉及肉制品的色泽是决定消费者是否接受的评判标准之一。由表1可知,随着贮藏时间延长,空白组猪肉糜的L*先下降后上升。可能是由于贮藏初期猪肉糜表面水分不断蒸发损失,光泽度下降,因此L*下降;随着贮藏时间延长,猪肉糜中蛋白质氧化变性,持水能力下降,致使猪肉糜内部的水分外渗到肉糜表面,增大了光的反射度,从而促使L*增加[28]。贮藏第9天时,没食子酸和BHA组猪肉糜的L*显著低于空白组(P<0.05),说明没食子酸与蛋白质相互作用,有利于水分的保持,减少水分渗出到表面。贮藏前6 d,空白组和没食子酸组猪肉糜的a*显著下降(P<0.05),说明贮藏时间越长,肌红蛋白逐渐被氧化成高铁肌红蛋白,导致肉糜颜色变暗,a*下降[28]。贮藏后期,没食子酸和BHA组猪肉糜的a*显著高于空白组(P<0.05),说明没食子酸和BHA能防止肌红蛋白被氧化成高铁肌红蛋白。有研究表明,迷迭香提取物能抑制法兰克福香肠脂肪氧化和蛋白氧化的程度,从而改善香肠的色泽及质地[29]。
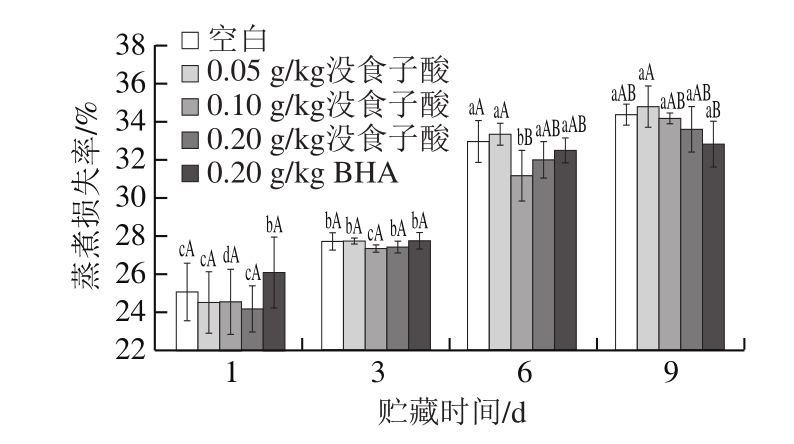
图 5 没食子酸对冷藏猪肉糜蒸煮损失的影响
Fig. 5 Effect of gallic acid on cooking loss of pork patties during chilled storage
由图5可知,随着贮藏时间延长,各组猪肉糜的蒸煮损失率均显著增加(P<0.05),说明贮藏时间越长,蛋白质的保水能力越低。仅贮藏第6天、没食子酸添加量为0.10 g/kg组的蒸煮损失率显著低于空白组(P<0.05),其他各贮藏时间、各添加量组与空白组之间差异均不显著(P>0.05),说明没食子酸不能有效降低肉糜的蒸煮损失,这可能是由于没食子酸与蛋白质的相互作用破坏了蛋白质的凝胶网络结构,抑制蛋白质之间相互交联,从而降低了蛋白质的持水能力。有研究表明,绿茶提取物能抑制蛋白质的交联能力,且高浓度绿茶提取物增加了肉糜乳化体系的蒸煮损失[30],这与本研究的结果相似。
空白组猪肉糜在冷藏过程中(4 ℃,9 d),TBARs值由0.20 mg/kg显著增加至0.85 mg/kg,而没食子酸和BHA显著降低了脂肪氧化程度;空白组猪肉糜的蛋白质总巯基含量在冷藏过程中显著降低,没食子酸和BHA在贮藏第9天能有效降低总巯基的损失程度;空白组猪肉糜的羰基含量和表面疏水性显著增加,没食子酸和BHA能减少羰基化合物的生成及表面疏水性增加的程度;在猪肉糜色泽方面,贮藏后期,没食子酸组的L*显著低于空白组,而a*显著高于空白组;在蒸煮损失方面,空白组与处理组猪肉糜无显著差异。因此,没食子酸可作为肉品抗氧化剂,抑制脂肪和蛋白氧化,并赋予肉制品良好的品质。
[1] 王乐田, 贾娜. 植物多酚对肉制品脂肪氧化和蛋白氧化的抑制机理及应用[J]. 中国食品学报, 2016, 16(8): 205-210. DOI:10.16429/j.1009-7848.2016.08.028.
[2] 马玉红. 脂质过氧化反应的研究[J]. 青海畜牧兽医杂志, 2007, 37(5):38-40. DOI:10.3969/j.issn.1003-7950.2007.05.023.
[3] FELLENBERG M A, SPEISKY H. Antioxidants: their effects on broiler oxidative stress and its meat oxidative stability[J]. World Poultry Science Journal, 2006, 62(1): 53-70. DOI:10.1079/wps200584.
[4] 袁凯, 张龙, 谷东陈, 等. 肉品中的蛋白质氧化机制及其影响因素[J].食品科学, 2018, 39(5): 329-335. DOI:10.7506/spkx1002-6630-201805048.
[5] 张秋会, 孙灵霞, 李苗云, 等. 肉制品的抗氧化控制措施[J]. 肉类研究, 2009, 23(7): 33-36. DOI:10.3969/j.issn.1001-8123.2009.07.012.
[6] 梁云. 几种天然抗氧化剂抗氧化性能比较研究[D]. 无锡: 江南大学,2008: 1-7. DOI:10.7666/d.y1398352.
[7] 丁阳平, 张曦, 周洁, 等. 没食子酸及其衍生物对α-淀粉酶作用机制研究[J]. 食品工业科技, 2012(2): 167-169. DOI:10.13386/j.issn1002-0306.2012.02.061.
[8] PRISCILLA D H, PRINCE P S M. Cardioprotective effect of gallic acid on cardiac troponin-T, cardiac marker enzymes, lipid peroxidation products and antioxidants in experimentally induced myocardial infarction in Wistar rats[J]. Chemico-Biological Interactions, 2009,179(2): 118-124. DOI:10.1016/j.cbi.2008.12.012.
[9] CAO Y, TRUE A D, CHEN J, et al. The dual role (anti- and prooxidant) of gallic acid in mediating myofibrillar protein gelation and gelin vitro digestion[J]. Journal of Agricultural and Food Chemistry,2016, 64(15): 3054-3061. DOI:10.1021/acs.jafc.6b00314.
[10] PARK D, XIONG Y L, ALDERTON A L. Concentration effects of hydroxyl radical oxidizing systems on biochemical properties of porcine muscle myofibrillar protein[J]. Food Chemistry, 2007, 101(3):1239-1246. DOI:10.1016/j.foodchem.2006.03.028.
[11] JONGBERG S, TØRNGREN M A, GUNVIG A, et al. Effect of green tea or rosemary extract on protein oxidation in Bologna type sausages prepared from oxidatively stressed pork[J]. Meat Science, 2013, 93(3):538-546. DOI:10.1016/j.meatsci.2012.11.005.
[12] ELLMAN G L. Tissue sulfhydryl groups[J]. Archives of Biochemistry and Biophysics, 1959, 82(1): 70-77. DOI:10.1016/0003-9861(59)90090-6.
[13] ORTUÑO J, SERRANO R, JORDÁN M J, et al. Shelf life of meat from lambs given essential oil-free rosemary extract containing carnosic acid plus carnosol at 200 or 400 mg/kg[J]. Meat Science,2014, 96(4): 1452-1459. DOI:10.1016/j.meatsci.2013.11.021.
[14] CHELH I, GATELLIER P, SANTÉ-LHOUTELLIER V. Technical note: a simplified procedure for myofibril hydrophobicity determination[J]. Meat Science, 2006, 74(4): 681-683. DOI:10.1016/j.meatsci.2006.05.019.
[15] DE JONG S, LANARI M C. Extracts of olive polyphenols improve lipid stability in cooked beef and pork: contribution of individual phenolics to the antioxidant activity of the extract[J]. Food Chemistry,2009, 116(4): 892-897. DOI:10.1016/j.foodchem.2009.03.053.
[16] YEN G C, DUH P D, TSAI H L. Antioxidant and pro-oxidant properties of ascorbic acid and gallic acid[J]. Food Chemistry, 2002,79(3): 307-313. DOI:10.1016/s0308-8146(02)00145-0.
[17] SOSZYŃSKI M, BARTOSZ G. Effect of postirradiation treatment on the radiation-induced haemolysis of human erythrocytes[J].International Journal of Radiation Biology, 1997, 71(3): 337-343.DOI:10.1080/095530097144229.
[18] YOO K M, LEE C H, LEE H, et al. Relative antioxidant and cytoprotective activities of common herbs[J]. Food Chemistry, 2008,106(3): 929-936. DOI:10.1016/j.foodchem.2007.07.006.
[19] 孔保华, 孙妍, 熊幼翎. 抗氧化剂对羟自由基引起的乳清分离蛋白氧化抑制效果的研究[J]. 食品科学, 2010, 31(3): 5-10. DOI:10.7506/spkx1002-6300-201003002.
[20] PARK D, XIONG Y L, ALDERTON A L. Concentration effects of hydroxyl radical oxidizing systems on biochemical properties of porcine muscle myofibrillar protein[J]. Food Chemistry, 2007, 101(3):1239-1246. DOI:10.1016/j.foodchem.2006.03.028.
[21] COOMBS C E O, HOLMAN B W B, COLLINS D, et al. Effects of chilled-then-frozen storage (up to 52 weeks) on an indicator of protein oxidation and indices of protein degradation in lambM.longissimus lumborum[J]. Meat Science, 2018, 135: 134-141. DOI:10.1016/j.meatsci.2017.09.013.
[22] CHAMBA M V M, HUA Y, KATIYO W. Oxidation and structural modification of full-fat and defatted flour based soy protein isolates induced by natural and synthetic extraction chemicals[J]. Food Biophysics, 2014, 9(3): 193-202. DOI:10.1007/s11483-014-9333-8.
[23] UTRERA M, ESTÉVEZ M. Impact of trolox, quercetin, genistein and gallic acid on the oxidative damage to myofibrillar proteins: the carbonylation pathway[J]. Food Chemistry, 2013, 141(4): 4000-4009.DOI:10.1016/j.foodchem.2013.06.107.
[24] LIU G, XIONG Y, BUTTERFIELD D. Chemical, physical, and gel-forming properties of oxidized myofibrils and whey-and soyprotein isolates[J]. Journal of Food Science, 2000, 65(5): 811-818.DOI:10.1111/j.1365-2621.2000.tb13592.x.
[25] BRANDS C M J, VAN BOEKEL M A J S. Kinetic modeling of reactions in heated monosaccharide? Casein systems[J]. Journal of Agricultural and Food Chemistry, 2002, 50(23): 6725-6739.DOI:10.1021/jf011164h.
[26] 贾娜, 刘丹, 张晓星, 等. 氧化条件下没食子酸对猪肉肌原纤维蛋白结构及凝胶特性的影响[J]. 食品工业科技, 2016, 37(23): 61-66.DOI:10.13386/j.issn1002-0306.2016.23.003.
[27] RAWEL H M, CZAJKA D, ROHN S, et al. Interactions of different phenolic acids and flavonoids with soy proteins[J]. International Journal of Biological Macromolecules, 2002, 30(3): 137-150.DOI:10.1016/S0141-8130(02)00016-8.
[28] HUR S J, PARK G B, JOO S T. Effect of storage temperature on meat quality of muscle with different fiber type composition from korean native cattle (Hanwoo)[J]. Journal of Food Quality, 2009, 32(3):315-333. DOI:10.1111/j.1745-4557.2009.00259.x.
[29] ESTÉVEZ M, VENTANAS S, CAVA R. Protein oxidation in frankfurters with increasing levels of added rosemary essential oil:effect on color and texture deterioration[J]. Journal of Food Science,2005, 70(7): c427-c432. DOI:10.1111/j.1365-2621.2005.tb11464.x.
[30] JONGBERG S, TERKELSEN L S, MIKLOS R, et al. Green tea extract impairs meat emulsion properties by disturbing protein disulfide cross-linking[J]. Meat Science, 2015, 100: 2-9. DOI:10.1016/j.meatsci.2014.09.003.
Effect of Gallic Acid on Inhibition of Lipid and Protein Oxidation and Quality of Pork Patties during Chilled Storage
贾娜, 孙嘉, 王乐田, 等. 没食子酸对猪肉糜脂肪和蛋白氧化的抑制作用及对肉糜品质特性的影响[J]. 肉类研究, 2019,33(3): 1-6. DOI:10.7506/rlyj1001-8123-20181228-243.http://www.rlyj.net.cn
JIA Na, SUN Jia, WANG Letian, et al. Effect of gallic acid on inhibition of lipid and protein oxidation and quality of pork patties during chilled storage[J]. Meat Research, 2019, 33(3): 1-6. DOI:10.7506/rlyj1001-8123-20181228-243.http://www.rlyj.net.cn