氢化物原子荧光法与石墨炉原子吸收法测定肉制品中微量铅
张 曦
(中国肉类食品综合研究中心,北京 100068)
摘 要:采用湿法消解技术作为前处理方式,确定了消解试剂和消解条件,利用氢化物原子荧光法及石墨炉原子吸收法,对肉制品中的铅微量元素进行测定并做比较研究。结果表明:2种方法回收率、精密度和检出限均能满足日常检测要求。随着荧光技术的发展,相对于原子吸收较为便宜的价格,在微量铅测定方面,荧光法更值得推荐。
关键词:肉制品;铅;氢化物原子荧光法;石墨炉原子吸收法
铅是一种常见的重金属污染物,广泛存在于大气、土壤、水和食物中。它是人体唯一不需要的微量元素,也是一种稳定的不可降解污染物,在环境中可长期积累,并且易通过消化道、呼吸道而被人体吸收,铅在进入生物体内后不易被排出,在食物链的生物放大作用十分明显,其富集系数在各营养级中可达到惊人的程度,较高营养级的生物会在体内成千万倍的富集铅,然后通过食物链进入人体,当摄入过量时,会对神经系统、消化系统和造血系统造成危害,铅污染已成为当前危害健康的重要原因之一
[1-4]。研究表明,在过去50年里,全球排放到环境中的铅为783 000 t,其中有相当一部分进入了土壤,致使世界土壤出现不同程度的污染
[5-6]。动物与人类生活在同一个生态环境中,由于家畜从体格上讲呼吸带都处于大气铅浓度较高的层次,再加上各种饲料通过食物链带入的铅污染等,以至肉制品一定程度上承受着铅污染带来的问题
[7]。2010—2012年达州市的监测研究发现,畜肉等群众经常消费的食品中铅合格率低于80%
[8]。目前食品中铅的主要检测方法有原子吸收法、电感耦合等离子体发射光谱法(inductively coupled plasma optical emission spectrometry,ICP-OES)、电感耦合等离子体质谱法(inductively coupled plasma mass spectrometry,ICPMS)等。近年来,肉与肉制品中铅的检测方法屡见报道,卢垣宇等
[8]采用干法消解比较了石墨炉原子吸收与ICP-MS测定肉制品和香辛料中的铅含量。梁绍成等
[9]采用微波消解ICP-OES法对动物源性食品中的铅镉砷汞含量进行了测定。本研究采用氢化物原子荧光法与石墨炉原子吸收法对肉制品中微量铅的含量进行测定,并对2 种方法的回收率、精密度、检出限进行考察,以期为肉制品铅含量检测提供参考。
1 材料与方法
1.1 材料与试剂
猪肉制品 市购;牛肝成分分析标准物质GBW(E)080193、铅标准溶液 国家标准物质研究中心;氢氧化钾、硼氢化钾、铁氰化钾、硝酸镁、磷酸氢二铵、硝酸钯 国药集团化学试剂有限公司。
1.2 仪器与设备
AFS-930双道原子荧光光度计、铅空心阴极灯 北京吉天仪器有限公司;TAS-990原子吸收分光光度计北京普析通用仪器有限责任公司;
1.3 方法
1.3.1 前处理
消解液:用天平称取1.000 g肉制品于磨口三角瓶中,消解试剂为浓硝酸和高氯酸混合液(7∶1,V/V),加入玻璃珠数粒及漏斗,放置电热板上消化至液体无色澄清、大量白烟冒出,加入10 mL超纯水赶酸至液量为1~2 mL,待三角瓶冷却用超纯水转移定容于25 mL容量瓶中。
氢化物原子荧光法:取1 mL消解液,添加12 mol/L盐酸溶液定容至10 mL,待测;石墨炉原子吸收法:取10 μL消解液,加不同基体改进剂5 μL(0.05% Mg(NO
3)
2溶液、0.5% NH
4H
2PO
4溶液、0.05% Pd(NO
3)
2溶液),待测。
1.3.2 氢化物原子荧光法条件
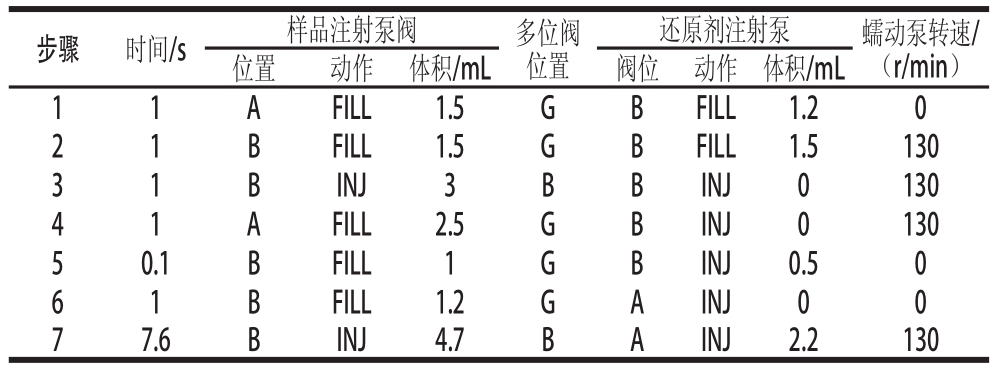
波长283.3 nm,灯电流90 mA,光电倍增管负高压280 mA,原子化器高度8 mm,载气流量(氩气)400 mL/min,屏蔽气流量(氩气)800 mL/min,读数时间7.6 s,延时1.5 s,进样量0.5 mL,读数方式为峰面积,顺序注射系统程序见表1。
表1 氢化物原子荧光法测定铅顺序注射系统程序
Table 1 Sequential injection system program for determination of lead by HG-AFS
步骤时间/s样品注射泵阀多位阀位置还原剂注射泵蠕动泵转速/(r/min)位置动作体积/mL阀位动作体积/mL 11AFILL1.5GBFILL1.20 21BFILL1.5GBFILL1.5130 31BINJ3BBINJ0130 41AFILL2.5GBINJ0130 50.1BFILL1GBINJ0.50 61BFILL1.2GAINJ00 77.6BINJ4.7BAINJ2.2130
1.3.3 石墨炉原子吸收法条件
波长283.3 nm,灯电流 3 mA,负高压440 mA,狭缝宽度0.4 nm,氘灯扣背景,进样量10 μL,基体改进剂5 μL,程序升温条件:干燥温度110 ℃,升温5 s,保持5 s;灰化温度350 ℃,升温10 s,保持10 s;原子化温度1 600 ℃,升温0 s,保持3 s;清除温度1 800 ℃,升温1 s,保持3 s。
2 结果与分析
2.1 消解条件确定
2.1.1 消解方法
由表2可知,干灰化法测定样品中的铅含量都有所偏低,由于灰化时间对其含量有所影响。灰化时间过短,样品未灰化完全;灰化时间过长时,样品中部分铅及其化合物汽化后挥发而使测得的铅含量偏低。故本实验确定湿法消解作为前处理方法。湿法消解是目前应用比较广泛的一种食品药品等重金属元素检测的前处理方法
[10-11],该方法实用性强,在实验过程中只要控制好消化温度,大部分元素很少或几乎没有损失,尤其对于铅这样的高温元素,回收率较为稳定
[12-13]。王吉秀等
[14]比较了湿法、微波以及干法消解测定中药材中的5种重金属元素,结果表明,消解方法的回收率均大于90%。
表2 不同前处理方法测定肉制品中的铅含量
Table 2 Comparison of results obtained by different pretreatment methods for the determination of lead content in meat products mg/kg

注:样品1~4为不含待测染素基质的肉制样品。
前处理样品1样品2样品3样品4消解方法0.0280.0360.0190.0104干灰化法0.0250.0340.0180.0099
2.1.2 消解体系
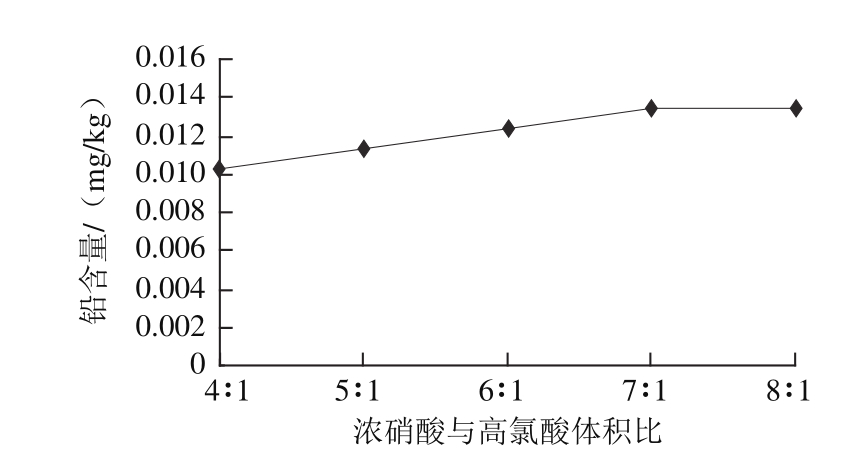
图1 消解体系对铅测定结果的影响
Fig.1 Effect of digestion system on the determination of lead
由图1可看出,当混酸比例为4∶1~7∶1(V/V),铅含量逐渐上升,7∶1(V/V)之后基本不变,故最终采用浓硝酸和高氯酸混合液(7∶1,V/V)作为消解试剂。
早在六七十年代就有文献报道运用高氯酸消解的方法测定组织,土壤以及植物中的多种元素含量
[15-18]。由于日常检测的肉制品中油脂含量较高,故将消解试剂中浓硝酸的比例加大,在反应初期起预氧化作用的浓硝酸与肉制品充分反应,破坏样品中有机质。热高氯酸是最强的氧化剂和脱水剂,由于其沸点较高,可在除去硝酸后的反应后期继续氧化肉制品,达到充分消解的目的
[19]。
氢化物原子荧光法对酸度要求比较苛刻,由于铅形成挥发性气体的酸度范围很窄,所以加水赶酸应等待至大量白烟冒出为止。江锐曙等
[20]选择2%盐酸溶液作为载流测定铅,可提高荧光强度,获得较高的灵敏度和精密度。
2.2 氢化物原子荧光法测定结果
选用铁氰化钾作为氧化剂,标准溶液和试样不需另加试剂,载流为12 mol/L盐酸溶液。根据样品酸度,调节还原剂中碱溶液浓度,以确保最终反应废液pH值为8~9左右。最终确定还原剂为1%氢氧化钾、2%硼氢化钾、2%铁氰化钾。在此条件下由仪器自动稀释配比测定1.000、2.000、4.000、8.000、10.00 ng/mL标准使用液,得标准曲线I=139.482 1C―6.837 9,相关系数0.999 9。
2.3 石墨炉原子吸收光谱法测定结果
肉制品复杂的基体组分对石墨炉原子吸收光谱法的测定有严重的背景干扰,在测定过程中较高的空白值会对肉制品中微量铅的测定产生较大影响,因此,需要加基体改进剂以获得低含量测定值。加入基体改进剂可改善基体的性能,使其易转化成为易挥发的化学形态,以利于灰化阶段的去除;同时,与分析物形成更稳定的化合物,降低分析物的挥发性,提高灰化温度和原子化温度,利于除去基体的干扰,避免分析元素与Cl
–形成共挥发物
[20-22]。
本研究选择0.05% Mg(NO
3)
2溶液、0.5% NH
4H
2PO
4溶液、0.05% Pd(NO
3)
2溶液3种基体改进剂,对高盐肉制品微量铅的测定进行比较。结果显示,当加入5 μL质量分数为0.05% Pd(NO
3)
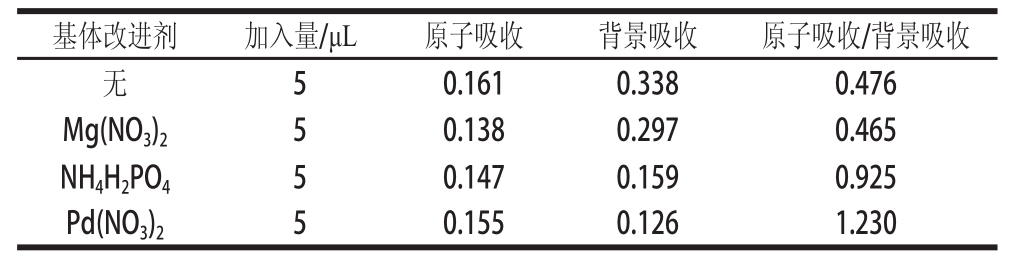
2溶液时,背景值最小为0.126,其信噪比值最高(表4)。由于钯价格较昂贵,故在实际应用过程中,基体改进剂多采用0.5% NH
4H
2PO
4溶液。
表4 不同基体改进剂对样品吸光度与背景吸光度的影响
Table 4 Effect of different matrix modifiers on absorbance and background absorbance
基体改进剂加入量/μL原子吸收背景吸收原子吸收/背景吸收无5 0.1610.3380.476 Mg(NO
3)
250.1380.2970.465 NH
4H
2PO
450.1470.1590.925 Pd(NO
3)
250.1550.1261.230
在此条件下,测定10.00、20.00、40.00、80.00 ng/mL标准使用液,得标准曲线Y=376.811 2C―29.837 6,相关系数0.999 3。
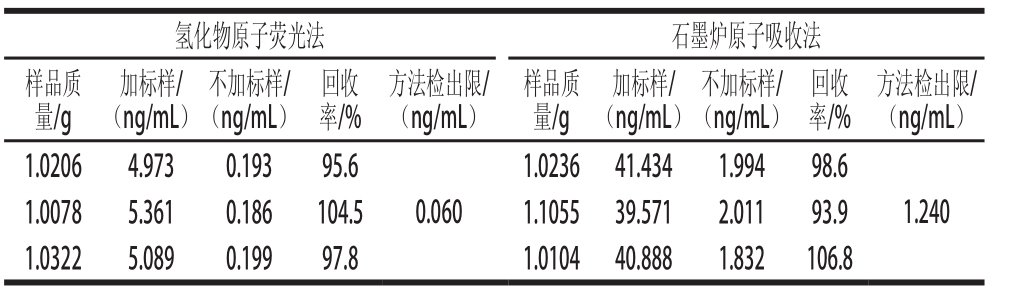
表5 不同测定方法加标回收率及方法检出限
Table 5 Spiked recoveries and detection limits of GFAAS and HG-AFS
氢化物原子荧光法石墨炉原子吸收法样品质量/g方法检出限/(ng/mL)1.02064.9730.19395.6 0.060加标样/(ng/mL)不加标样/(ng/mL)回收率/%方法检出限/(ng/mL)样品质量/g加标样/(ng/mL)不加标样/(ng/mL)回收率/% 1.023641.4341.99498.6 1.00785.3610.186104.51.105539.5712.01193.9 1.03225.0890.19997.81.010440.8881.832106.8 1.240
由表5可看出,对空白样品做11 次测定,使用氢化物原子荧光法,用R
SN=3确定方法检出限为0.060 ng/mL;以4 ng/mL为标准样品进行11 次测定,计算相对标准偏差为1.08%;以5 ng/mL做加标回收实验,测量3 次,回收率在95.6%~104.5%之间。使用石墨炉原子吸收法,用R
SN=3确定方法检出限为1.240 ng/mL;以40 ng/mL为标准样品进行11 次测定,由仪器自动计算浓度值,计算其相对标准偏差为1.49%;以40 ng/mL做加标回收实验,测量3 次,回收率在93.9%~106.8%之间。
两种方法均能满足日常检测的需求,氢化物原子荧光法具有更低方法检出限、较高灵敏度,样品消解之后直接稀释即可上机。而石墨炉原子吸收法受肉制品复杂基体的影响较大,需要加入基体改进剂进行试验,进而增加了污染的可能性。
2.4 标准物质测定
分别用氢化物原子荧光法和石墨炉原子吸收法对国家标准物质GBW(E)080193进行测定,铅含量各为1.29、1.28 mg/kg,回收率为99.2%、98.5%,测定值在证书给定范围内。
2.5 实际样品的测定
利用上述方法,对北京市城区、远郊超市及农贸市场中185 个批次的肉及肉制品进行了分析,结果表明其铅含量在0.009 8~0.048 mg/kg范围内。
3 结 论
氢化物原子荧光法检出限0.060 ng/mL,相对标准偏差1.08%,回收率95.6%~104.5%;石墨炉原子吸收法检出限1.240 ng/mL,相对标准偏差1.49%,回收率为93.9%~106.8%。对国家标准物质GBW(E)080193铅成分进行测定,其测定值在证书给定范围内。
石墨炉原子吸收法费时,选用合适的基体改进剂进行测定其受酸度的干扰较小;氢化物原子荧光法仪器价格便宜,耗时短,但铅形成挥发性气体的酸度范围很窄,故要严格控制消化后样品的酸度,尽量将酸赶尽,并且使标样介质的酸度与消化后样品的酸度保持一致。
两种方法均能满足日常检测的需求,氢化物原子荧光法具有较高的灵敏度、仪器性能稳定、操作简便,随着荧光技术的发展,相对于原子吸收较为便宜的价格,在微量铅测定方面,荧光法更值得推荐。
参考文献:
[1] 陈少芳, 谭国浩, 陈秀芳. 氢化物原子荧光法与石墨炉原子吸收法测定微量铅[J]. 中国卫生检验杂志, 2009, 19(5): 1049-1050.
[2] 梁进. 氢化物原子荧光法与石墨炉原子吸收法测定水中微量铅比较[J]. 现代仪器, 2006(5): 325-327.
[3] 李华斌, 戚其平, 姚孝元, 等. 铅对健康的影响研究进展[J]. 环境导报, 1999(1): 32-35.
[4] 钟格梅, 唐振柱. 我国环境中镉、铅、砷污染及其对暴露人群健康影响的研究进展[J]. 环境与健康杂志, 2006, 23(6): 562-565.
[5] WEBSTER R, OLIVER M A. Sample adequately to estimate variorums of soil properties[J]. Journal of Soil Science, 1992, 43: 177-192.
[6] SINGH O V, LABANA S, PANDEY G, et al. Phytoremeation: an overview of metallic ion decontamination from soil[J]. Applied Microbiology and Biotechnology, 2003, 61(5/6): 492-405.
[7] 王卓, 张兴伍, 李德华, 等. 2010年-2012年达州市食品中重金属及有害元素监测结果分析[J]. 中国卫生检验杂志, 2013(17): 3404-3409.
[8] 卢垣宇, 寻思颖, 冯永渝, 等. 干法消解-石墨炉原子吸收及电感耦合等离子体质谱测定肉制品和香辛料中铅含量的比较[J]. 食品科技, 2013, 38(12): 290-293.
[9] 梁绍成, 刘君超, 赵智峰, 等. 微波消解-ICP-OES法测定动物源食品中铅, 镉, 砷和汞含量的方法研究[J]. 中外食品工业: 下, 2013(5): 18-19.
[10] 方炳华, 肖珊美. 湿法消化-火焰原子吸收光谱法测定植株中矿质元素[J]. 中国林副特产, 2005, 78(5): 5-6.
[11] 王洪春. 食品类样品硝酸高氯酸湿法消化的实验现象与消化进程控制[J]. 预防医学情报杂志, 2005, 21(6): 764-765.
[12] 陈韫仪. 湿法消化氢化物原子荧光光谱法测定茶叶中的铅含量[J].福建轻纺, 2012, 7(5): 30-34.
[13] 曾晓丹, 王建刚, 张颖慧, 等. 湿法消解-原子荧光光谱法测定人参皂甙中的重金属元素[J]. 光谱实验室, 2011, 28(3): 1085-1088.
[14] 王吉秀, 祖艳群, 陈海燕, 等. 中药材圆果中重金属检测的消解方法研究[J]. 云南农业大学学报, 2011, 26(6): 856-860.
[15] ZASOSKI R J, BURAU R G. A rapid nitric: perchloric acid digestion method for multi-element tissue analysis[J]. Communications in Soil Science and Plant Analysis, 1977, 8(5): 425-436.
[16] KOPACEK J, HEJZLAR J. Semi-micro determination of total phosphorus in soils, sediments, and organic materials: a simplified perchloric acid digestion procedure[J]. Communications in Soil Science and Plant Analysis, 1995, 26(11/12): 1935-1946.
[17] BLANCHAR R W, GEORGE R, CALDWELL A C. Sulfur in plant materials by digestion with nitric and perchloric acid[J]. Soil Science Society of America Journal, 1965, 29(1): 71-72.
[18] 麦洁梅, 成晓玲, 张琪. 氢化物发生-原子荧光光谱法测定铅的最佳酸度条件选择[J]. 中国卫生检验杂志, 2007, 17(7): 1225-1226.
[19] 陈庆胜, 李敏. 食品检验湿法消解过程和机理探讨[J]. 中国中医药咨讯, 2010, 2(14): 259.
[20] 江锐曙, 蔡志斌. 食品痕量元素分析中基体改进剂的应用[J]. 中国卫生检验杂志, 2009, 19(6): 1446-1448.
[21] 胡海蓉. GFAAS法测定酱油镉含量中基体改进剂的应用[J]. 中国卫生检验杂志, 2009, 20(6): 1378-1379.
[22] 肖艳玲, 冯跃华, 卢黄, 等. 基体改进剂在石墨炉原子吸收法测定食品中铅的应用[J]. 安徽师范大学学报: 自然科学版, 2010, 33(1): 48-51.
Determination of Trace Lead in Meat Products by HG-AFS in Comparison with GFAAS
ZHANG Xi
(China Meat Research Center, Beijing 100068, China)
Absract: In this study, the digestion reagents and conditions were optimized for wet digestion as a sample pre-treatment for comparative determination of trace lead in meat products by hydride generation atomic fluorescence spectrometry (HGAFS) and graphite furnace atomic absorption spectrometry (GFAAS). The results showed that both methods could meet the analytical requirements of recovery, precision and limit of detection. However, GFAAS is a more recommendable method due to its cost advantage.
Key words:meat; lead; hydride generation atomic fluorescence spectrometry (HG-AFS); graphite furnace atomic absorption spectrometry (GFAAS)
中图分类号:TS252.7
文献标志码:A
文章编号:1001-8123(2014)03-0014-04
收稿日期:2014-01-21
作者简介:张曦(1985—),女,工程师,硕士,研究方向为食品检测。E-mail:0415zx@sina.com




